Evaluación de patrones de inflamación durante la ...
Transcript of Evaluación de patrones de inflamación durante la ...

Evaluación de patrones de inflamación durante la exposición a extractos
etanólicos de plantas en peces cebra (Danio rerio)
Luisa Matiz Ceron - 201326928
Resumen
Los compuestos naturales (NP) surgen como potenciales sustancias para la extracción de
moléculas químicas de importancia farmacéutica. Haciendo necesaria la evaluación in vivo
e in vitro de los patrones de estas sustancias. Se ha sugerido a Pentacalia ledifolia y Conyza
trihecatatis como posibles fuentes para extraer compuestos anti inflamatorios, debido al
conocimiento etnobotánico de algunas poblaciones sobres estas especies. Con este
propósito, se sugirió el uso de peces cebra como modelo de estudio. En este estudio se
evaluaron los patrones de inflamación, a través de la migración de neutrófilos en peces
cebra, durante la exposición a extractos etanolicos de las plantas Pentacalia ledifolia y
Conyza trihecatatis. Se determinó el pico máximo de migración de neutrófilos en peces
cebra, 7 – 8 hours post injury (hpi), de igual forma se visualizó un posible un patrón de anti
inflamación para P. ledifolia y C. trihecatactis, reflejado en una menor migración de
neutrófilos, sin embargo, no se pudo estimar en qué medida este efecto era de los
compuestos del extracto etanólico debido al efecto anti inflamatorio que también
presentaba el solvente (DMSO). Se estableció que incluso a concentraciones muy bajas de
dimetilsulfoxido (DMSO) hay un efecto anti inflamatorio, que tiende a ser obviado en la
literatura. Este efecto está enmascarando el resultado de los extractos etanolicos de ambas
plantas, sin embargo, se sugiere un proceso aditivo o sinérgico para el complejo DMSO-
extracto etanólico. Así mismo, se evaluó otro solvente (etanol) para comprobar las
propiedades anti inflamatorias anteriormente vistas al usar DMSO, mostrando un patrón
de anti inflamación, sin embargo menos específico para ambas plantas.
Introducción
En la actualidad los productos naturales (NP) representan una significativa fuente de
compuestos químicos aun no explorados por la ciencia (Crawford et al., 2011). Estos
compuestos, adaptados a las necesidades de cada organismo, tras procesos evolutivos, y
presentes en extractos constituidos por varias moléculas químicas, representan una
oportunidad en el desarrollo de medicamentos y el entendimiento de procesos biológicos.
Diversas son las plantas que se han empezado a utilizar en ensayos de NP, siendo las de
América y África las escogidas por su diversidad y propiedades desconocidas. En nuestro

caso se plantea el uso de dos plantas del páramo colombiano, de las especies Pentacalia
ledifolia y Conyza trihecatatis. En el caso de plantas del género Conyza, estas son
normalmente usadas como cicatrizantes e insecticidas. Específicamente, Conyza
trihecatactis es empleada como reductor de fiebre, estimulante de la menstruación y para
tratamiento de reumatismo, como diurético, anti hipertensivas y beneficiosa en el
tratamiento de afecciones al miocardio. (Loutfy, 2009; Hernández-Arias, 2014). Otras
especies de este género, como Conyza bonariensis, se utilizan para curar contusiones por
su efecto anti inflamatorio (Guzmán-Tirado, 1997). Por otro lado, de acuerdo con la
información etnobotánica, campesinos cundiboyacenses usan las plantas del género
Pentacalia como desinfectantes y cicatrizantes en heridas de difícil curación. Además, es
usada contra la sífilis, en erupciones cutáneas, dolores de garganta y úlceras (Garibello,
2010).
Dentro de las investigaciones realizadas para la evaluación de NP con propiedades anti
inflamatorias, las familias de compuestos alcaloides, fenoles y terpenoides, representan
una oportunidad para la generación de nuevas alternativas contra la inflamación
incontrolada (Bellik, Hammoudi, Abdellah, Iguer-Ouada, & Boukraâ, 2012). De igual
manera, se ha demostrado la efectividad de las isoflavonas generando anti inflamación (Yu,
Bi, Yu, & Chen, 2016), así como los esteroides de origen vegetal (Barnes, 2006).
Específicamente para los extractos de plantas que se plantea evaluar, Pentacalia ledifolia y
Conyza trihecatatis, se conoce la presencia de diversos compuestos aislados e identificados.
Para el caso de P. ledifolia los compuestos identificados son en su mayoría isoflavonas
(Ramírez, 2011), mientras que para C. trihecatatis la mayoría de sus metabolitos
pertenecen al grupo de los labdanos (Hernández-Arias, 2014). Investigaciones recientes en
estas dos familias de compuestos los han caracterizado por tener propiedades anti
inflamatorias (De Rosa & Tommonaro, 2012; Harris et al., 2013; Kim, Li, Wu, Lee, & Ryu,
2013; Tran, Wong, & Chai, 2017). Sin embargo, para ninguna de las dos especies se conoce
su composición química en totalidad, por lo que los extractos botánicos de estas plantas
involucran una oportunidad para describir nuevos productos naturales.
La inflamación es una respuesta esencial del cuerpo hacia los agentes exógenos, su
propósito es eliminar los patógenos para prevenir infección, limpiar las células necróticas y
el tejido dañado (Martin & Feng, 2009). En la inflamación, el reclutamiento de glóbulos
blancos o leucocitos es esencial para prevenir la entrada de microorganismos y comenzar
el cierre de la lesión (Martin & Feng, 2009). Por esta razón, el entendimiento de la biología
de los leucocitos, y esencialmente de los neutrófilos, principales células inmunes
involucradas en la respuesta inflamatoria, se hace necesario. Los neutrófilos corresponden
a la porción más grande de leucocitos en el cuerpo y son los primeros en migrar, guiados
por varias señales químicas, ayudando a limitar la invasión del patógeno.

Aunque la inflamación corresponde a un proceso de gran poder para la remoción de
patógenos y prevención de la infección, en casos donde ocurre de forma excesiva o nunca
ocurre, el tejido termina con un gran daño. Las consecuencias clínicas de un proceso de
inflamación no resuelto siguen siendo problemáticas para la medicina moderna, por causar
afecciones como la enfermedad de obstrucción pulmonar, artritis inflamatoria y
glomerulonefritis (Henry et al., 2013). Por esta razón, entender cómo funciona este proceso
inmunológico y como contrarrestarlo es una oportunidad para los productos naturales.
Para realizar estudios acerca de la respuesta inflamatoria usando neutrófilos, es usual la
extracción de estos de la sangre periférica, sin embargo, su corta vida hace que el trabajo
sea difícil y complejo. De esta forma se sugiere el uso de modelos biológicos que permitan
la visualización de neutrófilos bajo manipulaciones químicas. El pez cebra, Danio rerio,
modelo biológico de uso en el campo de la biología del desarrollo, presenta ventajas debido
a su alta variabilidad genética, similitud farmacológica con los humanos, pequeño tamaño,
transparencia, rápido desarrollo y alto número de embriones, que corresponden a los
principales estadios usados para experimentación (Crawford, Esguerra, & De Witte, 2008).
En el caso del sistema inmune, el pez cebra comparte muchas características con los
sistemas presentes en mamíferos, incluyendo las células involucradas en la respuesta del
sistema innato (Petrie, Strand, Tsung-Yang, Rabinowitz, & Moon, 2014), así como señales
celulares muy conservadas entre vertebrados e invertebrados tales como Wnt/β-catenina
y NOTCH (Correa et al., 2004; Fazio & Ricciardiello, 2016; Ma & Hottiger, 2016), que están
relacionadas con reclutamiento de células pro-inflamatorias, factores de transcripción
durante este proceso y la comunicación de las células que participan en él. Específicamente
en el proceso inflamatorio, se ha afirmado que vertebrados e invertebrados comparten la
morfología, bio-química y características funcionales de los neutrófilos (Henry et al., 2013).
Aunque la escala de tiempo y donde se generan los grupos celulares ocurre de manera
diferente en ambos grupos, la funcionalidad y objetivo parecen ser los mismos.
Concretamente en peces cebra, la aparición de los neutrófilos ocurre a las 32-48 hpf (Henry
et al., 2013). En el estudio de procesos de desplazamiento de grupos celulares,
específicamente de neutrófilos, son usadas pruebas citoquímicas e inmunomarcación como
el tinte Sudan Black de características lipofílicas (Mathias et al., 2010), la marcación de MPO
(Myeloperoxidase), así como anticuerpos LP (L-Plastin). De igual forma, debido al pequeño
tamaño de los embriones y larvas, se ha fomentado el desarrollo de líneas transgénicas para
realizar rastreos celulares con promotores específicos de neutrófilos como lyz y mpx,
marcados con proteínas fluorescentes (Gray et al., 2011; Henry et al., 2013; Petrie et al.,
2014). Por todo lo anterior, en este estudio se realizó un análisis de los patrones de
inflamación de las plantas Pentacalia ledifolia y Conyza trihecatatis, con el propósito de
establecer su potencial anti inflamatorio, mediante el conteo de neutrófilos en el pez cebra
como modelo animal.

Metodología
1.Modelo biológico
1.1 Condiciones de mantenimiento de los peces en el bioterio.
El mantenimiento y desarrollo de los animales se realizó de acuerdo con la regulación
del laboratorio de Biología del desarrollo (BIOLDES) de la Universidad de los Andes.
Con los estándares de Guide for the Care and Use of Laboratory Animals. A partir de la
guía se establecieron los siguientes parámetros fisicoquímicos para este laboratorio:
conductividad 600-800 μS/cm, pH 7.0 a 7.6, temperatura 27° C, con un mínimo de
25°C y un máximo de 29 °C, ciclo de luz/oscuridad 14/10 y suplemento de oxigeno
entre 6,5 y 8 mg/L en un sistema de recirculación de agua de Aquaneering Inc. De
igual forma, los animales son alimentados dos veces por día usando micro-crustáceos
(Artemia), copépodos y un suplemento de alimento granulado. En los tanques se
mantiene un máximo de 8 peces por litro de agua, donde se encuentran debidamente
etiquetados con sus cepas de procedencia, fecha de nacimiento y género.
1.2 Obtención de los embriones de pez cebra
Con el propósito de generar las larvas necesarias para la experimentación se usaron
ejemplares adultos sexualmente activos de las cepas silvestres AB, TAB5, TL y WIK.
Los cruces se realizaron usando un macho y dos hembras por caja de las cepas
anteriormente mencionadas. Estos fueron colocados entre lunes y viernes luego de
las 3:30 pm en “cajas de cruce”, que son dejadas toda la noche y posteriormente,
recolectadas luego de las 9:30 am del siguiente día, con el propósito de dejar un lapso
entre el apareamiento, resultado del cambio oscuridad/luz. Con respecto al
apareamiento, este sucede de manera externa debido a la liberación de los ovocitos
por parte de la hembra y la deposición del esperma sobre ellos, por parte del macho.
Los huevos resultantes son colectados en cajas de Petri con agua de huevo (20 μL azul
de metileno, 1,5 mL stock de sales: 40 g sal marina Crystal Sea® Marinemix/1L agua
destilada, 1 litro de agua corriente) y se transfieren a una incubadora a una
temperatura de 28.5°C donde se desarrollarán hasta el estadio necesario (4-5 dpf) no
superior a los 5 dpf.
2. Experimentación
2.1 Despigmentación de embriones
Para la evaluación de la migración de leucocitos se requiere una baja cantidad de
melanocitos sobre el cuerpo de pez. Para lograr esto se usó feniltiourea (PTU, por sus
siglas en inglés) a 200 μM. El PTU es aplicado desde las 6 hpf, a una concentración de

200 μM y debe ser cambiado cada dos dias. A las 24 hpf se sugiere realizar un
procesimiento de decorionacion de los embriones de manera manual, debido a que
el PTU genera endurecimiento en el corion, lo que impide la salida de manera natural
(a las 48 hpf) por parte del embrión. El PTU inhibe la síntesis de la enzima tirosinasas
de manera reversible, lo cual impedirá la síntesis de melanina sobre el epitelio dermal
y ocular del pez. Se siguieron presentando los iridiforos y xantoforos en todo el cuerpo
del animal.
2.2 Anestesia y cortes de aleta caudal
Como modelo para fomentar y evaluar de los patrones de inflamación se usó una
lesión en la aleta caudal de las larvas. Para realizar los cortes de la aleta caudal se
aplicó una solución de tricaina 0.00168ppm en 24 mL de agua destilada, seguido de
un baño frio en hielo, durante no más de 5 min, para inmovilizar, pero no matar al
pez. El ritmo cardiaco debe ser de 0 bmp para proceder. Se realizó el corte utilizando
una aguja de punta gruesa, usando un estereoscopio. El corte se debe realizó en la
aleta caudal, comprometiendo una parte del musculo de esta misma (Imagen 1).
Posteriormente, se transfirieron las larvas con el corte a cajas de Petri con agua de
huevo y se ingresaron a la incubadora a 28.5 °C. Se debe registro su actividad durante
la siguiente hora para descartar posibles cortes mortales en los individuos
experimentales.
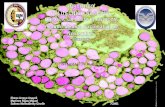
Imagen 1. Lugar de corte. Se debe comprometer el musculo para generar una mayor
movilización de neutrófilos. El corte de debe realizar sin afectar la vena y aorta caudal del
pez. Fondo de la imagen editado usando Adobe Illustrator CS6.

2.3 Evaluación de pico máximo de migración de neutrófilos
2.3.1 Evaluación de migración de neutrófilos
Para realizar la evaluación de la migración de neutrófilos se realizó un ensayo de
inflamación general basado en un corte de aleta caudal, tal como se describió
anteriormente. Se analizó el patrón de migración de los neutrófilos, usando una
tinción histológica con Sudan Black B mediante una pre fijación con
Paraformaldehido (PFA) al 4%. Se realizó la observación de las poblaciones de
neutrófilos desde las 0 hpi (hours post injury) hasta las 11 hpi. Todos los peces
tuvieron las mismas condiciones y fueron tomados progresivamente para observar
la migración de los neutrófilos.
2.3.2 Citoquímica
Este procedimiento histológico fue tomado de Hanly, 2001. Se realizaron los
ajustes necesarios para realizar los objetivos propuestos.
Se tomaron 0,1 g de Sudan Black B (Sigma Aldrich-S2380) y se disolvieron en 33,3
mL de etanol absoluto, mediante un agitador magnético en un baño de agua a 30°.
Se preparo adicionalmente una solución de fenol tamponado, que consiste en 8 g
de fenol y una solubilización en etanol absoluto. Esta solución fue añadida a un
recipiente que contiene 0.15 g de fosfato de ácido de sodio disueltos en 50 mL de
agua destilada, agitando hasta homogenizar. La solución de trabajo debe estar
constituida por 30 mL de solución inicial de Sudan Black B y 20 mL del tampón de
fenol. Para la preservación del colorante se almaceno en un frasco ámbar
protegido de la luz.
Para la tinción, se debe fijo con PFA 4% por una noche a 4°C. Luego, se lavó con
PBS 1X, cuatro veces durante 1 minuto. Posteriormente, se incubó con Sudan Black
B por 45 minutos a temperatura ambiente. Finalizada esta incubación las muestras
fueron lavadas exhaustivamente con etanol al 70% hasta la ausencia de colorante
en el sobrenadante. Para generar una mejor visualización de los neutrófilos se
aplicó una solución de glicerol 80% (1:1:8, agua, PBS 1x y glicerina), en la cual se
sumergieron las larvas y se esperó a su precipitación (1 hora aproximadamente).
Para la rehidratación se usa PBST (PBS 1X con Tween 20 al 1%), realizando tres
lavados de 10 minuto. La visualización de los neutrófilos se realizó con un
microscopio estereoscopio Leica (MDG33) en un aumento de 60X en campo claro.

2.4 Curva de toxicidad para Diclofenaco
Se evaluaron diferentes concentraciones de Diclofenaco sódico 75mg/3mL en
solución inyectable (Voltaren). Lo anterior, se realizó con el propósito de establecer
una concentración no letal y con propiedades anti inflamatorias.
Se realizó un ensayo con base en la concentración de 1.01 μM, la cual estaba
establecida como poco letal para larvas de peces cebra (Chen et al., 2014). Las
concentraciones evaluadas fueron 1, 0.40, 0.20, 0.08, 0.06, 0.04, 0.02, 0.01, 0.008
y 0.006 mM. El ensayo fue realizado a través de cuatro replicas con las diferentes
concentraciones al azar, mediante placas de cultivo celular de 24 pozos y durante
11 horas. Las larvas incluidas en la prueba eran revisadas cada hora. Se estableció
la concentración letal 50 (CL50).
2.5 Determinación de patrones de anti inflamación de los extractos vegetales
2.5.1 Evaluación de la actividad anti inflamatoria de los extractos vegetales
Luego de realizar el corte a los 5 dpf, se aplicaron los tratamientos. De cada uno de
los extractos vegetales Pentacalia ledifolia y Conyza trihecatatis, se prepararon
soluciones a partir de un stock de 200mg/L con 0.02 g del extracto etanólico diluido
en 1 mL de solución DMSO 1% y llevado hasta 100 mL usando agua de huevo. Se
evaluó las concentraciones de 30-35 mg/L, y 4-2 mg/L para P. ledifolia y C.
trihecatatis respectivamente, debido a la baja mortalidad que hay en estas
concentraciones (Garzon & Forero, 2016). Además, se evalúo el patrón de
migración de neutrófilos en DMSO 1%, agua de huevo y Diclofenaco 0,008 mM,
sometidos a corte y sin él.
En dos placas de cultivo celular de 12 pozos se tomaron 2 pozos por cada
tratamiento con un mínimo de 3 peces en cada pozo. La prueba se inició desde la
realización del corte en la aleta caudal, y durante un periodo de 8 horas. Se
visualizo la migración de neutrófilos usando los protocolos de citoquímica
mencionados anteriormente.
2.5.2 Determinación de patrones de migración de neutrófilos para porcentaje de
DMSO en cada extracto vegetal
Se determino si la baja concentración de DMSO (dimetilsulfóxido) usada (< 1%)
para disolver el extracto etanólico de las plantas posee un efecto anti inflamatorio
significativo. Para esto, se realizó una evaluación de la migración de neutrófilos
durante las 8 hpi (al realizarse una herida en la aleta caudal). De esta forma los
correspondientes porcentajes fueron (Conyza 4 mg/L = 0,02%; Conyza 2 mg/L =

0,01%; Pentacalia 35 mg/L = 0,175%; Pentacalia 30 mg/L = 0,150%; DMSO = 1 %).
Se visualizó la migración de neutrófilos usando los protocolos de citoquímica
mencionados anteriormente.
2.5.3 Determinación de patrones de migración de neutrófilos para porcentaje de
etanol en cada extracto vegetal
Se determino si usando un solvente diferente al DMSO se mantenía el patrón de
anti inflamación. Se usaron las concentraciones de Conyza 0.9, 2, 5 mg/L y
Pentacalia 20, 30, 40 mg/L. Así mismo, se determinó si la baja concentración de
etanol usada (< 1%) para disolver el extracto etanólico de las plantas posee un
efecto anti inflamatorio significativo. Para esto, se realizó una evaluación de la
migración de neutrófilos durante 8 hpi (al realizarse una herida en la aleta caudal).
De esta forma los correspondientes porcentajes fueron (Conyza 0,9 mg/L =
0,0045%; Conyza 2 mg/L = 0,01%; Conyza 5 mg/L = 0,025%; Pentacalia 20 mg/L =
0,1%; Pentacalia 30 mg/L = 0,2%; Pentacalia 40 mg/L = 0,150%; etanol = 1 %). Se
visualizó la migración de neutrófilos usando los protocolos de citoquímica
mencionados anteriormente.
3. Análisis de imagen y datos:
El análisis del conjunto de neutrófilos en migración en cada corte se realizó con Fiji
(Schindelin et al., 2012) de manera manual mediante el complemento Colony counter y con
Icy (De Chaumont et al., 2012), de manera automática usando spot counter (Parámetros =
Scale 4, sensitividad 40.0 y 13 pixeles) con el propósito de comparar métodos. Se contó la
cantidad de neutrófilos presentes en el corte, específicamente los presentes en un campo
de 2 cm desde el punto más extremo del corte caudal para ambos programas. Para los
procedimientos estadísticos se usó el programa R (Gentleman et al., 2009 R versión 3.4.4)
con una significancia de 0.05. Usando un ANCOVA para evaluar el efecto del programa
usado y la cantidad de neutrófilos que migró cada hora. Posteriormente, se usó un test de
Tukey para determinar que categorías eran las más significativas. Para la evaluación de los
patrones anti inflamatorios de los extractos de las plantas se realizó un ANOVA y un test de
Tukey para determinar que categorías eran las más significativas. Lo mismo se realizó para
ambos solventes.

4. Resultados
4.1 Evaluación de pico máximo de migración de neutrófilos
Imagen 2. Migración de neutrófilos registrada entre 3 a 11 hpi comparando dos métodos de
conteo.

Imagen 3. Patrón de migración de neutrófilos entre 0-11 hpi. Fondo de la imagen editada usando
Adobe Illustrator CS6.
Se realizo un ANOVA de dos lados para evaluar la cantidad de neutrófilos que son contados
en cada hora con respecto a cada programa usado (Icy e ImageJ) y posteriormente un
TukeyHSD test. Primero, se encontró una diferencia significa entre el número de neutrófilos
que se cuentan usando ImageJ o Icy, con un valor P de 0.011. Sin embargo, al realizar la
estimación de los patrones de confianza (95%), se encontró que en general ambos
programas se comportan de la misma manera, prediciendo un patrón similar. Se encontró
una única relación significativa siendo el valor p entre el inicio de la migración de los
neutrófilos 3 hpi-8 hpi para ImageJ y 7 hpi para Fiji (Imagen 2). De igual forma, en la imagen
3, se puede apreciar un aumento en el número de neutrófilos, que progresivamente
comienza a disminuir luego del pico máximo. Se decide realizar la siguiente fase de
experimentación durante las 8 hpi usando solamente los datos de Icy.

4.2 Curva de toxicidad Diclofenaco sódico
De acuerdo con registro realizado, se estableció que a 1.01 μM era una concentración
segura, sin embargo, no presentaba patrones de anti inflamación. Por esta razón se decido
hacer una curva de toxicidad entre 1 y 0.006 Mm.
Se estableció que la CL50 corresponde a 0.039 mM. Siendo necesario usar una
concentración menor a esta como control positivo. Se eligió usar 0.008 mM, ya que es
inferior al LC50, a partir de esta concentración se registró una mortalidad nula y es la
primera en registrar un patrón de anti inflamación.
Se realizo un ANOVA de para evaluar la cantidad de neutrófilos que son contados en cada
tratamiento usado Icy y posteriormente un TukeyHSD test. No se encontraron relaciones
significativas (Imagen 4 y 5). Sin embargo, se observa un patrón de migración menor para
los tratamientos de extractos etanolicos de ambas plantas, siendo mayor para P. ledifolia
(Imagen 5). También se encontró un proceso anti inflamatorio para el DMSO al 1%, siendo
el que se usa para el stock inicial (200mg/L).

4.3 Determinación de patrones de anti inflamación de los extractos vegetales
Imagen 4. Migración de neutrófilos en extractos etanolicos de Pentacalia ledifolia (a) y Conyza
trihecatactis (b).

Imagen 5. Patrón de migración de neutrófilos 8 hpi Conyza trihecatatis y Pentacalia ledifolia.
Fondo de la imagen editada usando Adobe Illustrator CS6.

4.4 Determinación de patrones de migración de neutrófilos para porcentaje de DMSO en
cada extracto vegetal
Imagen 6. Migración de neutrófilos para concentraciones de solvente (DMSO) en extractos de
Pentacalia ledifolia (a) y Conyza trihecatactis (b). Negro indica los controles sin corte, gris los
conjuntos de extracto de la plantas-DMSO y blanco los porcentajes de etanol contenidos en los
conjuntos extracto-etanol.
Se realizo un ANOVA de dos lados para evaluar la cantidad de neutrófilos que son contados
en cada porcentaje de DMSO (presente en cada concentración de extracto etanólico).
Posteriormente, se realizó un TukeyHSD test. No se encontró una diferencia significa entre
el número de neutrófilos del agua contra los extractos de las plantas-DMSO y DMSO por sí

solo. Se encontró que en general hay una menor migración de neutrófilos cuando participa
el conjunto extracto-DMSO para ambas plantas.
4.5 Determinación de patrones de migración de neutrófilos para porcentaje de etanol en
cada extracto vegetal
Imagen 6. Migración de neutrófilos para concentraciones de solvente (etanol) en extractos de
Pentacalia ledifolia (a) y Conyza trihecatactis (b). negro indica los controles, gris porcentajes de
etanol en los extractos de la plantas-etanol y blanco los conjuntos de planta-etanol.

Se realizo un ANOVA de dos lados para evaluar la cantidad de neutrófilos que son contados
en cada porcentaje de DMSO (presente en cada concentración de extracto etanólico).
Posteriormente, se realizó un TukeyHSD test. No se encontró una diferencia significa entre
el número de neutrófilos del agua contra los extractos de las plantas-etanol y etanol por sí
solo. Se encontró que en general hay una menor migración de neutrófilos cuando el etanol
actúa por sí solo, por lo que no es un buen solvente para nuestros propósitos.
5. Discusión
La inflamación corresponde a proceso complejo en el cual varias poblaciones celulares y
sus factores de comunicación están interviniendo. En esta evaluación experimental se
describe de manera sencilla los patrones de migración de una de estas poblaciones
celulares, los neutrófilos, primeras células en migrar durante la activación de los epitelios.
Con respecto a los patrones de migración de neutrófilos se estableció que su pico máximo
ocurre a las 7-8 hpi (Imagen 2). Este pico máximo ocurre debido a la migración masiva de
neutrófilos para prevenir y limitar la entrada de patógenos, donde posteriormente ocurre
un proceso de apoptosis (ilustrado en el declive en nuestro caso). La vida media de los
neutrófilos en humanos se ha determinado entre 7 a 10 horas (Cartwright, Athens &
Wintrobe, 1964; Price, Chatta & Dale, 1996). Esto indica que en el pez cebra se están
llevando a cabo procesos similares a los que ocurren en la inflamación para la migración de
neutrófilos, indicando este modelo animal como un candidato específico para estudiar
estos patrones. Aunque, otras características acerca de la naturaleza de los neutrófilos no
fueron evaluadas en este ensayo, se sugiere la similitud en los tiempos de migración al
tejido alterado como un factor positivo más para la comparación entre humano-pez cebra.
En este ensayo se evaluaron dos programas para el conteo de neutrófilos (Icy y Fiji). Se
encontró una sobreposición de los intervalos de confianza para ambos programas (Imagen
2), indicando que ambos muestran el mismo patrón. La razón principal para el uso de ambos
programas era disminuir el sesgo al momento de contar las células y estimar la mejor forma
de realizar el conteo. Se determino que ambos generan patrones similares de migración,
teniendo picos diferentes de máxima migración, 7 hpi para Icy y 8 hpi para ImageJ. Ambos
tienen el mismo patrón ascendente-pico máximo-descendiente. Los datos tomados con
ImageJ presentan mayor variabilidad, mientras que los de Icy tiene una sobreestimación sin
embargo su variabilidad en menor. La constante sobre estimación de la cantidad de
neutrófilos con Icy, puede deberse al conteo erróneo de pigmentos. Ya que, el programa no
puede diferenciar los pigmentos de los neutrófilos si se encuentran en la zona de conteo.
Para disminuir este sesgo se sugiere el uso de líneas de peces sin pigmento, ya que el uso
de PTU, aunque es una buena variante cuando no se poseen estas líneas, no limpia
completamente las larvas. De igual forma el uso de líneas transgénicas, ya que permitirían

usar este procedimiento sin sobrestimar los neutrófilos presentes. Sin embargo, ya que el
patrón de sobreestimación es constante en todos los tratamientos y presenta menor
variabilidad que ImageJ, se decido evaluar solo los datos obtenidos con Icy.
Debido a la naturaleza lipofílica del Sudan Black B, en este ensayo se estarían tiñendo las
poblaciones de eosinófilos, monocitos y neutrófilos del pez por igual. Sin embargo, ya que
las poblaciones que presentan migración en procesos de inflamación corresponden de
forma mayoritaria a monocitos y neutrófilos, los eosinófilos quedan descartados.
Finalmente, con esta técnica no es posible diferenciar las poblaciones de monocitos de las
de neutrófilos, sin embargo, por ser esta ultima la primera en migrar y la más prominente
entre los leucocitos (Lieschke et al., 2001), se puede afirmar que hay un proceso de
migración casi exclusivo por parte de los neutrófilos. No obstante, se reitera el uso de
animales transgénicos para marcadores únicos de neutrófilos con el fin de validar los datos.
Por otro lado, aunque se ha reportado una baja letalidad y desarrollo normal en diclofenaco
sódico correspondiente a 1.01 μM (Chen et al., 2014), en este ensayo se encontró que esa
concentración no produce un efecto anti inflamatorio significativo por lo que se evaluaron
diferentes concentraciones a partir de 1.01 mM. Se encontró que la concentración de 0.039
mM corresponde a la CL50. Además, se estableció que a una concentración de 0.008 mM la
mortalidad de las larvas es cero y es la primera en la que se produce efecto anti inflamatorio.
Sin embargo, ya que estas concentraciones fueron establecidas a partir de una formula
inyectable de venta libre y no de un reactivo de laboratorio tal como en Chen y
colaboradores en el 2014, los resultados no pueden ser comparables. No obstante, de
acuerdo con los datos de diclofenaco a 0.008 mM (Valor P < 0.05) se sugiere que este tiene
un efecto anti inflamatorio evidente y puede ser usado como control positivo (Imagen 5).
Para ambos extractos de plantas, Pentacalia ledifolia y Conyza trihecatatis, parece haber un
efecto anti inflamatorio evidenciado en la migración de neutrófilos. Siendo las más altas las
de P. ledifolia, seguidas por C. trihecatatis (Imagen 5). Aunque, no se conoce con certeza
los componentes metabólicos de estos extractos etanolicos, se puede atribuir sus
propiedades antiinflamatorias a moléculas de labdanos, en el caso de C. trihecatatis e
isoflavonas (Ramírez, 2011) para P. ledifolia. Ambos compuestos por presentar propiedades
anti inflamatorias (Bellik, Hammoudi, Abdellah, Iguer-Ouada, & Boukraâ, 2012). Sin
embargo, no se descarta la posibilidad que estos no correspondan a los responsables de la
anti-inflamación, o que sea un conjunto de compuestos químicos los que estén produciendo
el efecto, ya que, los compuestos aislados y conocidos para estas dos plantas aun
corresponden a un espectro muy reducido. Sin embargo, aunque las plantas parecen tener
un potencial anti inflamatorio, el solvente usado en este ensayo, DMSO, también está
presentando un efecto similar, aunque en general menor por si solo al ser evaluados los

porcentajes correspondiente de cada dilución de los extractos (Imagen 6), presentando la
posibilidad de un efecto sinérgico o adicional con el extracto etanolico. Sin embargo, no
podemos esclarecer en qué medida el solvente es el causante de la anti inflamación
observada.
Se ha reportado el DMSO como sustancia anti inflamatoria (Swanson, 1985; Elisia et al.,
2016) y ampliamente usada en veterinaria (Brayton, 1986; Smith et al., 1998; Arden et al.,
1990) para el tratamiento de caballos. Se encontró que todos los porcentajes de DMSO
producen una menor migración de neutrófilos. Sin embargo, se observó una menor
migración de neutrófilos al estar presentes los extractos etanolicos y el DMSO, que cuando
solo se evaluaba el porcentaje de DMSO correspondiente. Indicando un efecto aditivo o
sinérgico en el conjunto de extractos etanolicos y el DMSO. Sin embargo, no se puede
establecer en qué medida el efecto anti inflamatorio es producido por una u otra parte del
conjunto.
Al evaluar los extractos de las plantas usando etanol la migración de neutrófilos en general
es mayor que en el DMSO (Imagen 6). Además, el etanol al 1% tiene un efecto
antiinflamatorio mayor que el DMSO al mismo porcentaje. Así mismo, en los ensayos de
etanol-planta en general no es posible ver el efecto que tiene los compuestos de las plantas
por si solos, por lo cual aunque el DMSO parece ser una mejor alternativa, se sugiere este
ensayo como una revisión inicial, para focalizar posteriores observaciones con instrumentos
más precisos y análisis químicos sobre la composición de los compuestos, que confirmen
las propiedades anti inflamatorias vistas en primera medida usando esta técnica en el pez
cebra.
6. Conclusión
Gracias a este ensayo se concluye que el pez cebra es una herramienta útil para la
evaluación de patrones de migración de neutrófilos. De igual forma, que el programa Icy
representa una herramienta útil para el conteo de esta población celular. Además, los
extractos de P. ledifolia y C. trihecatatis parecen generar un patrón anti inflamatorio,
reduciendo la migración de neutrófilos, aunque, parte de este proceso puede estar mediado
por el solvente, como ocurre para los dos que fueron evaluados en este ensayo. Sugerimos
este estudio como un acercamiento inicial a la determinación del potencial anti inflamatorio
de una sustancia, recomendando el uso de compuestos que no requieran la disolución en
solventes. Todo con el propósito de la posterior determinación de la composición de la
sustancia mediante un análisis químico. Así mismo, se sugiere el uso de animales
transgénicos para comparar los resultados obtenidos con secuencias visuales completas en
el mismo individuo. Por otro lado, aunque no era nuestro propósito inicial se establecieron
las propiedades anti inflamatorias del etanol y el DMSO en varias concentraciones inferiores

al 1%. Esto es muy importante, ya que indica la necesidad de evaluar todos los porcentajes
usados de estos solventes, aunque sean muy pequeños. Lo anterior, se resalta ya que en
algunos artículos se tiende a obviar estos por su pequeño valor.
7. Referencias
Arden, W. A., Slocombe, R. F., Stick, J. A., & Parks, A. H. (1990). Morphologic and ultrastructural
evaluation of effect of ischemia and dimethyl sulfoxide on equine jejunum. American journal
of veterinary research, 51(11), 1784-1791.
Bain, B. J. (2010). Neutrophil dysplasia demonstrated on Sudan black B staining. American journal
of hematology, 85(9), 707-707.
Barnes, P. J. (2006). How corticosteroids control inflammation: Quintiles Prize Lecture 2005. British Journal of Pharmacology, 148, 245–254. https://doi.org/10.1038/sj.bjp.0706736
Brayton, C. F. (1986). Dimethyl sulfoxide (DMSO): a review. The Cornell Veterinarian, 76(1), 61-90.
Bellik, Y., Hammoudi, S. M., Abdellah, F., Iguer-Ouada, M., & Boukraâ, L. (2012). Phytochemicals to prevent inflammation and allergy. Recent Patents on Inflammation & Allergy Drug Discovery, 6(2), 147–58. https://doi.org/IAD-EPUB-20120220-001 [pii]
Cartwright, G. E., Athens, J. W., & Wintrobe, M. M. (1964). Analytical review: The kinetics of granulopoiesis in normal man. Blood, 24(6), 780-803.
Chen, J. B., Gao, H. W., Zhang, Y. L., Zhang, Y., Zhou, X. F., Li, C. Q., & Gao, H. P. (2014). Developmental toxicity of diclofenac and elucidation of gene regulation in zebrafish (Danio rerio). Scientific reports, 4, 4841.
Correa, R. G., Tergaonkar, V., Ng, J. K., Izpisua-belmonte, J. C., Verma, I. M., & Dubova, I. (2004). Characterization of NF- κ ?/ I κ ? Proteins in Zebra Fish and Their Involvement in Notochord Development Characterization of NF- ⟩ / I ⟩ Proteins in Zebra Fish and Their Involvement in Notochord Development. Mol. Cell. Biol, 24(12), 5257–5268. https://doi.org/10.1128/MCB.24.12.5257
Crawford, A. D., Esguerra, C. V., & De Witte, P. A. M. (2008). Fishing for drugs from nature: Zebrafish as a technology platform for natural product discovery. Planta Medica, 74(6), 624–632. https://doi.org/10.1055/s-2008-1034374
Crawford, A. D., Liekens, S., Kamuhabwa, A. R., Maes, J., Munck, S., Busson, R., … de Witte, P. A. M. (2011). Zebrafish bioassay-guided natural product discovery: Isolation of angiogenesis inhibitors from East African medicinal plants. PLoS ONE, 6(2), 1–9. https://doi.org/10.1371/journal.pone.0014694
De Chaumont, F., Dallongeville, S., Chenouard, N., Hervé, N., Pop, S., Provoost, T., ... & Lagache, T. (2012). Icy: an open bioimage informatics platform for extended reproducible research. Nature methods, 9(7), 690.
De Rosa, S., & Tommonaro, G. (2012). Bioactive marine prenylated quinones/quinols. Studies in

Natural Products Chemistry (Vol. 36). https://doi.org/10.1016/B978-0-444-53836-9.00023-2
Elisia, I., Nakamura, H., Lam, V., Hofs, E., Cederberg, R., Cait, J., ... & Guns, E. S. (2016). DMSO represses inflammatory cytokine production from human blood cells and reduces autoimmune arthritis. PLoS One, 11(3), e0152538.
Fazio, C., & Ricciardiello, L. (2016). Inflammation and Notch signaling: a crosstalk with opposite effects on tumorigenesis. Cell Death and Disease, 7(12), e2515. https://doi.org/10.1038/cddis.2016.408
Garibello. C. (2010). ESTUDIO DE HOJAS DE Pentacalia vaccinioides (Kunth) COMO NUEVA FUENTE
NATURAL DE SUSTANCIAS ESTEROIDALES Y CUMARINAS, Pontificia Universidad Javeriana.
Garzon, L., & Forero, T. (2016). EFECTOS BIOLÓGICOS DE EXTRACTOS ETANÓLICOS DE Conyza trihecatactis y Pentacalia ledifolia USANDO COMO MODELO EL PEZ CEBRA.
Gentleman, R., Ihaka, R., Bates, D., Chambers, J., Dalgaard, J., & Hornik, K. (2009). The R project for statistical computing. URL: http://www. r-project. org/254.
Gray, C., Loynes, C. A., Whyte, M. K. B., Crossman, D. C., Renshaw, S. A., & Chico, T. J. A. (2011). Simultaneous intravital imaging of macrophage and neutrophil behaviour during inflammation using a novel transgenic zebrafish. Thrombosis and Haemostasis, 105(5), 811–819. https://doi.org/10.1160/TH10-08-0525
Guzmán-Tirado M. A. (1997). Aproximación a la Etnobotánica de la provincia de Jaén, Universidad
de Granada.
Hanly, M. G. (2001). Methods in Leukocyte Cytochemistry. In Hematologic Malignancies (pp. 277-
300). Humana Press.
Harris, C. B., Chowanadisai, W., Mishchuk, D. O., Satre, M. A., Slupsky, C. M., & Rucker, R. B. (2013). Dietary pyrroloquinoline quinone (PQQ) alters indicators of inflammation and mitochondrial-related metabolism in human subjects. Journal of Nutritional Biochemistry, 24(12), 2076–2084. https://doi.org/10.1016/j.jnutbio.2013.07.008
Henry, K. M., Loynes, C. a, Whyte, M. K. B., & Renshaw, S. a. (2013). Zebrafish as a model for the study of neutrophil biology. Journal of Leukocyte Biology, 94(4), 633–42. https://doi.org/10.1189/jlb.1112594
Hernández-Arias J. M. (2014). DITERPENOS DE Ageratina vacciniaefolia, Conyza trihecatactis, Gnaphalium graveolens Y EVALUACIÓN DEL EFECTO ANTIINFLAMATORIO Y CITOTÓXICO, 69.
Kim, T. H., Li, H., Wu, Q., Lee, H. J., & Ryu, J. H. (2013). A new labdane diterpenoid with anti-inflammatory activity from Thuja orientalis. Journal of Ethnopharmacology, 146(3), 760–767. https://doi.org/10.1016/j.jep.2013.02.001
Lansink, A.G.W. Histochemie (1968) 16: 68. https://doi.org/10.1007/BF00306212
Lieschke, G. J., Oates, A. C., Crowhurst, M. O., Ward, A. C., & Layton, J. E. (2001). Morphologic and functional characterization of granulocytes and macrophages in embryonic and adult

zebrafish. Blood, 98(10), 3087-3096.
Loutfy,B. (2009). Medicinal Plants of North Africa, 3 edición. Indiana: Universidad de Indiana.
Ma, B., & Hottiger, M. O. (2016). Crosstalk between wnt/??-catenin and NF-??B signaling pathway during inflammation. Frontiers in Immunology, 7(SEP). https://doi.org/10.3389/fimmu.2016.00378
Martin, P., & Feng, Y. (2009). Inflammation: Wound healing in zebrafish. Nature, 459(7249), 921–923. https://doi.org/10.1038/459921a
Mosser, D. M., & Edwards, J. P. (2009). NIH Public Access. Genetics, 8(12), 958–969. https://doi.org/10.1038/nri2448.Exploring
National Research Council (U.S.) Committee for the Update of the Guide for the Care and Use of Laboratory Animals, Institute for Laboratory Animal Research (U.S.), & National Research Council (US) Committee for the Update of the Guide for the Care and Use of Laboratory Animals. (2011). Guide for the Care and Use of Laboratory Animals. https://doi.org/10.17226/12910
Price, T. H., Chatta, G. S., & Dale, D. C. (1996). Effect of recombinant granulocyte colony-stimulating factor on neutrophil kinetics in normal young and elderly humans. Blood, 88(1), 335-340.
Petrie, T. a, Strand, N. S., Tsung-Yang, C., Rabinowitz, J. S., & Moon, R. T. (2014). Macrophages modulate adult zebrafish tail fin regeneration. Development (Cambridge, England), 141(13), 2581–91. https://doi.org/10.1242/dev.098459
Ramírez, E. J. (2011). Variabilidad química de extractos y fracciones obtenidas de tres especies dela tribu Senecioneae:Gynoxys hirsuta, Pentacalia ledifolia, Senecio pampae, 18.
Rueden, C. T.; Schindelin, J. & Hiner, M. C. et al. (2017), "ImageJ2: ImageJ for the next generation of scientific image data", BMC Bioinformatics 18:529, doi:10.1186/s12859-017-1934-z.
Santana Alba, I. F. (2010). Estudio químico de la especie colombiana Pentacalia abietina (Willd. ex.
Wedd) Cuatr. Como nueva fuente natural de compuestos tipo kaurano y quinol (Master's thesis, Facultad de Ciencias).
Smith, G., Bertone, A. L., Kaeding, C., Simmons, E. J., & Apostoles, S. (1998). Anti-inflammatory
effects of topically applied dimethyl sulfoxide gel on endotoxin-induced synovitis in horses. American journal of veterinary research, 59(9), 1149-1152.
Swanson, B. N. (1985). Medical use of dimethyl sulfoxide (DMSO). Reviews in clinical & basic
pharmacology, 5(1-2), 1-33. Schindelin, J.; Arganda-Carreras, I. & Frise, E. et al. (2012), "Fiji: an open-source platform for
biological-image analysis", Nature methods 9(7): 676-682, PMID 22743772, doi:10.1038/nmeth.2019.

Tran, Q. T. N., Wong, W. S. F., & Chai, C. L. L. (2017). Labdane diterpenoids as potential anti-inflammatory agents. Pharmacological Research, 124, 43–63. https://doi.org/10.1016/j.phrs.2017.07.019
Yu, J., Bi, X., Yu, B., & Chen, D. (2016). Isoflavones: Anti-inflammatory benefit and possible caveats. Nutrients. https://doi.org/10.3390/nu8060361