S0 S1 S2 h A k NR IC h F fluorescencia T1 cruce intersistemas ISC k NR ISC h P fosforescencia...
-
Upload
alano-narvaez -
Category
Documents
-
view
82 -
download
6
Transcript of S0 S1 S2 h A k NR IC h F fluorescencia T1 cruce intersistemas ISC k NR ISC h P fosforescencia...

S0
S1
S2
hA
kNR IC
hF
fluorescencia
T1cruce intersistemas ISC
kNR ISC hP
fosforescencia
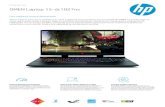
DIAGRAMA DE JABLONSKI (1898-1980)
conversión interna IC
relajación vibracional
relajación vibracional

LUMINISCENCIA emisión de luz desde un estado electrónicamente excitado
Se alcanza el estado excitado por absorción de luz en:
FLUORESCENCIA estado singulete excitado, transición permitida, ns
FOSFORESCENCIA estado triplete excitado, transición prohibida, ms
Se alcanza el estado excitado por una reacción química:
QUIMIOLUMINISCENCIA

10-15 s
10-8 s
10-3 s

OBSERVAR: la escala de tiempo de los procesos:
• ABSORCION: ~ 10-15 seg
• CONVERSION INTERNA: ~ 10-11-10-9 seg
• FLUORESCENCIA: ~ 10-10 a 10-7 seg
• FOSFORESCENCIA: ~ 10-6 a 1 seg (es una transición “prohibida” )
• RELAJACION VIBRACIONAL: ~ 10-12-10-10 seg
Los pasos propiamente dichos de absorción y de emisión son extremadamente rápidos, tanto que los núcleos no llegan a moverse (principio de Franck-Condon). La absorción sólo da información del entorno inmediato a la molécula que absorbe.
La relajación vibracional por lo general es mucho más rápida que la fluorescencia, entonces la molécula se relaja completamente y (en general) sólo vemos la emisión desde el estado S1.
La escala de tiempo de fluorescencia es la misma que la escala de tiempo de movimientos moleculares, por eso el espectro de fluorescencia posee información de un entorno más amplio que el de absorción.

FLUORESCENCIA
• 1er. paso: absorción o excitaciónenergía suficiente para llegar a nivel
electrónico superior S1 o S2
λexc
• 2do. paso: emisión de luzenergía radiativa emitida menor que la
absorbida, λem > λexc
Corrimiento de Stokes
ESTADO EXCITADO


Rendimiento (Q) = fotones emitidos <1 fotones absorbidos
= constante de velocidad de emisión
= constante de velocidad de decaimiento no radiativo
RENDIMIENTO CUANTICO DE FLUORESCENCIA (Q):
en términos cinéticos de cada proceso:


= tiempo de vida intrínseca o natural,
sin ningún proceso no radiativo
= tiempo de vida medida
TIEMPO DE VIDA: tiempo promedio que un fluoróforo pasa en el estado excitado antes de volver al estado basal (por cualquier vía)
TIEMPO DE VIDA NATURAL: es el tiempo de vida si sólo volviera al estado basal por fluorescencia
Se relacionan:

Parámetros a medir en fluorescencia
• Intensidad de fluorescencia (ISS)
• Espectros de excitación y emisión (IF vs λ)
• λmax(ex), λmax(em)
• Rendimiento cuántico de fluorescencia (Q)
• Vida media del fluoróforo ()
• Anisotropía (r) (tiempo de correlación rotacional)
• Eficiencia RET (E) (distancia de Föster)

Intensidad de fluorescencia (estado estacionario) ISS
Intensidad resuelta en el tiempo ()
Pulso de luzIluminación continua

ESPECTROFLUORÍMETRO

ESPECTROFLUORÍMETRO
FUENTE DE LUZ Xe, Hg-Xe, Hg (high- low-P), Diodo (lase, LED)
MONOCROMADORES excitación y emisión vs FILTROS
ancho de banda
polarizadores
DETECTOR tubo fotomultiplicador (PMT)
MUESTRA geometría de iluminación de la muestra
La medida de IF es relativa a la geometría del equipo

Intensidad de Fluorescencia y concentración del fluoróforo
Efecto de filtro interno

Cuantificación del fluoróforo midiendo Intensidad de fluorescencia IF
IF (λex, λem) = IA Φ Z Z = factor instrumental
Φ= rendimiento cuántico de F
IA = IT - I0 = I0 (1 – exp(-2.3 ε c l)
ε = coef. Absortividad a λexc
c = concentración del fluoróforo
IF (λex, λem) = I0 Φ Z 2.3 ε c l
IF es proporcional a la conc. Si trabajamos con conc. diluidas
Si Aλ << 1 IA = I0 (2.3 ε c l)

Usar soluciones diluidas A < 0..05
Control con solo solvente
Usar adecuada λexc, filtro, conc. fluoróforo
Filtrar la solución


Fluoróforos en bioquímica
• Fluorescencia intrínseca fluorescencia natural, propia del sistema
• Fluorescencia extrínseca agrego a la muestra un fluoróforo externo (sonda fluorescente)

Fluorescencia en:
• Proteínas, fluorescencia intrínseca debido a residuos aminoacídicos aromáticos, predomina el triptofano.
Además marcado con sondas fluorescentes (FITC, DNS). GFP y derivados.
• Ácidos nucleicos, sin fluorescencia intrínseca, se agregan sondas fluorescentes catiónicas planares (EtBr, DAPI)
•Membranas, no fluorescentes, se agregan sondas liposolubles con baja fluorescencia en agua (DPH, ANS) o fosfolípidos marcados

Fluorescencia en:
• NAD(P)H
• FAD, FMN
• Piridoxal fosfato (PLP)
• Clorofilas
• Indicadores fluorescentes (pH, Na+, Cl-, Ca2+, O2)

0.4 ns en solución1-5 ns unido a DH
4.7 ns en solución(2.3 ns FMN)0.3-1 ns unido a prot.


Phe Abundancia: 3.5%
ex = 260 nm, em= 282 nm (Q. ~ 5)
Insensible al entorno
Tyr Abundancia: 3.5%
ex = 275 nm, em= 303 nm (Q. ~ 220)
Insensible al entorno, quencheable
Ionizable, tirosinato emite (<Q)
Trp Abundancia: 1.1%
ex = 295 nm, em= 350 nm (Q. ~ 770)
Sensible al entorno, quencheable
Varias

Sondas fluorescentes para proteínas
DNS-Cl sensible a polaridad del entorno, fluorescencia polarizada
Fluoresceína (y Rodaminas) absorbe y emite en el visible, alto rendimiento,
ε=80.000 M-1cm-1

Compuestos de B (BODIPY) absorben y emiten en el visible, alto
rendimiento, ε=80.000 M-1cm-1, fotoestables, insensible al solvente y pH

Sondas fluorescentes para ácidos nucleicos
Bases modificadas fluorescentes

GFP = Green Fluorrescent Protein
Formación espontánea del fluoróforo al plegarse

X
X*
hν
hν’
Relajación por solvente
Transferencia de energía
Quenching
Transferencia de carga
Disociación de H+
Formación de complejos
Formación de oligómeros
(ns)
¿Qué le puede suceder al estado excitado del fluoróforo antes de emitir y volver al estado basal?

10-10 s

Efectos del solvente y del entorno local sobre la fluorescencia
H = hexano
CH = ciclohexano
T = tolueno
EA = acetato de etilo
Bu = butanol
HO
Acido dimetilamino naftalen sulfónico (dansilo)

Efectos del solvente y del entorno
k >> 1/ k 1/
Corrimientos de Stokes dinámicos

Cambio en la emisión por cambio de solvente o cambio del entorno (ej. unión a proteína)
Miro la fluorescencia de la sonda fluorescente, el TNS

Cambio en la emisión por cambio de solvente o cambio del entorno (ej. unión a proteína)
HSA = albúmina humana
ANS = Anilinonaftalensulfonato (fluoróforo muy sensible a la polaridad entorno)

Determinar constantes de unión de un ligando si este es fluorescente y su fluorescencia cambia con la unión o si la fluorescencia intrínseca cambia por efecto de la unión de un ligando

Emisión del triptofano es sensible al entorno (ej. desnaturalización de proteína)
N = nativa
U = desplegada “unfolded”

Usos de fluorescencia en bioquímica
• Localización subcelular• Cambios en la concentración • Interacciones moleculares• Cambios conformacionales• Distancias intra/intermoleculares• Difusión rotacional • Caracterización estructural• Actividad enzimática
●●●