República Bolivariana de Venezuela Ministerio para la ... · diagrama de flujo y de bloque . ......
Transcript of República Bolivariana de Venezuela Ministerio para la ... · diagrama de flujo y de bloque . ......
República Bolivariana de Venezuela Ministerio para la Educacion Superior Universitaria
Universidad Jose Antonio Paez
Alumno
24686096 Yuscarly Hernández
22610451 Axel Lugo
17249123 Arturo Mora
San Diego 2016
Introducción
El presente trabajo tiene como finalidad estudiar ,informar y
mencionar los principales procesos industriales que al gas natural
conierne,explicando así su obtención ,materia prima y derivados al
final del proceso de obtención, utilizando herramientas como el
diagrama de flujo y de bloque
El gas natural constituye una importante fuente de
energía fósil liberada por su combustión. Es una mezcla de
hidrocarburos gaseosos ligeros que se extrae, bien sea de
yacimientos independientes (gas libre), o junto a yacimientos
petrolíferos o de carbón (gas asociado a otros hidrocarburos gases
y líquidos peligrosos).
Objetivos del gas natural
* Convencer a la población sobre el uso del gas natural en
nuestras viviendas.
*Informar a la población todo a cerca de este combustible
beneficioso.
* Dar a conocer a las personas sobre los beneficios del gas natural
como combustible energético en el caso del uso doméstico.
* Informar a la población que sería mucho mejor el uso del gas
natural a comparación del petróleo o gasolina, ya que es más
económico, más seguro, más práctico y menos contaminante.
* Hacer que la gente se interese más en este tema del gas natural
en las viviendas, realizando encuestas, ya que la gente no está
informada de todos los maravillosos beneficios que nos puede
ofrecer este gas.
Origen
Los primeros descubrimientos de yacimientos de gas natural
fueron hechos en Irán entre los años 6000 y 2000 A.C. Estos
yacimientos de gas, probablemente encendidos por primera vez
mediante algún relámpago, sirvieron para alimentar los "fuegos
eternos" de los adoradores del fuego de la antigua Persia.
También se menciona el uso del gas natural en China hacia el 900
A.C. Precisamente en China se reporta la perforación del primer
pozo conocido de gas natural de 150 metros de profundidad en el
211 A.C. Los chinos perforaban sus pozos con varas de bambú y
primitivas brocas de percusión, con el propósito expreso de
buscar gas en yacimientos de caliza. Quemaban el gas para secar
las rocas de sal que encontraban entre las capas de caliza.
El gas natural era desconocido en Europa hasta su descubrimiento
en Inglaterra en 1659, e incluso entonces, no se masificó su
utilización. La primera utilización de gas natural en Norteamérica
se realizó desde un pozo poco profundo en la localidad de
Fredonia, estado de Nueva York, en 1821. El gas era distribuido a
los consumidores a través de una cañería de plomo de diámetro
pequeño, para cocinar e iluminarse.
A lo largo del siglo 19, el uso del gas natural permaneció
localizado porque no había forma de transportar grandes
cantidades de gas a través de largas distancias, razón por la que
el gas natural se mantuvo desplazado del desarrollo industrial por
el carbón y el petróleo.
A principios de la séptima década del siglo veinte tuvo su origen
en Rusia la cañería de gas más larga. La red de Northern Lights,
de 5470 kilómetros de longitud, cruza los Montes Urales y unos
700 ríos y arroyos, uniendo Europa Oriental con los campos de gas
de Siberia del Oeste en el círculo Ártico. Otra red de gas, más
corta, pero de gran dificultad de ingeniería, es la que se extiende
desde Argelia, a través del Mar Mediterráneo hasta Sicilia. El mar
tiene más de 600 metros de profundidad en algunos tramos de la
ruta.
El transporte de gas por largas distancias se hizo practicable a
fines de la segunda década del siglo 20 por un mayor avance de la
tecnología de cañerías. En Estados Unidos entre 1927 y 1931 se
construyeron más de 10 grandes sistemas de transmisión de gas.
Cada uno de estos sistemas se construyó con cañerías de unos 51
centímetros de diámetro y en distancias de más de 320
kilómetros. Después de la Segunda Guerra Mundial se
construyeron más sistemas de mayores longitudes y diámetros. Se
hizo posible la construcción de cañerías de 142 centímetros de
diámetro.
Características
Se denomina gas natural a una mezcla de gases, cuyos
componentes principales son hidrocarburos gaseosos.
Básicamente es un combustible de origen fósil que procede de la
descomposición de materia orgánica.
No existe una teoría rigurosa sobre su formación pero se puede
asegurar que proviene de un proceso análogo al de la formación
del petróleo.
El gas natural se encuentra en la naturaleza en las llamadas
“bolsas de gas “, bajo tierra, cubiertas por capas impermeables
que impiden su salida al exterior.
El gas natural se puede encontrar acompañando al crudo en pozos
petrolíferos (gas natural asociado) o bien en yacimientos
exclusivos de gas natural (gas natural no asociado).
Está constituido principalmente por metano en proporciones que
generalmente oscilan entre el 80% y el 90% del volumen, y aún
más; el resto son hidrocarburos de orden superior, parafínicos en
su casi totalidad con algunos isoparafínicos. Contiene también
vapor de agua en proporciones variables de saturación y aún agua
condensada y puede contener anhídrido carbónico, nitrógeno,
hidrógeno sulfurado, helio, etc.
El gas natural no contiene olefínicos, hidrocarburos éstos que se
originan en procesos de destilación destructiva o reforming.
El poder calórico del gas natural es variable de acuerdo a su
composición, estando comprendido generalmente entre 9.000 y
9.500 cal/m3, a menos que se trate de un gas con importante
contenido de inertes o por el contrario de hidrocarburos pesados,
siendo así de menor o mayor poder calórico respectivamente.
La densidad, medida respecto de la del aire tomada como unidad,
oscila comúnmente entre 0,6 y 0,7 según sea el contenido de
hidrocarburos condensables (propano y superiores), pudiendo aún
ser mayor si fuese muy rico en estos últimos.
No tiene color ni olor, aunque para su detección, se incorpora un
componente químico (mercaptano) que le proporciona un olor
característico.
Según sea el contenido de gasolina se lo denomina gas rico o gas
seco. Como zona límite entre ambos categorías puede
establecerse una banda comprendida entre 10 y 20 litros de
gasolina por cada 1.000 m3 de gas.
Clasificación
Gas licuado: El propano C3H8 y el butano C4H10 si bien en
condiciones normales de temperatura y presión están en estado
gaseoso, al comprimirse se licuan, lo que se logra a presiones
moderadas, permitiendo su almacenamiento en tanques o
cilindros, para su utilización en estado gaseoso a presión
ligeramente superior a la atmosférica. Ello constituye lo que se
conoce como gas envasado cuyas características se verán
posteriormente.
Bio-Gas: El bio-gas proviene de la descomposición de la materia
orgánica por medio de las bacterias, estando compuesto
básicamente por metano (50 a 70 %) y dióxido de carbono (30 a 45
%), con pequeñas proporciones de oxígeno, hidrógeno y nitrógeno.
El bio-gas es producido por la putrefacción de residuos fósiles,
vegetales y materia orgánica en ausencia de oxígeno, por parte de
las bacterias anaeróbicas.
Fundamentos Legales
2051-93: Gas natural. Determinación del contenido de sulfuro de
hidrógeno y mercaptano por absorción en sulfato de cadmio.
Método de valorización yodométrica.
Es la aplicación de intervalos de concentración entre 0g y 5g de
sulfuro de hidrogeno y de 0g ya 1g de azufre mercaptano por litro
de gas natural
El gas natural y sus productos de combustión no deben ser
excesivamente corrosivos para materiales con los que entra en
contacto por ello ; es muy importante que el contenido de sulfuro
de hidrogeno y otros compuestos de azufre se bajo
Aplicaciones del Gas Natural
Industrial Generación de vapor
Industria de alimentos
Secado
Cocción de productos cerámicos
Fundición de metales
Tratamientos térmicos
Temple y recocido de metales
Generación eléctrica
Producción de petroquímicos
Sistema de calefacción
Hornos de fusión
Comercio y Servicios Calefacción central
Aire acondicionado
Cocción/preparación de alimentos
Agua caliente
Energía
Cogeneración eléctrica
Centrales térmicas
Residencial Cocina
Calefacción
Agua caliente
Aire acondicionado
Transporte de pasajeros
Taxis
Buses
Adicionalmente, el gas natural es utilizado como materia prima en
diversos procesos químicos e industriales. De manera
relativamente fácil y económica puede ser convertido a hidrógeno,
etileno, o metanol; los materiales básicos para diversos tipos de
plásticos y fertilizantes.
Combustibles que el Gas Natural puede sustituir
Industrial Carbón
Electricidad
DHM
Diesel
Fuel Oil
Gas licuado
Gasolina
Kerosene
Leña
Generación eléctrica Carbón
Fuel Oil
Comercio Carbón
Electricidad
Fuel Oil
Gas de ciudad
Gas licuado
Kerosene
Residencial Electricidad
Gas de ciudad
Gas licuado
Kerosene
Leña
Propiedades Fisicas y Quimicas
Los siguientes, son los componentes principales del gas natural,
estos varían según el yacimiento:
Componente % Componente %
Metano 95,0812 i-pentano 0,0152
Etano 2,1384 Benceno 0,0050
Propano 0,2886 Ciclohexano 0,0050
n-butano 0,0842 Nitrógeno 1,9396
i-butano 0,0326 CO2 0,3854
Las propiedades del gas natural según la composición indicada en
el cuadro 1, son las siguientes:
Densidad: 0,753 kg/m³ Poder calorífico: 9,032 kcal/m³
Cp (presión
constante):
8,57
cal/mol.°C
Cv (volumen
constante):
6,56
cal/mol.°C
1. Metano: Llamado gas de los pantanos, hidrocarburo
de fórmula CH4, el primer miembro de la serie de los
alcanos. Es más ligero que el aire, incoloro, inodoro e
inflamable. Se encuentra en el gas natural, como en el
gas grisú de las minas de carbón, en los procesos de
las refinerías de petróleo, y como producto de la
descomposición de la materia en los pantanos. Es uno
de los principales componentes de la atmósfera de los
planetas Saturno, Urano y Neptuno.
Fórmula
desarrollada
2. Etano: Gas incoloro e inflamable, hidrocarburo de
fórmula C2H
6, el segundo miembro de la serie de los
alcanos.
Fórmula
desarrollada
3. Eteno o Etileno: El eteno es un hidrocarburo de
fórmula C2H
4, el miembro más simple de la clase de
compuestos orgánicos llamados alquenos. Es un gas
incoloro, con un olor ligeramente dulce, arde con una
llama brillante, es ligeramente soluble en agua.
Fórmula
desarrollada
4. Propano: El tercer hidrocarburo de la serie de los
alcanos, de fórmula C3H
8. Gas incoloro e inodoro. Se
encuentra en el petróleo en crudo, en el gas natural y
como producto derivado del refinado del petróleo. El
propano no reacciona vigorosamente a temperatura
ambiente, pero,a temperaturas más altas, arde en
contacto con el aire.
Fórmula
desarrollada
5. Butano: Cualquiera de los dos hidrocarburos saturados o alcanos, de
fórmula química C4H
10, en ambos compuestos, los átomos de carbono
se encuentran unidos formando una cadena abierta. En el n-butano
(normal), la cadena es continua y sin ramificaciones, mientras que en
el i-butano (iso), o metilpropano, uno de los átomos de carbono forma
una ramificación lateral. Esta diferencia de estructura es la causa de
las distintas propiedades que presentan. El n-butano y el i-butano
están presentes en el gas natural, en el petróleo y en los gases de las
refinerías. Poseen una baja reactividad química a temperatura normal,
pero arden con facilidad al quemarse en el aire o con oxígeno.
Fórmula desarrollada:
n-butano i-butano
6. Pentano: Quinto miembro de los alcanos alcanos, de
fórmula química C5H
12, se presenta con dos
configuraciones el n-pentano y el i-pentano.
Fórmula
desarrollada
7. Benceno: Líquido incoloro de olor característico y
sabor a quemado, de fórmula C6H
6, en estado puro arde
con una llama humeante debido a su alto contenido de
carbono. Sus vapores son explosivos, y el líquido es
violentamente inflamable.
Fórmula
desarrollada
8. Ciclohexano: Líquido volátil e incoloro con olor
penetrante, de fórmula C6H
12, que acompaña al gas
natural.
Fórmula
desarrollada
Propiedades principales de los componentes del gas natural (15 °C
y 1 atmósfera)
Combustible
P.F.
°C
P.E.
°C
P.M.
kg
Densidad
kg/m³
Poder
Calorífico
kcal/m³
Calor de
Combustión
kcal/kg
Metano
-
182,5
-
161,5
0,016 0,7175 9024 13187
Etano -183 -87 0,030 1,3551 15916 12267
Etileno
-
169,4
-
103,8
0,028 1,26 - -
Propano
-
189,9
-42,1 0,044 2,0098 22846 11955
n-butano
-
138,3
-0,5 0,058 2,7068 30144 11862
i-butano -145 -10,2 0,058 2,7091 29955 -
n-pentano -130 36 0,072 3,5066 38149 -
i-pentano - - 0,072 3,4354 37630 -
Benceno 5,5 80,1 0,078 890 - 10026
Ciclohexano 6,55 80,74 0,084 - - 11167
Combustión
Es el proceso de oxidación rápida de un combustible acompañado
de un aumento de calor y frecuentemente de luz. En el caso de los
combustibles comunes, el proceso consiste en una combinación
química con el oxígeno de la atmósfera que lleva a la formación
de dióxido de carbono, monóxido de carbono y agua, junto con
otros productos como dióxido de azufre, que proceden de los
componentes menores del combustible.
A los combustibles gaseosos como el gas natural,el gas refinado o
los gases manufacturados, se les añade aire antes de la
combustión para proporcionarles una cantidad suficiente de
oxígeno. La mezcla de aire y combustible surge del quemador a
una velocidad mayor que la de la propagación de la llama,
evitando así el retroceso de ésta al quemador, pero permitiendo el
mantenimiento de la llama en éste. Estos combustibles, en
ausencia de aire, arden con llamas relativamente frías y
humeantes. Cuando el gas natural arde en el aire alcanza
temperaturas que superan los 1.930 °C.
Las reacciones de combustión de los gases que nos interesan son
las siguientes:
Metano:
CH4 + 2O
2 → CO
2 +
2H2O
Etano:
2C2H
6 + 7O
2 → 4CO
2 +
6H2O
Eteno:
C2H
4 + 3O
2 → 2CO
2 +
2H2O
Propano:
C3H
8 + 10O
2 → 3CO
2 +
4H2O
Butano:
2C4H
10 + 13O
2 →
8CO2 + 10H
2O
Pentano:
C5H
12 + 8O
2 → 5CO
2 +
6H2O
Benceno:
2C6H
6 + 15O
2 →
12CO2 + 6H
2O
Ciclohexano:
C6H
12 + 9O
2 → 6CO
2 +
6H2O
Limites de inflamabilidad
El gas natural es susceptible de reaccionar con aire u oxigeno
produciendo llama y gran cantidad de calor, el gas como
combustible y el aire como comburente. La inflamación del gas
depende de los limites de inflamabilidad, la temperatura de
autoignición y la mínima energía para su inflamación.
Por ejemplo, una mezcla de gas y aire puede producir llama
únicamente cuando la mezcla contiene una proporción de gas
suficiente.
Para el gas natural, el (L.I.I.) limite inferior de inflamabilidad (5%)
es aquel hasta el cual la mezcla es pobre en combustible.
Superado el (L.S.I.) limite superior de inflamabilidad (15%) la
mezcla pasa a tener un exceso de combustible. Entre ambos
limites se encuentra toda la mezcla inflamable cuando además
coincide una energía de activación.
Si a presión atmosférica la temperatura aumenta el LII se reduce,
en cambio el L.S.I. aumenta. Si a temperatura constante varia la
presión, tenemos:
Presión 1,013 bar 7 bar 14 bar 21 bar 100 bar
L.I.I. 5% 4,98% 4,93% 4,9% 4,6%
L.I.S. 15% 18% 24% 32% 50%
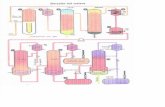
En las siguientes secciones se presenta información sobre: 1)
sistemas de procesado y recuperación de materiales, 2)
recuperación de productos de conversión química, 3) recuperación
de productos de conversión biológica, 4) recuperación de energía
de la conversión de productos, y 5) diagramas de flujo de sistemas
de recuperación de materiales y energía. En la Figura 9-1 se indica
la secuencia para la presentación de esta información, que a su
vez, es un diagrama típico de flujo para la recuperación de
recursos, conversión de productos, y energía de los desechos
sólidos. El término sistema frontal denota los procesos (reducción
de tamaño, separación, etc.) usados para recuperar materiales y la
preparación de componentes individuales para la conversión
subsiguiente. El término sistemas posteriores denota los procesos
químicos y biológicos (incineración con recuperación de calor,
fermentación controlada, etc.) e instalaciones auxiliares
relacionadas, usadas para la conversión de desechos sólidos
procesados en varios productos.
Impacto Ambiental
El CO2 emitido a la atmósfera tras la combustión del gas natural se
trata de un gas de efecto invernadero que contribuye
alcalentamiento global de la Tierra. Esto se debe a que el CO2 es
transparente a la luz visible y ultravioleta, mientras que absorbe la
radiación infrarroja que emite la superficie de la Tierra al espacio
exterior, ralentizando el enfriamiento nocturno de esta.
La combustión del gas natural produce menos gases de efecto
invernadero que otros combustibles fósiles como los derivados
petrolíferos (fuelóleo, gasóleo o gasolina) y especialmente que
elcarbón. Además es un combustible que se quema de forma más
limpia, eficiente y segura, no produce dióxido de azufre (causante
de la lluvia ácida) ni partículas sólidas.
La razón por la cual produce poco CO2 es que la molécula de su
principal componente, el metano, contiene
cuatro átomos de hidrógeno por cada uno de carbono, produciendo
dos moléculas de agua por cada una de CO2. Mientras que los
hidrocarburos de cadena larga (p. ej. los contenidos en el gasóleo)
producen prácticamente sólo una molécula de agua por cada una
de CO2 (además, la entalpía estándar de formación del agua es
muy elevada).
Sin embargo, los escapes de gas natural que se producen en los
pozos suponen un aporte muy significativo de gases de efecto
invernadero, ya que el metano equivale a 23 veces el efecto
invernadero que el dióxido de carbono (datos del IPCC). Por
ejemplo, el accidente de marzo de 2012 en la plataforma
petrolífera Elgin -operada por la petrolera Total en el Mar del
Norte- supuso un escape de unos 5,5 millones de m3
diarios.6
Como
la densidad del metano en condiciones estándar es 0,668 kg/m37
el
escape fue de 3674 toneladas diarias, que equivalen a 84 502
toneladas diarias (equivalentes de dióxido de carbono). La
duración de la detención de dicho escape se estimó en 6 meses, lo
que suponen 15 millones de toneladas equivalentes de dióxido de
carbono (las emisiones industriales de Estonia en el año 2009).
El gas natural procede generalmente de las perforaciones que se
realizan en los yacimientos petrolíferos, de la descomposición de
la materia orgánica con el tiempo.
En dichos yacimientos, el petróleo más liviano que el agua, suele
flotar sobre lagos subterráneos de agua salada. En la parte
superior se encuentra el gas, que ejerce enormes presiones, con lo
cual hace fluir el petróleo hacia la superficie.
En la figura se muestra la disposición de un yacimiento de
petróleo y gas.
Referencias
http://historiaybiografias.com/gas_natural1/
http://www.sencamer.gob.ve/sencamer/normas/2051-93.pdf
h
http://www.innergy.cl/usos.htm
https://www.google.co.ve/search?q=insumos+del+gas+natural&esp
v=2&biw=916&bih=662&site=webhp&source=lnms&tbm=isch&sa=
X&ved=0ahUKEwjJgNKVqbrNAhVHmR4KHb2ZA1QQ_AUIBigB#tbm
=isch&q=diagrama+de+bloque+del+gas+natural&imgrc=QWmeoIbg
rU71ZM%3A
tps://es.wikipedia.org/wiki/Gas_natural#Impacto_ambiental