Presentaci n 10 electroquimica - C.A.E. Centro de Apoyo al ......reacciones de transferencia de...
Transcript of Presentaci n 10 electroquimica - C.A.E. Centro de Apoyo al ......reacciones de transferencia de...

ELECTROQUÍMICA

TERMODINTERMODINÁÁMICA DE SISTEMASMICA DE SISTEMASELECTROQUELECTROQUÍÍMICOS. PILAS GALVMICOS. PILAS GALVÁÁNICAS.NICAS.22
Sistemas electroquímicos: Aquéllos en los que ocurren
reacciones de transferencia de electrones.
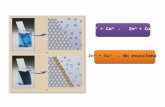
Zn + Cu2+ → Zn2+ + CuZn
Cu2+
SO42-
Zn2+
Cu
Reacción por contacto directo.
Así no es un dispositivo útil para generar
corriente eléctrica.
Pila electroquímica: Dispositivo en el que se produce una
corriente eléctrica (flujo de e- a través de un circuito) gracias a
una reacción espontánea (pila galvánica o voltaica) o en que
se utiliza corriente eléctrica para llevar a cabo una reacción
química no espontánea (célula electrolítica).

Tipos de reacciones redox (según su espontaneidad).
• Reacciones espontáneas (se produce energía eléctrica a partir de la energía liberada en una reacción química):
• Pilas voltaicasPilas voltaicas• Reacciones no espontáneas (se
producen sustancias químicas a partir de energía eléctrica suministrada):
• ElectrElectr óólisislisis

Pilas voltaicas.• Si se introduce una barra de Zn en una
disolución de CuSO4 (Cu2+ + SO42–) se
producirá espontáneamente la siguiente reacción:
• Cu2+ (aq) + Zn (s) → Cu (s) + Zn2+ (aq)• El Zn se oxida (pierde electrones) y el Cu2+
se reduce (los gana).
• Si hacemos que las reacciones de oxidación y reducción se produzcan en recipientes separados, los electrones circularán (corriente eléctrica).

Tipos de electrodos.• Se llama así a cada barra metálica
sumergida en una disolución del mismo metal. En una pila hay dos electrodos:
•• ÁÁnodonodo : Se lleva a cabo la oxidación– Allí van los aniones. – En el ejemplo anterior sería el electrodo de
Zn.
•• CCáátodotodo : Se lleva a cabo la reducción – Allí van los cationes.
– En el ejemplo anterior sería el electrodo de Cu.

Pila Daniell. • Consta de dos
semiceldas• Una con un
electrodo de Cu en una disolución de CuSO4
• Otra con un electrodo de Znen una disolución de ZnSO4.
©E
d. E
CIR
. Q
uím
ica
2º
Bac
h.

John Frederic Daniell(1790-1845)
Zn → Zn2+ + 2e-
Oxidación
Cu2+ + 2e- → Cu
Reducción
Zn (s) | Zn2+ (1 M) || Cu2+ (1 M) | Cu(s)
(-) (+)
Pila Daniell

• Están unidas por un puente salino que evita que se acumulen cargas del mismo signo en cada semicelda.
• Entre los dos electrodos se genera una diferencia de potencial que se puede medir con un voltímetro.
© Ed. ECIR. Química 2º Bach. Pila Daniell

Pilas comerciales.�
(Imágenes cedidas por © Grupo ANAYA. S.A. Química 2º Bachillerato)
Alcalina De mercurio (botón)Salina

La batería de la celda seca
Leclanché cell
Dry cell
Zn (s) Zn2+ (aq) + 2e-Anode:
Cathode: 2NH4 (aq) + 2MnO2 (s) + 2e- Mn2O3 (s) + 2NH3 (aq) + H2O (l)+
Zn (s) + 2NH4 (aq) + 2MnO2 (s) Zn2+ (aq) + 2NH3 (aq) + H2O (l) + Mn2O3 (s)
En realidad, esta ecuación es una simplificación. E=1,5 V

Batteries
Zn(Hg) + 2OH- (aq) ZnO (s) + H2O (l) + 2e-Anode:
Cathode: HgO (s) + H2O (l) + 2e- Hg (l) + 2OH- (aq)
Zn(Hg) + HgO (s) ZnO (s) + Hg (l)
Mercury Battery
E= 1,35 V. Tiene mayor capacidad y vida más larga. Se utiliza en marcapasos, aparatos auditivos, relojes electrónicos

El acumulador de plomo
Anode:
Cathode:
Lead storagebattery
PbO2 (s) + 4H+ (aq) + SO2- (aq) + 2e- PbSO4 (s) + 2H2O (l)4
Pb (s) + SO2- (aq) PbSO4 (s) + 2e-4
Pb (s) + PbO2 (s) + 4H+ (aq) + 2SO2- (aq) 2PbSO4 (s) + 2H2O (l)4
ES RECARGABLE. Consume H2SO4 de forma que se puede saber cuando se ha descargado

Batteries
Solid State Lithium Battery

Celdas combustibles
A fuel cell is an electrochemical cell that requires a continuous supply of reactants to keep functioning
Anode:
Cathode: O2 (g) + 2H2O (l) + 4e- 4OH- (aq)
2H2 (g) + 4OH- (aq) 4H2O (l) + 4e-
2H2 (g) + O2 (g) 2H2O (l)NO ALMACENAN ENERGIA. SE PARECEN A UN MOTOR.

FUERZA ELECTROMOTRIZ DE LAS PILAS.FUERZA ELECTROMOTRIZ DE LAS PILAS.POTENCIALES DE ELECTRODO.POTENCIALES DE ELECTRODO.33
La corriente eléctrica fluye debido a una diferencia de potencial entre
los dos electrodos, llamada fuerza electromotriz (fem, ∆ε).
(-) (+)
Unidades: voltios (V)
∆G = Welec = − q⋅∆ε
Fuerza impulsora
∆ε ∆G
q = n F ; F = 96485 C⋅mol-1
∆∆∆∆G = −−−− n F ∆ε∆ε∆ε∆ε

Michael Faraday(1791-1867)
∆∆∆∆G = −−−− n F ∆ε∆ε∆ε∆ε
• Reacción espontánea: ∆G < 0 ⇒ ∆ε > 0• Reacción no espontánea: ∆G > 0 ⇒ ∆ε < 0
(la reacción espontánea será la inversa)
• Equilibrio: ∆G = 0 ⇒ ∆ε = 0 (no se produce energía eléctrica;
la pila se ha agotado)
En condiciones estándar: ∆Gº = − n F ∆εº
(Concentraciones de los iones = 1 M)
∆εº es una propiedad intensiva

En lugar de tabular valores de ∆εº de todas las pilas, tabulamos
potenciales de electrodo
• Se escoge un electrodo de referencia al que por convenio se le
asigna el valor de potencial cero: Electrodo estándar de hidrógeno.
2 H+ (aq) + 2 e- ↔ H2 (g) εº = 0.00 V
• Se construyen pilas con un electrodo
de hidrógeno y otro que cuyo potencial
queramos averiguar y se mide la fem
de la pila.
• Dicha fem será el potencial estándar
del otro electrodo.

Se tabulan potenciales estándar (εº) de reducción
⇓Serie electroquímica
A mayor εº, mayor tendencia a reducirse tiene la especie oxidada del
par redox (más oxidante es).
p.ej.: Zn2+ + 2e- ↔ Zn εº = −0.76 V
Cu2+ + 2e- ↔ Cu εº = +0.34 V
Más tendencia a reducirse; más oxidante
La fem de una pila se calcula como: ∆ε∆ε∆ε∆εº = εεεεº(cátodo) −−−− εεεεº(ánodo)[reducción] [oxidación]
Para que funcione la pila (reacción espontánea): ∆εº > 0
p.ej.: 0.34 – (−0.76) = 1.10 V

Tabla de Tabla de potenciales potenciales de de reduccireducci óónn
1,51MnO4–
`+ 8 H++ 5 e– → Mn2+ + 2 H2O MnO4– / Mn2+
1,500Au3+ + 3 e– → AuAu3+ / Au
1,36Cl2 + 2 e– → 2 Cl–Cl2 / Cl–
1,07Br2 + 2 e– → 2 Br–Br2 / Br–
0,80Ag+ + 1 e– → AgAg+ / Ag
0,79Hg2+ + 2 e– → 2 HgHg2+ / Hg
0,53MnO4–
`+ 2 H2O + 3 e– → MnO2 + 4 OH–MnO4–/MnO2
0,53I2 + 2 e– → 2 I–I2 / I–
0,34Cu2+ + 2 e– → CuCu2+ / Cu
0,002 H+ + 2 e– → H2H+ / H2
–0,13Pb2+ + 2 e– → PbPb2+ / Pb
–0,14Sn2+ + 2 e– → SnSn2+ / Sn
–0,25Ni2+ + 2 e– → NiNi2+ / Ni
–0,40Cd2+ + 2 e– → CdCd2+ / Cd
–0,41Fe2+ + 2 e– → FeFe2+ / Fe
–0,74Cr3+ + 3 e– → CrCr3+ / Cr
–0,76Zn2++ 2 e– → ZnZn2+ / Zn
–1,18Mn2+ + 2 e– → MnMn2+ / Mn
–1,66Al3+ + 3 e– → AlAl3+ / Al
–2,37Mg2++ 2 e– → MgMg2+ / Mg
–2,71Na++ 1 e– → NaNa+ / Na
–2,87Ca2++ 2 e– → CaCa2+ /Ca
–2,92K+ + 1 e– → KK+ / K
–3,04Li+ 1 e– → LiLi+ / Li
E° (V) SemirreacciónSistema

E0 = 0.76 Vcelda
fem estándar (E 0 )´celda
0.76 V = 0 - EZn /Zn0
2+
EZn /Zn = -0.76 V02+
Zn2+ (1 M) + 2e- Zn E0 = -0.76 V
E0 = EH /H - EZn /Zncell0 0
+ 2+2
E0 = Ecátodo - Eánodocelda0 0
Zn (s) | Zn2+ (1 M) || H+ (1 M) | H2 (1 atm) | Pt (s)
Voltímetro
Puente salino
Electrodo de Pt
Electrodo de Zinc
Electrodo de hidrógeno
H2 gaseoso a 1 atm
EJEMPLO

Pt (s) | H2 (1 atm) | H+ (1 M) || Cu2+ (1 M) | Cu (s)
2e- + Cu2+ (1 M) Cu (s)
H2 (1 atm) 2H+ (1 M) + 2e-Ánodo (oxidación):
Cátodo (reducción):
H2 (1 atm) + Cu2+ (1 M) Cu (s) + 2H+ (1 M)
E0 = Ecatodo - Eanodocelda0 0
E0 = 0.34 Vcelda
Ecelda = ECu /Cu – EH /H 2+ +2
0 0 0
0.34 = ECu /Cu - 00 2+
ECu /Cu = 0.34 V2+0
Voltímetro
Puente salino
Electrodo de Pt
Electrodo de Cobre
Electrodo de hidrógeno
H2 gas a 1 atm
EJEMPLO

• El valor de E0 es para la reacción tal como se escribe
• Los valores más positivos de E0 se obtienen para lassustancias con mayor tendencia a reducirse
• Las semireacciones de celda son reversibles
• El signo de E0 cambia para la reacción inversa
• La modificación de los coeficientes estequiométricosde la semireacción nomodifica el valor de E0

Ejemplo: Decir si será espontánea la siguiente reacción redox:
Cl2(g) + 2 I– (aq)→ 2Cl– (aq) + I2 (s)
• La reacción dada es la suma de las siguientes semirreacciones:
•• RedRed. (c. (cáátodo)todo) : : Cl2(g) + 2e–→ 2Cl–(aq)
•• OxidOxid .. ((áánodo)nodo) :: 2 I–(aq) → I2 (s) + 2e–
• Para que la reacción sea espontánea tiene que cumplirse que ∆ Epila > 0:
∆ Epila = Ecatodo – Eánodo = +1’36 V – 0’54 V = = +0’72 V > 0
luego es espontespont ááneanea (las moléculas de Cl2 tienen más tendencia a reducirse que las de I2).

∆∆∆∆∆∆∆∆EpilaEpila = 3,17 V= 3,17 V
Ejercicio D: Una pila consta de un electrodo de Mg introducido en una disolución 1 M de Mg(NO3)2 y un electrodo de Ag en una disolución 1 M de AgNO3 . ¿Qué electrodo actuaráde cátodo y de ánodo y cuál será el voltaje de la pila
correspondiente?
•• ¿¿QuQuéé especie se reduce?especie se reduce?• La que tenga mayor potencial de reducción. En este
caso la Ag (+0,80 V) frente a los –2,37 V del Mg.
•• RedRed. (c. (cáátodo)todo) : : Ag+(aq) + 1e–→ Ag(s)
•• OxidOxid .. ((áánodo)nodo) :: Mg(s) → Mg2+(aq) + 2e–
• ∆Epila = Ecatodo – Eánodo = +0,80 V – (–2,37 V)

Ejercicio E: Dada lasiguiente tabla de potencia-
les normales expresados en voltios:a) Escriba el nombre de: -La forma reducida del oxidante más fuerte. -Un catión que pueda ser oxidante
y reductor. -La especie más reductora.
-Un anión que pueda ser oxidante y reductor. b) Escriba y ajuste dos reacciones que sean espontaneas entre especies de la tabla que correspondan a: -Una oxidación de un catión por un anión.
-Una reducción de un catión por un anión.
Cuestión de Selectividad
Cuestión de Selectividad
Par redox E0 (V)
Cl2 / Cl– 1,35
ClO4–/ClO3
– 1,19
ClO3–/ClO2
– 1,16
Cu2+/Cu0 0,35
SO32–/ S2– 0,23
SO42– / S2– 0,15
Sn 4+/Sn2+ 0,15
Sn2+ / Sn0 -0,14
Cl–
Sn2+
Sn0
ClO3–
ClO3–+ Sn2+ + 2 H+ →→→→ ClO2
– + Sn4+ + H2O
S2– + 4 Cu2+ + 4 H2O →→→→ SO42– + 8 H+ + 4 Cu

¿Cual es la fem de una celda electroquímica hecha de un electrodo de Cd en una disolución 1,0 M de Cd(NO3)2 y de un electrodo de Cr en una disolución 1,0 M de Cr(NO3)3?
Cd2+ (ac) + 2e- Cd (s) E0 = -0.40 V
Cr3+ (ac) + 3e- Cr (s) E0 = -0.74 V
Cd es más oxidante
Cd oxidará al Cr
2e- + Cd2+ (1 M) Cd (s)
Cr (s) Cr3+ (1 M) + 3e-Ánodo (oxidación):
Cátodo (reducción):
2Cr (s) + 3Cd2+ (1 M) 3Cd (s) + 2Cr3+ (1 M)
x 2
x 3
E0 = Ecatodo - Eanodocelda0 0
E0 = -0.40 – (-0.74) celda
E0 = 0.34 V celda

DEPENDENCIA DE LA FEM CON LASDEPENDENCIA DE LA FEM CON LASCONCENTRACIONES. ECUACICONCENTRACIONES. ECUACIÓÓN DE NERNST.N DE NERNST.44Si las condiciones no son estándar ¿cuánto vale la fem?
∆G = ∆Gº + RT ln Q
∆G = − n F ∆ε∆Gº = − n F ∆εº
− n F ∆ε = − n F ∆εº + RT ln Q
Q- lnnF
RTεºε ∆=∆ Ecuación de Nernst
A 25ºC : Q- logn
0.0592εºε ∆=∆

EspontaneidadEspontaneidad de de laslas reaccionesreacciones RedoxRedox
∆G = -nFEcelda
∆G0 = -nFEcelda0
n = número de moles de electrones en la reacción
F = 96.500J
V • mol = 96.500 C/mol
∆G0 = -RT ln K= -nFEcelda0
Ecelda0 =
RTnF
ln K(8.314 J/K•mol)(298 K)
n (96,500 J/V•mol)ln K=
=0.0257 V
nln KEcelda
0
=0.0592 V
nlog KEcelda
0

Walther Hermann Nernst(1864-1941)
“En reconocimiento a su trabajo en termoquímica”.
1920
Premio Nobel de Química

Otras aplicaciones de la ecuación de Nernst
a) Obtención de constantes de equilibrio de reacciones redox
En el equilibrio: ∆ε = 0 y Q = Keq
C)25º(a10K
Klogn
0.0592εº0;log
n
0.0592εºε
0.0592
∆εºn
eq
eq
=
∆=∆=∆ -Q-
b) Obtención de εº en condiciones no estándar
C)25º(a10K
Klogn
0.0592εº0;log
n
0.0592εºε
0.0592
∆εºn
eq
eq
=
∆=∆=∆ -Q-
Q- logn
0.0592εºε =
A 25ºC : Q- logn
0.0592εºε =

c) Determinación de productos de solubilidad.
Se usa cuando se conocen los potenciales de dos semirreacciones
que combinadas dan el equilibrio de solubilidad buscado.
AgCl (s) + 1e- ↔ Ag (s) + Cl- (aq) εº = 0.222 V
Ag+ (aq) + 1e- ↔ Ag (s) εº = 0.799 V
AgCl (s) + 1e- ↔ Ag (s) + Cl- (aq)
Ag (s) ↔ Ag+ (aq) + 1e-
AgCl (s) ↔ Ag+ (aq) + Cl- (aq) ∆εº = 0.222-0.799 = −0.577 V
( )(AgCl)K108.11010K PS
100592.0
577.01
0.0592
∆εºn
eq =⋅=== −
−⋅

2e- + Fe2+ Fe
2Ag 2Ag+ + 2e-Oxidation:
Reduction:
What is the equilibrium constant for the following reaction at 250C? Fe2+ (aq) + 2Ag (s) Fe (s) + 2Ag+ (aq)
=0.0257 V
nln KEcell
0
E0 = -0.44 – (0.80)
E0 = -1.24 V
0.0257 Vx nE0
cellexpK =
n = 2
0.0257 Vx 2-1.24 V
= exp
K = 1.23 x 10-42
E0 = EFe /Fe – EAg /Ag0 0
2+ +

TIPOS DE ELECTRODOS.TIPOS DE ELECTRODOS.555.1. Electrodos activos.
• Participan en la reacción química de la pila.
• Se consumen o forman a medida que se produce la reacción.
p.ej.: pila Daniell ⇒ Varillas de Zn y Cu (Zn + Cu2+ → Zn2+ + Cu)
5.2. Electrodos inertes.
• No participan en la reacción química de la pila.
• Sólo proporcionan el soporte donde ocurre la transferencia de e-
p.ej.: Varilla de Pt (Cu + 2 Fe3+ → Cu2+ + 2 Fe2+)
5.3. Electrodos de gas.
• En él participa una especie gaseosa. p.ej.: electrodo de hidrógeno

Electrólisis• Cuando la reacción redox no es espontánea en un
sentido, podrá suceder si desde el exterior se suministran los electrones.
• En el ejercicio D anterior en el que el electrodo de Magnesio hacía de ánodo y se oxidaba frente al de plata que hacía de cátodo formando una pila de f.e.m = 3,17 V, se puede forzar la formación de Mg(s) (reducción) si desde el exterior se suministran los 3,17 V que se necesitan vencer (por ejemplo usando una pila que proporcione mayor voltaje).

Aplicaciones de la electrólisis.• Se utiliza industrialmente para obtener
metales a partir de sales de dichos metales utilizando la electricidad como fuente de energía.
• Se llama galvanoplastia al proceso de recubrir un objeto metálico con una capa fina de otro metal:
•• Ejemplo:Ejemplo: Zn2+ + 2 e– → Zn (cincado)(en este caso los electrones los suministra la corriente eléctrica)

Aplicaciones de la electrólisis.
© Editorial ECIR. Química 2º Bachillerato.
Electrorrefinado del Cu. Electrodeposición de Ag.

Comparación de la polaridad de los electrodos en pilas y electrólisis.
© ECIR. Química 2º Bachillerato

Electrólisis. Ecuación de Faraday.
• La carga de un electrón es de 1’6 x 10–19 C y la de 1 mol de electrones (6’02 x 1023) es el producto de ambos números: 96500 C = 1 F.
• Con un mol de electrones se es capaz de reducir 1 mol de metal monovalente o ½ mol de metal divalente, es decir, un equivalente del metal (Mat/valencia).
• 1 equivalente precisa 96500 Cneq (m (g)/Meq) precisarán Q

Ecuación de Faraday (cont.).
• De la proporción anterior se deduce:
m Qneq = —— = —————
Meq 96500 C/eq
• De donde, sustituyendo Q por I · t (más fáciles de medir) y despejando “m” se obtiene:
× × × ×= =
×-( )
96500 º 96500eq at
M I t M I tm g
n e

Ejemplo: Se realiza la electrólisis de un disolución de tricloruro de hierro, haciendo pasar una corriente de 10 A durante 3 horas. Calcula la cantidad de hierro depositado en el cátodo.
• El tricloruro en disolución estará disociado:FeCl3 → 3 Cl– + Fe3+
• La reducción será: Fe3+ + 3 e– → FeM/nº e- x I x t (55,8/3) g/eq x 10 A x 3 x 3600 s
m (g) = ————— = —————————————96500 C/eq 96500 C/eq
m (g) = m (g) = 20,82 g20,82 g

Ejercicio F: Una corriente de 4 amperioscircula durante 1 hora y 10 minutos a través de dos
células electrolíticas que contienen, respectivamente, sulfato de cobre (II) y cloruro de aluminio, a) Escriba las reacciones que se producen en el cátodo de ambas células electrolíticas.b) Calcule los gramos de cobre y aluminio metálicos que se habrán depositado. Datos: Masas atómicas: Cu = 63,5 y Al = 27,0. Constante de Faraday : F = 96500 C·eq-1
a)a) Cu2+ + 2 e– → Cu ; Al3+ + 3 e– → Al
b) b) Meq · I · t (63,5/2) g/eq·4 A· 4200 sm (Cu) = ————— = ——————————— = 5,53 g5,53 g
96500 C/eq 96500 C/eq
Meq · I · t (27,0/3) g/eq·4 A· 4200 sm (Al) = ————— = ——————————— = 1,57 g1,57 g
96500 C/eq 96500 C/eq
Problema Selectividad
Problema Selectividad

¿Qué cantidad de Ca se producirá en una celdaelectrolítica de CaCl2 fundido si se hace pasar a través de la celda una corriente de 0,452 A durante 1,5 horas?
Ánodo:
Cátodo: Ca2+ (l) + 2e- Ca (s)
2Cl- (l) Cl2 (g) + 2e-
Ca2+ (l) + 2Cl- (l) Ca (s) + Cl2 (g)
2 moles e- = 1 mol Ca
mol Ca = 0.452Cs
x 1.5 hr x 3600shr 96.500 C
1 mol e-x
2 mol e-
1 mol Cax
= 0.0126 mol Ca
= 0.50 g Ca

Electrólisis del NaCl• La reacción 2 Na + Cl2 → 2 NaCl es una reacción
espontánea puesto que E(Cl2/2Cl–) > E(Na+/Na) • Y lógicamente, la reacción contraria será no
espontánea: 2 NaCl → 2 Na + Cl2
•• RedRed. (c. (cáátodo)todo) : : 2 Na+(aq) + 2e– → 2 Na (s)
•• OxidOxid .. ((áánodo)nodo) :: 2Cl–(aq) → Cl2(g) + 2e–
Epila = Ecatodo – Eánodo = –2’71 V – 1’36 V = – 4’07 VEl valor negativo de Epila reafirma que la reacción no es
espontánea. Pero suministrando un voltaje superior a 4’07 V se podrá descomponer el NaCl en sus elementos: Na y Cl2

Electrólisis del NaCl
© Ed. Santillana. Química 2º Bachillerato

Electrolisis del aguaBatería
CátodoÁnodo
Oxidación Reducción
Disolución diluida de H2SO4

Corrosión.
Gota de agua corroyendo
una superficie de hierro.© Ed. Santillana. Química 2º
• Un problema muy importante es la corrosión de los metales; por ejemplo, el hierro:
•• OxidOxid .. ((áánodo)nodo) ::Fe (s) → Fe2+(aq) + 2e–
•• RedRed. (c. (cáátodo)todo) : : O2(g) + 4 H+(aq) + 4e– → 2 H2O(l)
• En una segunda fase el Fe2+ se oxida a Fe3+ :
4 Fe2+(aq) + O2(g) + 4 H2O(l) →2 Fe2O3(s) + 8 H+(aq)

Protección catódica.• Sirve ara prevenir la
corrosión.• Consiste en soldar a
la tubería de hierro a un ánodo de Mg que forma una pila con el Fe y evita que éste se oxide, ya que que quien se oxida es el Mg.
Tubería protegida por un ánodo de
Magnesio.© Grupo ANAYA S.A. Química 2º.

APLICACIONES ELECTROLISIS
Cu (s) (impure) Cu2+ (aq) + 2e-
Cu2+ (aq) + 2e- Cu (s) (pure)
PURIFICACIÓN DE METALES
El cobre en sus menas contiene impurezas como el zinc, la plata, hierro y oro.Los metales reactivos en el ánodo de cobre como el hierro y el zinc se oxidan y pasan a la disolución. Los metales mas electropositivos no se disuelven pero según se disuelve el ánodo de cobre, estos metales caen al fondo de la celda.

AluminumImpure Al2O3 (s) + 2OH- (aq) 2AlO2
- (aq) + H2O (l)
AlO2- (s) + H3O+ (aq) Al(OH)3 (s)
2Al(OH)3 (s) Al2O3 (s) + 3H2O (g)∆
Anode:
Cathode:
3[2O2- O2 (g) + 4e-]
4[Al3+ + 3e- Al (l)]
2Al2O3 4Al (l) + 3O2 (g)
BAUXITA (Al2O3.2H20)CRIOLITA (Na3AlF6)

Chemistry In Action: Recycling Aluminum