Practica 17 Isomeria Esructural y Estereoisomeria
-
Upload
ernesto-zapata-diaz -
Category
Documents
-
view
148 -
download
6
Transcript of Practica 17 Isomeria Esructural y Estereoisomeria

05/06/2011
1
PRACTICA Nº 17ISOMERÍA
ESTRUCTURAL Y ESTEREOISOMERIA
CONCEPTOS BÁSICOS:
ISOMERÍA:Es una propiedad de ciertos compuestos químicos que con igual fórmula
química, es decir, iguales proporciones relativas de los átomos que conforman su molécula, presentan estructuras moleculares distintas. Dichos compuestos reciben la denominación de isómeros.
ISOMEROS:Son compuestos que tienen la misma fórmula molecular pero diferente
fórmula estructural (y por tanto diferentes propiedades). Por ejemplo, el alcohol etílico o etanol y el éter dimetílico.
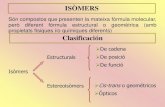
ISÓMERO ESTRUCTURAL:Los isómeros estructurales difieren en la forma de unir los átomos y a
su vez se clasifican en isómeros de cadena de posición y de función.

05/06/2011
2
ISÓMERO DE CADENA:
• Tienen componentes de la cadena acomodados en diferentes lugares.
• Se distinguen por la diferente estructura de las cadenas carbonadas.
ISÓMERO DE POSICIÓN:
• Los grupos funcionales de un compuestos, se unen de diferentes posiciones.
• El grupo funcional ocupa una posición diferente en cada isómero

05/06/2011
3
ISÓMERO DE FUNCIÓN:Aquí, la diferente conectividad de los átomos, pueden generar diferentes grupos funcionales en la cadena.
El grupo funcional es diferente
.
ESTEREOISOMEROS:tienen todos los enlaces idénticos y se diferencian por la disposición espacial de los grupos. Se clasifican: * isómeros cis - trans o geométricos,
* enantiómeros * diastereoisómeros.
ESTEREOISOMEROS CONFORMACIONALES:
• Son no aislables por separado a temperatura ambiente.
• Se llaman CONFORMEROS.• La transformación de unos en
otros consiste en giros de grupos en el espacio alrededor de enlaces sencillos.
• A temperatura ambiente se interconvierten tan rápidamente que resulta imposible mantenerlos aislados por separado.

05/06/2011
4
ESTEREOISOMEROS CONFIGURACIONALES: Son estereoisómeros aislables por separado a temperatura
ambiente o próxima a ella. En la mayor parte de los casos para transformar uno en otro, no
basta con realizar giros alrededor de enlaces sencillos sino que es necesario romper y formar enlaces.
ISÓMEROS GEOMÉTRICOS: Los que se originan por la distinta orientación de átomos o grupos
respecto de un doble enlace o un plano de anillo.
ISÓMEROS CIS/TRANS: Son compuestos que difieren en la disposición espacial de sus
grupos. Se llaman CIS los isómeros geométricos que tienen los grupos al mismo lado y TRANS los que lo tienen a lados opuestos.
DESIGNACIÓN E -Z: Según las Reglas de Cahn-Ingold-Prelog. Si los
sustituyentes de mayor prioridad están juntos se les denomina Z (del alemán Zusammen = Juntos), si están opuestos se les denomina E (de Engegen = de través)
cis y trans-2-ButenoIsómeros cis y trans del 2-Buteno
cis y trans del 1,2-Dimetilciclopentano

05/06/2011
5
ISÓMEROS ÓPTICOS:
Los que se originan por la distinta orientación espacial en torno a un estereocentro (generalmente un C con hibridación sp3 unido a 4 sustituyentes distintos).
CENTRO QUIRAL O ASIMÉTRICO:
Se llama centro quiral o asimétrico a un átomo unido a cuatro sustituyentes diferentes. Una molécula que posee un centro quiral tiene una imagen especular no superponible con ella, denominada enantiómero.
ENANTIÓMEROS:Los enantiómeros son imágenesespeculares no superponibles. Se caracterizan por poseer un átomo unido a cuatro grupos distintos llamado asimétrico o quiral.
Enantiómeros: (R) y (S)-1-Bromo-1-cloroetano
La presencia de un carbono asimétrico (con sustituyentes distintos: metilo, hidrógeno, cloro y bromo) hace posible que la molécula y su imagen especular sean distintas.
(R) y (S)-Alanina

05/06/2011
6
DIASTEROISOMEROS:
Moléculas que se diferencian por la disposición espacial de los grupos.
No son imágenes especulares. Deben tener dos centros quirales. En uno los sustituyentes están dispuestos igual en ambas moléculas
y en el otro deben cambiar.
Alquenos cis y trans.
REGLAS PARA NOMBRAR ENANTIÓMEROS:
Para dar notación R/S a un centro quiral es necesario:
1. A los átomos unidos al quiral se debe poner números atómicos (en isótopos, tiene prioridad el de mayor masa atómica).
2. Cuando dos o más sustituyentes tienen la misma prioridad, se continua comparando las cadenas átomo a átomo hasta encontrar un punto de diferencia.

05/06/2011
7
3. Los enlaces dobles y triples se desdoblan considerándolos como si fueran enlaces sencillos.
4. Para asignar notación R/S:Seguimos el orden de prioridades a, b, c de los sustituyentes. De acuerdo al sentido de las agujas del reloj: el centro es R (rectus-derecha).Si se sigue el sentido contrario a las agujas del reloj: es S (sinester-izquierda).
SE APLICA SOLO: cuando el grupo d está hacia el fondo del plano(enlace a trazos), si d sale hacia nosotros (cuña) la notación es la contraria (R giro a la izquierda, S giro a la derecha).
MEZCLA RACEMICA: Mezcla equimolar de enantiómeros (50%R, 50%S). Uno de los enantiómeros de la mezcla gira el plano de polarización
de la luz el mismo ángulo pero en sentido contrario que el otro. La mezcla en igual proporción de ambos enantiómeros no muestra
rotación óptica y es por tanto ópticamente inactiva.
FORMA MESO:Molécula aquiral debido a la presencia de un elemento de simetría
(plano, centro de inversión o eje impropio).
Aunque las formas meso presentan carbonos asimétricos, el plano de simetríaelimina su quiralidad y por tanto su capacidad para rotar la luz polarizada.
ACTIVIDAD ÓPTICA:Los enantiómeros presentan propiedades físicas idénticas, Excepto su comportamiento frente a la luz polarizada. Dextrógiro (+): gira en el sentido de las agujas del reloj, Levógiro (-): gira en sentido contrario al de las agujas del reloj

05/06/2011
8
OBJETIVOS: Conocer la Isomería y Estereoisomería del Carbono. Reconoce la capacidad enlazante del carbono formando
estructuras biológicas. Detalla la estere isomería y su fundamento en aplicaciones biológicas.
COMPETENCIAS:
Competencias cognoscitivas: Reconoce los conceptos teóricos básicos de isomería y
esterosisomería en compuestos químicos y su comportamiento biológico.
Reconoce e identifica los problemas planteados en estereoisomerìa. Competencias procedimentales: Integra los conceptos teóricos y las aplicaciones de la
estereoisomería en compuestos y su comportamiento biológico. Desarrolla las ecuaciones Redox, identificando la actividad química
que se desarrolla en la reacción. Identifique el agente reductor – agente oxidante.
Competencias actitudinales:* Describe en forma correcta los problemas que se presentan en estereoisomería y plantee una solución, con la participación activa del grupo y la supervisión y conducción del facilitador.
PROBLEMAS
1. ¿Cuál o cuáles son correctas?a) El hexano tiene 5 isómeros estructurales.b) El heptano tiene 9 isómeros estructurales.c) El etano no tiene isómeros estructurales.
2. ¿Cuántos enantiómeros tiene el ácido láctico? a)2 b) 3 c) 4 d) 5 e) 6
3. Cuales son correctas?a) El 2-bromo-3-cloro butano muestra 4 isómeros ópticos.b) El 2,3-diclorobutano muestra 4 isómeros ópticos.c) El 2,3-dihidroxibutanodioico tiene 3 isómeros ópticos.

05/06/2011
9
4. Dadas las fórmulas:
I. CH3-CH2-CHO II. CH3-CH2-O-CH2CH3III. CH3-CH2-CH2-CH2-OH IV. CH3-C – CH3V. CH3-CH2-CH-CH3 ║
OH ONo es correcto:a) II y III son isómeros funcionales. d) III y V son isómeros de posición.b) I y IV son isómeros de función. e) II y V son isómeros de función.c) II y IV son isómeros funcionales.
5. Dadas las estructuras:
I. CH2-CH=CH–CH2 IV. CH3-CH2-COO-CH3OH OH
II. CH3-CH2-CH2-COOH V. CH3-O-CH=CH-O-CH3III. CH3-CH2-CH2-CHO
No es correcto:a) I y IV son isómeros funcionales. d) II, IV y V son isómeros de función.b) II y III son isómeros de función. e) I y II son isómeros funcionales.
c) IV y V son isómeros funcionales.
Conclusiones
1. Conocer y reconocer isómeros, Diasteroisomeros y Enantiomeros.
2. Seguir los pasos descritos para nombrar enantiomeros.
3. Evaluar las estructuras de las moléculas y poder identificar su rotación óptica.
4. Analizar estructuras isómeras, diateroisomeras y enantiomeras con actividad biológica, terapéutica u odontológica.

















![1 hibridacion isomeria[1][1]](https://static.fdocuments.mx/doc/165x107/5596a15f1a28ab4e718b488f/1-hibridacion-isomeria11.jpg)
