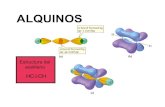
Los Alquinos
-
Upload
edris-compres -
Category
Documents
-
view
30 -
download
0
Transcript of Los Alquinos

Los AlquinosLos alquinos son hidrocarburos alifáticos con al menos un triple enlace -C≡C- entre dos átomos de carbono. Se trata de compuestos metaestables debido a la alta energía del triple enlace carbono-carbono.
Su fórmula general es CnH2n-2.
Nomenclatura:Para que den nombre a los hidrocarburos del tipo alquino se siguen ciertas reglas similares a las de los alquenos.
1. Se toma como cadena principal la cadena continua más larga que contenga el o los triples enlaces.
2. La cadena se numera de forma que los átomos del carbono del triple enlace tengan los números más bajos posibles.
3. Dicha cadena principal a uno de los átomos de carbono del enlace triple. Dicho número se sitúa antes de la terminación -ino. Ej.: CH3-CH2-CH2-CH2-C≡C-CH3, hept-2-ino.
4. Si hay varios triples enlaces, se indica con los prefijos di, tri, tetra... Ej.: octa-1,3,5,7-tetraino, CH≡C-C≡C-C≡C-C≡CH.
5. Si existen dobles y triples enlaces, se da el número más bajo al doble enlace. Ej.: pent-2-en-4-ino, CH3-CH=CH-C≡CH
6. Los sustituyentes tales como átomos de halógeno o grupos alquilo se indican mediante su nombre y un número, de la misma forma que para el caso de los alcanos. Ej.: 3-cloropropino, CH≡C-CH2Cl; 2,5-dimetilhex-3-ino, CH3-C(CH3)-C≡C-C(CH3)-CH3.
CH CH etino(acetileno) CH3–C CH propino CH3–CH2–C CH 1-butino CH3-C C-CH3 2-butino CH C- etinilo CH C-CH2– 2-propinilo CH3–C C- 1-propinino CH3–CH2–CH2–C CH 1-pentino

Serie Homologa:
Fórmula NombreCH≡CH Etino (Acetileno)CH≡C–CH3 PropinoCH≡C–CH2–CH3 1-ButinoCH≡C-(CH2)2–CH3 1-PentinoCH≡C-(CH2)3–CH3 1-HexinoCH≡C–(CH2)4–CH3 1-HeptinoCH≡C–(CH2)5–CH3 1-OctinoCH≡C–(CH2)6–CH3 1-NoninoCH≡C–(CH2)7–CH3 1-Decino
Propiedades Fisicas:Son insolubles en agua, pero bastante solubles en disolventes orgánicos usuales y de baja polaridad: ligroína, éter, benceno, tetracloruro de carbono. Son menos densos que el agua y sus puntos de ebullición muestran el aumento usual con el incremento del número de carbonos y el efecto habitual de ramificación de las cadenas. Los puntos de ebullición son casi los mismos que para los alcanos o alquenos con el mismo esqueleto carbonado.
Los tres primeros términos son gases; los demás son líquidos o sólidos. A medida que aumenta el peso molecular aumentan la densidad, el punto de fusión y el punto de ebullición.
1. Estado Físico: son gases hasta el C5, líquidos hasta el C15 y luego sólidos 2. Puntos de Ebullición: son más altos que los de los correspondientes alquenos y alcanos 3. Puntos de Fusión: se puede decir lo mismo que para el punto de ebullición 4. Densidad: igual que en los casos anteriores 5. Solubilidad: se disuelven en solventes no polares
Los acetilenos son compuestos de baja polaridad, por lo cual sus propiedades físicas son muy semejantes a la de los alquenos y alcanos.

Propiedades Químicas:
Los alquinos a diferencia de los alquenos son muy reactivos, y pueden reaccionar con muchos agentes. En general la química de los alquinos, y en especial la del acetileno, como componente más abundante y barato, es compleja y peligrosa. Una importante parte de los compuestos producidos partiendo de este gas son sustancias explosivas. Usando ciertas condiciones, los alquinos pueden reaccionar con cationes metálicos para formar derivados metálicos sólidos (sales orgánicas).
Con el sodio, potasio y litio forman compuestos estables en seco, pero que se descomponen al hidrolizarlos (agregar agua) regenerándose el alquino original. Sin embargo los derivados metálicos delcobre y la plata, se pueden manipular de manera segura solo cuando están húmedos, si están secos, son muy inestables y pueden descomponerse con violencia explosiva al ser golpeados. Una mezcla de acetileno y cloro reacciona de manera explosiva al ser iluminada. Los alquinos también pueden ser polimerizados como los alquenos, estos son procesos complejos.
El ácido sulfúrico acuoso en presencia de Sulfato de mercurio como catalizador hidrata los alquinos, dando Cetonas. La hidroboración con boranos impedidos, seguida de oxidación con Agua oxigenada, produce Enoles que se Tautomerizan a Aldehídos o Cetonas. El Bromo molecular y los haluros de alquilo se adicionan a los alquinos de forma similar a los Alquenos.
Reacciones:Muchas de las reacciones de los alquinos son reacciones de adición que siguen el siguiente esquema:
Otras de las reacciones de los alquinos se deben a la acidez del hidrógeno de los alquinos terminales.
Tipo Reacción

Hidrogenación
Hidro-halogenac
ión(X = Cl,
Br, I)(markovni
kov)Hidro-
bromacióncon
peróxidos(antimarkovnikov)
Hidratación
(markovnikov)
Hidroboración-
oxidación(antimarkovnikov)
Halogenación
(X = Cl, Br)
Ozonólisis

Tratamiento con
KMnO4 en caliente
Acidez dealquinosterminale
s
Obtención:
Los alquinos se obtienen mediante reacciones de eliminación a partir de dihaloalcanos vecinales o geminales. Se obtiene acetileno por la simple adición controlada de agua al Carburo de calcio (CaC2) a temperatura normal. Como el carburo de calcio es una sustancia muy barata, que sale de calentar cal viva (CaO) con Carbón, el acetileno es un gas barato y fácil de producir.
Usos Industriales:
El acetileno es un gas de olor etéreo cuando es puro. Arde fácilmente en el aire y, si tiene suficiente cantidad de oxígeno, arde con gran desprendimiento de calor (la temperatura de la llama alcanza los 3000 grados centígrados, por lo que se usa en soldaduras y para corte de metales) La mayor parte de los alquinos se fabrica en forma de acetileno. A su vez, una buena parte del acetileno se utiliza como combustible en la soldadura a gas debido a las elevadas temperaturas alcanzadas.En la industria química los alquinos son importantes productos de partida por ejemplo en la síntesis del PVC (adición de HCl) de caucho artificial etc. El grupo alquino está presente en algunos fármacos citostáticos. Los polímeros generados a partir de los alquinos, los polialquinos, son semiconductores orgánicos y pueden ser dotados parecido al silicio aunque se trata de materiales flexibles.