Ley de fick, presión osmótica
-
Upload
guia-biofisica -
Category
Education
-
view
2.380 -
download
9
Transcript of Ley de fick, presión osmótica

Ley de Fick, presión osmótica

Flujo neto de difusión Jneto=J12-J21
El flujo difusivo que atraviesa una superficie (J) es directamente proporcional al gradiente de
concentración.
Difusión y ley de Fick

El coeficiente de difusión en la membrana, Dm, representa el grado de resistencia que ofrece la membrana al paso del soluto.
Es específico
Ley de Fick

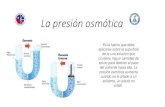
Es la presión que ejercen las moléculas de agua sobre la membrana celular.
Depende de la cantidad agua con relación a la de solutos en el medio.
Tiende a ser igual a ambos lados de la membrana en condiciones normales.◦ Sus fluctuaciones ocasionan el movimiento de
moléculas en ambas direcciones a través de la membrana.
Presión osmótica

Presión osmótica

Presión osmótica

Medios hipertónico e hipotónico

En las plantas, las soluciones hipotónicas producen presiones osmóticas que causan una presión de turgor.
◦ Turgencia significa que la célula está muy llena y se infla. ◦ Mantiene las plantas erguidas en medio hipotónico.
En condiciones hipertónicas las plantas se marchitan.
Células vegetales y presión osmótica

Células vegetales y presión osmótica
Solución hipotónica Hipertónica Hipertónica

Células animales y presión osmótica

Calcular la presión que ejerce una solución 1 M, a 0ºC
Nota: se cumple para soluciones diluidas
Presión y ley general de los gases

¿Cómo cambia la presión osmótica cuando el soluto es un electrólito?
El factor van’t Hoff (i) se utiliza para modificar las ecuaciones de las propiedades coligativas.
i depende de la molalidad
de la solución
i = núm. de partículas en solución después de la disociación
núm de partículas en solución antes de la disociación

Expresa la concentración de partículas osmóticamente activas
Toma en cuenta el factor Van’t Hoff
Ejercicio: Calcular la osmolaridad de la solución fisiológica.
Osmolaridad

Si la mem deja pasar al agua y al soluto, no
Se basa en la cantidad de moléculas del soluto que se reflejan
Coeficiente de reflexión o de Staverman
𝝈=𝝅𝒆𝒇𝒆𝒄𝒕𝒊𝒗𝒂
𝝅𝒄𝒂𝒍𝒄𝒖𝒍𝒂𝒅𝒂

Si la mem es impermeable al soluto (σ=1), la sol. es isoosmótica e isotónica.
Si hay cierta permeabilidad (σ<1), la sol. es isoosmótica pero no isotónica.
¿Es lo mismo soluciones isotónicas e isoosmóticas?
Ejemplo: el glicerol tiene σ=0.88 en el eritrocito. Calcular su osmolaridad efectiva.