Hidrocarburos
-
Upload
charito-ybarra -
Category
Business
-
view
8.258 -
download
2
Transcript of Hidrocarburos

Rosario Ybarra Miranda
HIDROCARBUROS

• Es el grupo de compuestos orgánicos más sencillo, porque sólo están formados por carbono e hidrógeno.
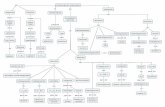
Hidrocarburos acíclicos y cíclicos
• Según la estructura de enlaces entre los átomos de carbono, se clasifican en:
Aromáticos
Hid
roca
rbur
os
Acíclicos
Cíclicos
Saturados
InsaturadosAlquenos
Alquinos
Nafténicos
Alcanos
Rosario Ybarra Miranda

HIDROCARBUROS ALICICLICOS
Rosario Ybarra Miranda

• Son hidrocarburos acíclicos saturados (o alifáticos).
• Se disponen en el espacio en forma simétrica y se orientan hacia los vértices de un tetraedro regular, lo que les permite enlaces simples entre sus átomos.
• Su fórmula general es CnH2n+2 ,donde “n” es el número de átomos de carbono presentes en la molécula.
Para un alcano de 12 átomos de carbono
C12H26
Molécula
de metanoC
H
H
HH
Rosario Ybarra Miranda

Rosario Ybarra Miranda
Nº de C PREFIJOS FÓRMULA NOMBRE
1 met CH4 metano
2 et C2H6 etano
3 prop C3H8 propano
4 but C4H10 butano
5 pent C5H12 pentano
6 hex C6H14 hexano
7 Hept C7H16 heptano
8 oct C8H18 octano
9 non C9H20 nonano
10 dec C10H22 decano
11 undec C11H24 undecano
12 dodec C12H26 dodecano
20 icos C20H42 icosano
Para nombrar a los alcanos seguimos las reglas de la IUPAC.
• Se usa el sufijo o terminación “ano”.
• Para indicar el número de carbonos en la cadena, usamos un prefijo que depende del número de carbonos en la molécula.

Rosario Ybarra Miranda
• Para nombrar cadenas ramificadas observemos el siguiente ejemplo:
CH3 - CH - CH2 - CH - CH2 - CH2 - CH3
CH3 CH2 - CH3
1 2 3 4 5 6 7 Se enumera la cadena mas larga
Cadena principal : Heptano
Sustituyentes: metilo , etilo
Nominación: 4-etil-2-metilheptano
• Los alcanos se encuentran en la naturaleza como petróleo y gas natural. A escala industrial se obtienen por destilación fraccionada del petróleo y del gas natural.
• En el laboratorio se obtienen mediante la síntesis de Wurtz.

PROPIEDADES FÍSICAS
• Los alcanos son compuestos apolares, insolubles en agua.
• Tienen puntos de fusión y ebullición relativamente bajos. A medida que aumenta el número de átomos de carbono, aumenta el punto de fusión, de ebullición y la densidad.
5 10 15 200
-100
0
150
300
400
Número de carbonos
Pun
to d
e eb
ullic
ión
ºC
Gases
Líquidos
Sólidos
Rosario Ybarra Miranda

Rosario Ybarra Miranda
• Son poco reactivos por eso se llaman parafinas. Sus enlaces simples son muy estables y difíciles de romper.
PROPIEDADES QUÍMICASR
EA
CC
ION
ES
• Combustión. Arden en presencia de oxígeno y producen dióxido de carbono y agua.
• Sustitución con halógenos. Reaccionan con cloro y bromo, para dar halogenuros de alquilo, como resultado de la sustitución de un hidrógeno por un halógeno.
• Craking o craqueo. Es la ruptura mediante el calor o por catalizadores de un hidrocarburo de cadena muy larga. El craqueo del petróleo permite la producción de la gasolina.

Rosario Ybarra Miranda
APLICACIONES DE ALCANOS
• Se usan como combustibles: gasolina, diesel, kerosene y gas licuado de petróleo (GLP).
PR
OD
UC
TO
S D
E
HA
LOG
EN
AC
IÓN
• Tetracloruro de carbono. Disolvente de pinturas.
• Cloroformo. Fue uno de los primeros anestésicos.
• Cloro metano. Materia prima para obtener gomas de silicona.
• Diclometano. Disolvente de fibras.

• También llamados olefinas, son hidrocarburos acíclicos no saturados.
• Presentan hibridación sp2 y se orientan hacia los vértices de un triángulo equilátero que poseen enlace doble.
• Su fórmula general es CnH2n , y se usa cuando presenta un solo enlace doble en la cadena.
• Para nombrar a los alquenos se usa la raíz del nombre de los alcanos, pero cambiando la terminación “ano” por “eno”.
CH3 - CH CH - CH2 - CH2 - CH3
1 2 3 4 5 6 Se enumera la cadena por el extremo más cercano al
enlace doble
Cadena principal: 6C , un enlace doble, hexeno
Sustituyentes: no tiene
Nominación: 2- hexeno Rosario Ybarra Miranda

Rosario Ybarra Miranda

Rosario Ybarra Miranda
• Los alquenos que tienen más de un enlace doble se denominan polialquenos y para nombrarlos se usan los sufijos dieno, trieno, etcétera, según los enlaces presentes.
CH3 - CH - CH2 - C C CH3
6 5 4 3 2 1
Cadena principal: 6C, dos enlaces dobles, hexadieno
Nominación: 3 - etil - 5 - metil - 1,2 - hexadieno
CH3 CH2 - CH3
Sustituyentes: metilo , etilo
• Los alquenos de interés industrial se obtienen por cracking de fracciones de petróleo.
• Sintéticamente se obtienen por deshidrogenación, deshalogenación y la deshidrohalogenación.

PROPIEDADES FÍSICAS• Los tres primeros alquenos son gases, hasta los
alquenos de 18 carbonos son líquidos, y los restantes son sólidos.
• La densidad, el punto de fusión y ebullición se incrementan a medida que aumenta el número de carbonos.
• No se disuelven en agua, pero sí en compuestos apolares como éter, benceno y cloroformo.
PROPIEDADES QUÍMICAS
• Son más reactivos que los alcanos, debido a la presencia del enlace doble.
Rosario Ybarra Miranda

Rosario Ybarra Miranda
RE
AC
CIO
NE
S• Combustión. Arden en presencia de oxígeno
con una llama más luminosa que los alcanos.• Adición. Resulta cuando uno o varios halógenos
o el hidrógeno se incorporan a la molécula de un alqueno al romperse el doble enlace.
• Polimerización. Unión de cientos de moléculas de un mismo alqueno para dar compuestos de cadenas más largas llamados polímeros.
polietileno• Se emplean en la fabricación de
plásticos, fibras sintéticas, envolturas, tales como el teflón, que es un tetrafluoretileno.

Rosario Ybarra Miranda

• También llamados acetilénicos o etínicos, por ser el etino el primer compuesto en su serie.
• Tienen un triple enlace entre sus dos carbonos, este tipo de enlace ocurre entre carbonos hibridizados sp.
• Su fórmula general es CnH2n–2 y se usa cuando presenta un solo triple enlace en la cadena, así un alquino de 30 carbonos es C30H28
• Para nombrar a los alquinos se usa la raíz del nombre de los alcanos, pero cambiando la terminación “ano” por “ino”.
CH3 - CH2 - C C - CH3
12345 Se enumera la cadena por el extremo más cercano al
enlace triple
Cadena principal: 5C, un enlace triple, pentino
Sustituyentes: no tiene
Nominación: 2- pentino
Rosario Ybarra Miranda

Rosario Ybarra Miranda
• En caso que la cadena presente dos o más enlaces triples, se denominan polialquinos, y para nombrarlos se usan los sufijos diino, triino, tetraino, etcétera.
• Se generan por reacción de termólisis a temperaturas elevadas y con enfriamiento muy rápido.
• También se obtiene de manera natural, un ejemplo es el caucho, que se extrae realizando incisiones en los troncos de los árboles del género ficus.
CH3 - CH2 - C C - C C - CH3
12345
Cadena principal: 7C , dos enlaces triples, heptadiino
Sustituyentes: no tiene
Nominación: 2,4 - heptadiino
67

Rosario Ybarra Miranda
PROPIEDADES FÍSICAS
• Los tres primeros alquinos son gases, a partir del butino (C4H6) hasta el hexadecino son líquidos, y los demás son sólidos.
• Son totalmente insolubles en agua, pero se disuelven bien en éter, tetracloruro de carbono y benceno.
PROPIEDADES QUÍMICAS
• Los alquinos arden como llama luminosa produciendo elevadas temperaturas. Un ejemplo es el acetileno (C2H2) que es un gas altamente inflamable, incoloro, que se usa para cortar y soldar metales.

Rosario Ybarra Miranda
HIDROCARBUROS
CÍCLICOS

Rosario Ybarra Miranda
Hidrocarburos nafténicos
• Cicloalcanos. Tienen sólo enlaces simples.
• Cicloalquenos. Tienen uno o más enlaces dobles.
• Cicloalquinos. Tienen uno o más enlaces triples.
• Los hidrocarburos cíclicos se nombran en forma similar que los lineales de igual número de carbonos, pero anteponiendo la palabra ciclo.
CH2
CH2H2C
H2C
ciclobutano
C
CH2H2C
C
CH2
ciclopentino

PROPIEDADES FÍSICAS
• Sus propiedades físicas y químicas son muy parecidas a sus homólogos acíclicos que tienen el mismo número de carbonos y tipos de enlace.
• Por ejemplo, los alcanos y los cicloalcanos tienen reactividad similar; y por calentamiento con hidrógeno, los cicloalcanos se convierten en alcanos.
CH2H2C
CH2
ciclopropano
+ H2
propano
CH3 - CH2 - CH3
• Sus puntos de fusión y ebullición varían en relación con el número de carbonos presentes en los anillos.
Rosario Ybarra Miranda

Rosario Ybarra Miranda
• Los terpenos. Son los principales componentes de las resinas y del aguarrás, las cuales son producidos por varias plantas ( de las que se extrae la trementina, el limoneno, el pineno, el mentol, el alcanfor, el eucalipto) y también por algunos insectos.
limonenoH3C
CH3
CH2
• El octanaje de la gasolina. Es el porcentaje de isooctano en una mezcla de heptano con isooctano. A mayor índice de octano de la gasolina corresponde un mejor funcionamiento del motor de combustión interna.

Rosario Ybarra Miranda
HIDROCARBUROS
AROMATICOS

Rosario Ybarra Miranda
• Son compuestos que poseen por lo menos un anillo bencénico o ciclo de seis átomos de carbono unido por enlaces dobles alternados y por enlaces simples.
• Esta característica del enlace confiere gran estabilidad y propiedades peculiares, como un olor fuerte característico.
Hid
roca
rbur
osar
omát
icos
• Mononucleares
• Polinucleares
• Monosustituidos
• Polisustituidos

Rosario Ybarra Miranda

Rosario Ybarra Miranda

Rosario Ybarra Miranda
DERIVADOS DEL BENCENO

Rosario Ybarra Miranda

• Los hidrocarburos aromáticos como el benceno, el tolueno y el xileno se usan como disolventes a nivel industrial y en el laboratorio.
Usos
• El naftaleno es un hidrocarburo aromático que se usa para combatir a las polillas.
Rosario Ybarra Miranda