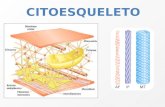
El citoesqueleto es un sistema subcelular formado por ... · Propiedades generales del...
-
Upload
trannguyet -
Category
Documents
-
view
224 -
download
0
Transcript of El citoesqueleto es un sistema subcelular formado por ... · Propiedades generales del...
Materila de Estudio
Libros
Alberts, Molecular Biology of the Cell
Lodish, Molecular Cell Biology
Artículos
Thomas D. Pollard, et al. Actin, a Central Player in Cell Shape and Movement. Science 326, 1208
(2009)
Thomas D. Pollard, et al. Cellular Motility Driven by Assembly and Disassembly of Actin Filaments.
Cell 112, 453–465 (2003)
Ronald D. Vale, et al. The Way Things Move: Looking Under the Hood of Molecular Motor Proteins.
Science 288, 88 (2000)
Andre P. Carter. Crystal clear insights into how the dynein motor moves. Journal of Cell Science 126,
705–713 (2013)
Hancock. Bidirectional cargo transport: moving beyond tug of war Bidirectional cargo transport: moving
beyond tug of war. Nature Reviews Molecular Cell Biology (2014)
iBioseminars
JULIE THERIOT: CELL MOTILITY AND THE CYTOSKELETON
Protein Polymers, Crawling Cells and Comet Tails: http://www.ibiology.org/ibioseminars/cell-biology/julie-
theriot-part-1.html
THOMAS POLLARD: CELL MOTILITY AND CYTOKINESIS
I. Mechanism of cell motility 1: http://www.ibiology.org/ibioseminars/thomas-pollard-part-1.html
II. Mechanism of cell motility 2: http://www.ibiology.org/ibioseminars/thomas-pollard-part-2.html
RON VALE: MOLECULAR MOTOR PROTEINS
Molecular Motor Proteins: http://www.ibiology.org/ibioseminars/cell-biology/ron-vale-part-1.html
Propiedades generales del citoesqueleto
Cumple una función
estructural en las células
Es esencial para el tráfico
intracelular y la motilidad
celular
Compuesto por filamentos
poliméricos proteicos
Los polímeros son de
naturaleza dinámica
Los polímeros ensamblan
estructuras de mayor orden y
complejidad
Es capaz de generar trabajo
mecánico
Diferentes estructuras formadas por el citoesqueleto. Microfilamentos
Alberts et al., MBC2002
microvellosidades
fibras de estrés
sarcómeros
Microfilamentos:• polímeros de actina de doble cadena• estructuras flexibles organizadas en arreglos lineales, redes bidimensionales y geles 3D• estructuras dinámicas (filopodios y lamelipodios) vs. estables (estereocilios)• estructuras transientes (anillo contráctil)
Diferentes estructuras formadas por el citoesqueleto. Microtúbulos
Hirokawa´s lab
vesícula
Moléculas Motoras convierten la
energía de la hidrólisis de ATP en
fuerza mecánica que puede
mover organelas a lo largo de los
filamenteos
Alberts et al., MBC2002MTs de interfase MTs del huso
axonemas
huso mitótico
célula en interfase
Microtúbulos:
• cilindros huecos formados por
tubulina
• rígidos y largos
• MTOC
Diferentes estructuras formadas por el citoesqueleto. Filamentos intermedios
Alberts et al., MBC2002
IFs de procesos gliales
IFs de células epiteliales
malla de laminas
Filamentos intermedios:
• fibras formadas por proteínas de filamentos intermedios
• resistencia mecánica
• pueden mantener juntas a las células epiteliales, ayudan en la extensión de axones
neuronales, o permiten formar uñas o pelo
Células motiles o migratorias requieren un citoesqueleto dinámico
VIDEO 10
La fagocitosis de bacterias depende del rearreglo del citoesqueleto de las células
fagocíticas especializadas (macrófagos y neutrófilos)
Los procesos de motilidad celular están conservados a través de protozoarios y eucariotas
Acanthamoeba y macrófagos capturan microorganismos mediante un proceso de
fagocitosis dependiente de la polimerización de actina que involucra la formación
de seudópodos y la motilidad celular
https://www.youtube.com/watch?v=qBIdfJEJMK0
Los filamentos del citoesqueleto son polímeros dinámicos
Alberts et al., MBC2002
El ensamblado repetitivo de subunidades
pequeñas resulta en la formación de
polímeros:
• actina microfilamentos
• tubulina microtúbulos
• varias subunidades filamentos
intermedios
Las subunidades se meantienen unidas
en el polímero mediante interacciones no
covalentes débiles
Proteínas accesorias asociadas al
citoesqueleto regulan la distribución
espacial y el comportamiento dinámico de
los filamentos
La polimerización/depolimerización de los
filamentos permite rápidos ajustes de la
estructura del citoesqueleto y de la forma
celular
La actina es una proteína globular de 375 aminoácidos (43 kDa). Sitios de unión en los
monómeros de actina (G-actina) median la interacción cabeza-cola con otros dos monómeros
para polimerizar filamentos de actina (F-actina). Los filamentos están formados por dos
protofilamentos que se mantienen unidos a travás de contactos laterales. La orientación
constante de los monómeros en los polímeros determina su polaridad estructural [extremos
(+) y (-)].
Estructura cristalina del
monómero de actina
(difracción de rayos X)
Filamento de actina
(microscopía electrónica)
Estructura de la actina globular y filamentosa
Estudios in vitro revelan las propiedades dinámicas de los polímeros
Preparaciones de actina soluble purificadas de
músculo esquelético polimerizan espontáneamente
a concentraciones fisiológicas de iones.
La cinética de polimerización de actina puede ser
monitoreada in vitro por viscosimetría,
sedimentación, espectroscopía de fluorescencia o
microscopía.
vis
cosid
ad
tiempo
sin Mg2+
sin Ca2+
La fluorescencia del polímero de actina
marcada con pireno es 7-10 veces más
grande que la del monómero y la señal es
proporcional a la concentración en masa del
polímero.
tiempo
fluore
scencia
Espectroscopía de fluorescencia
Viscosimetría
Cinética de polimerización de actina
Durante una fase inicial se forman pequeños núcleos (fase de nucleación) y luego la polimerización
incrementa linealmente en función del tiempo (fase de elongación) hasta alcanzar un estado estacionario
donde la masa del polímero permanece constante. La concentración de monómeros en el estado estacionario
es la concentración crítica o Cc; concentraciones mayores o menores a la Cc inducen el aumento o
disminución de la masa del polímero, respectivamente.
VIDEO 1
Lodish et al MCB2004
nucleación elongación estado estacionario
La tasa de adición de monómeros está dada
por la constante de velocidad kon (M-1 sec-1) y la
tasa de pérdida por koff (sec-1). El número de
monómeros que se adicionan al polímero por
segundo es proporcional a la concentración de
subunidades libres (konC), pero las
subunidades dejan el extremo del polímero a
una velocidad constante (koff) que no depende
de la concentración.
Concentración crítica
A medida que el polímero crece, C cae
hasta alcanzar un valor constante,
concentración crítica (Cc). En este
equilibrio,
konC = koff
por lo tanto
En un extremo del polímero, a la Cc la
velocidad de adición es igual a la
velocidad de depolimerización y no hay
elongación neta.
Cc =koff
kon
=1
K
+
polímero (con n subunidades) subunidad polímero (con n + 1 subunidades)
kon
koff
Constantes de velocidad de adición y pérdida de monómeros
La reacción acrosomal del esperma de cangrejo extiende fascícuos de actina que sirven de núcleos para la reacción de polimerización in vitro
pro
ce
so
acro
so
mal
(fascíc
ulo
sd
e F
-actin
a)
Microscopía de campo claro de
esperma del cangrejo Limulus no
reactivo (1a) y luego de la
reacción acrosomal (1b)
Los filamentos de actina son polímeros polares
La polaridad de los microfilamentos de actina puede determinarse mediante
microscopía electrónica después de incubar los polímeros con fragmentos S1 de
miosina.
(+)(-)
Microscopía electrónica de la polimerización
de filamentos de actina en los extremos (+) y
(-) de un proceso acrosomal de Limulus. Las
constantes de velocidad se calculan a partir
de la medida de la longitud de los fascículos
de filamentos de actina.lo
ngitud
(μm
)
tiempo
(+)
(-)
Las constantes de velocidad de adición y pérdida de monómerosson diferentes en los extemos (+) y (-) del polímero
Pollard (1986) JCB 103: 2747-2754
La tasa de adición (kon) de subunidades en forma T es mucho más ràpida en el extremo (+) (12
M-1 s-1) que en el extremo (-) (1.3 M-1 s-1), mientras que la tasa de disociación es similar en los
dos extremos. Luego de la adición de subunidades ocurre la hidrólisis rápida del nucleótido
trifosfato y la disociación lenta de Pi. El cambio conformacional asociado a la hidrólisis es
responsable de la diferencia en las tasas de asociación y disociación de los dos extremos.
Las constantes de velocidad de adición y pérdida de monómerosson diferentes en los extemos (+) y (-) del polímero
Pollard (2009) Science
La actina es una enzima con actividad ATPasa
Cuando el filamento crece, en el extremo (+) la elongación es más rápida que la hidrólisis. Las
subunidades del extremo (+) se encuentran en forma T. La hidrólisis es más rápida que la
elongación en el extremo (-) y las subunidades terminales están en forma D.
Si se considera uno solo de los extemos, el balance entre la tasa de adición y disociación se
alcanza a la Cc=koff /kon. Cc+ es menor que Cc
-. En el estado estacionario la concentración de
subunidades libres será intermedia entre Cc+ y Cc
-.
Cc(T) es menor que Cc(D)Para C > Cc(T) pero < Cc(D)
se observa treadmilling
Alberts et al., MBC2002
En el estado de treadmilling hay movimiento hacia el extremo (+) debido al flujo de subunidades a través del polímero
El treadmilling es un estado estacionario de los polímeros con adición neta de
subunidades en la forma T en el extremo (+) y pérdida neta de subunidades en la
forma D en el extremo (-). La longitud del polímero permanece invariable.
Lodish et al MCB2004
La polimerización de actina es capaz de generar fuerza mecánica
tiempo
dis
tancia
fuerz
a
La fuerza que genera la elongación de un fascículo de
filamentos de actina puede medirse directamente usando
una trampa óptica. La trampa óptica sostiene una
microesfera donde se encuentran inmobilizados acrosomas
de Limulus próxima a una barrera rígida. Cuando ocurre la
elongación de los filamentos de actina, la distancia que se
desplaza la microesfera es proporcinal a la fuerza. La
elongación puede impedirse cuando se aplica una furza del
orden del pN.
Trampas ópticas
Footer (2007) PNAS
Los objetos dieléctricos son atraídos al centro
del rayo. La fuerza aplicada sobre el objeto es
directamente proporcional a su desplazamiento
desde el centro de la trampa
Proteínas accesorias de unión a actina
La nucleación espontánea de filamentos es desfavorable debido a la inestabilidad de los
oligómeros de actina. La elongación de filamentos es favorable, especialmente en el extremo
(+). La célula emplea proteínas accesorias para (i) mantener un pool de actina no polimerizada
mediante proteínas de unión a los monómeros de actina, (ii) promover la nucleación (forminas
y Arp2/3), (iii) restringir el largo de los filamentos, (iv) regular el ensamblado y el recilado de los
filamentos, y (v) entrecruzar filamentos en fascículos o redes.
Pollard (2009) Science
El complejo Arp2/3 comprende siete subunidades de Actin RelatedProteins (ARPs)
Arp2/3 se aisló de la ameba Acanthamoeba castellanii como un ligando de profilina, una
proteína de unión a actina. Luego se identificó asociado a estructuras ricas en actina de
levaduras. Arp2/3 purifica como un complejo de siete polipéptidos en proporciones
estequiométricas en una columna de cromatografía de afinidad. Las subunidades de mayor
peso molecular son actin related proteins.
La estructura cristalina de Arp2 y Arp3 revela que la cara superior de ambas es muy similar el extremo (+)
de la molécula de actina. Sin embargo las diferencias en los lados y en la cara opuesta impiden que
estas proteínas formen filamentos por sí mismas o se ensamblen en filamentos junto con actina.
SD
S-P
AG
E
Arp3
Arp2
Machesky (1994) JCB
Actin Related Proteins (ARPs) se comportan como agentes nucleantes de la polimerización de filamentos de actina
ARP2/3 nuclea el crecimiento de los filamentos de actina a partir del extremo menos,
permitiendo la elongación rápida de los filamentos por el extremo más.
Reconstrucción 3D de imágenes de
microscopía electrónica de la ramificación de
filamentos de actina mediada por el complejo
Arp2/3 de Acanthamoeba. Las reconstrucción
de las ramificaciones de preparaciones de
bovino (F) y levadura (G) son muy similares y
presentan densidades electrónicas conectando
los dos filamentos.
Alberts et al., MCB2002
Rouiller (2008) JCB 180(5):887-895
Rouiller (2008) JCB 180(5):887-895
Arp2 y Arp3 son las primeras dos subunidades en el nuevo filamento
La reconstrucción de la ramificación muestra que el complejo Arp2/3
interacciona con el filamento madre. La formación de la ramificación resulta en
cambios conformacionales en el filamento madre y en el complejo Arp2/3. Arp2
(rojo) y Arp3 (naranja) se reorganizan como un dímero que sirve de molde
para la elongación de un nuevo filamento.
(-)
(+)
vista en estéreo
La unión de un factor activador al
complejo ARP provoca un cambio
conformacional de Arp2 y Arp3. El
complejo ARP activado se asemeja al
extremo (+) de un filamento de actina
y las subunidades se ensamblan en
esta estrucutra.
Factores promotores de la nucleación de la familia WASp de proteínas activan al complejo ARP2/3
tiempo
fluore
scencia
actina
actina + Wasp
actina
Arp2/3
Wasp
actina + Arp2/3
La combinación de Wasp y el complejo
Arp2/3 promueve la polimerización
espontánea de monómeros de actina
(Machesky, 1999).
Lodish et al MCB2004
La microscopía de reflexión total
interna de fluorescencia permite
observar la polimerización de actina
marcada con rodamina en tiempo real.
El complejo Arp2/3 activado se une a
un filamento de actina preformado
para nuclear filamentos ramificados a
los lados del filamento madre.
VIDEOS 2 y 3
El complejo Arp2/3 media la formación de filamentos ramificados
Las ramificaciones del
filamento madre que nuclea el
complejo Arp2/3 emanan a un
ángulo de 70º. Sucesivas
rondas de nucleación resultan
en una red ramificada de
filamentos de actina.
Amann (2001) PNAS
Las forminas son factores de nucleación de actina que aceleran la elongación de filamentos de actina in vitro
Las forminas forman un complejo
dimérico que puede nuclear la formación
de un nuevo filamento de actina y quedar
asociado con el extremo más mientras
ocurre la elongación. El dímero se
mantine unido a una de las dos
subunidades de actina expuestas en el
extremo más permitiendo el ensamblado
nuevas subunidades.
Lodish et al MCB2004
VIDEO 4
FH2
FH1
Las forminas posibilitan la elongación de filamentos no ramificados.
actinaprofilina
Higgs (2005) TiBS
Okada (2010) JCB
Las forminas + profilina aumentan
la tasa de elongación en el
extremo (+). Los dominios FH2
forman un dímero que rodean el
extremo (+) de un filamento. Los
dominios FH1 contienen sitios de
unión a profilina. Profilina-actina se
ensambla en el dominio FH1,
luego el monómero de actina se
transfiere al extremo (+)
liberándose de profilina
Microscopía TIRF de la polimerización de
actina en presencia de mDia y profilina.
Organización de la formina mDia
thimosyn profilin
Timosina y profilina se unen a los monómeros de actina libres paracontrolar la elongación de filamentos in vivo
Timosina bloquea todas las reacciones de polimerización (nucleación y elongación de los
extremos (+) y (-)). Profilina inhibe la nucleación y la elongaión del extremo (-), pero no la
elongación del extremo (+).
Proteínas de capping se unen al extemo más de filamentos y bloquean la adición y la pérdida de subunidades en ese extremo
En una reacción de polimerización de actina in vitro, el agregado de proteínas
de capping sólo permite la adición y la pérdida de subunidades por el extremo
menos disminuyendo la velocidad de elongación por encima de la Cc y la
velocidad a la que el filamento se acorta por debajo de la Cc.
La unión de cofilina a los filamentos de actina provoca
una alteración en el giro normal del filamento, los
contactos entre subunidades de actina se debilitan y
en algunos casos se rompen.
ADF (actin depolymerizing factor)/cofilina induce la fragmentación de filamentos de actina
microscopía electrónica
+ c
ofilin
a
Andrianantoandro (2006) Mol Cell
McGough (1997) JCB
VIDEO mmc3
mic
roscopía
TIR
F
Cofilina aumenta la tasa de elongación en el
extremo (+), no en el extremo (-) de los
filamentos de actina. Cofilina aumenta la tasa
de depolimerización desde el extremo (-), no
desde el extremo (+). El resultado neto es un
aumento en la tasa de treadmilling.
Cofilina promueve el reciclado de monómeros de actina
tiempo
Abs 3
10nm
Polimerización in vitro
Turbidimetría
actina
actina
+ cofilina
El agregado de cofilina
aumenta la Ccrit
Ccrit
Carlier (1997) JCB
Cofilina se une a la forma D de actina en los filamentos
La afinidad de cofilina por la forma
D es dos veces más grande que
por la forma T de actina en los
filamentos. Como la tasa de
elongación en el extremo (+) es
más grande que la tasa de
hidrólisis de ATP, cofilina induce la
fragmentación de filamentos a a
medida que “envejecen”. Los
extremos menos que se generan
por acción de cofilina se acortan
rápidamente para promover el
reciclado de monómeros de actina.
Profilina sirve de buffer de los
monómeros de ADP-actina e
intercambia ADP por ATP. Los
monómeros de ATP-actina unidos
a profilina se adicionan al extremo
más o son secuestrados por
timosinaLodish et al MCB2004
Modelo de nucleación dendrítica en el frente de avance de células migratorias
Factores promotores de la
nucleación asocian al
complejo Arp2/3 con un
monómero de actina en el
lado de un filamento para
nuclear un filamento
ramificado. El extremo (+)
del filamento crece hasta la
asociación de una proteína
de cap que termina la
elongación. La hidrólisis del
nucleótido unido a las
subunidades provoca el
envejecimiento del
filamento. Cofilina fragmenta
los filamentos promoviendo
la disociación de la forma D
de actina desde el extremo
(-). Profilina recicla las
subunidades de actina a la
forma T que quedan
disponibles para elongar
extremos (+).
Pollard (2009) Science
Las proteínas involucradas en la migración celular son las mismasque las involucradas en la endocitosis en levaduras
La endocitosis en levaduras constituye un
sistema que permite estudiar con
resolución espacial y temporal la hipótesis
de nucleación dendrítica de actina. Los
parches de actina son muy pequeños
comparados con el frente de avance de
una célula migratoria. En estos parches de
actina los filamentos se ensamblan de
novo, proveen la fuerza para formar e
internalizar una vesícula endocítica desde
la membrnana plasmática y se
desensamblan en un proceso autolimitado.
Wsp1 ARPC5
Sirotkin (2005) JCB
VIDEO V2
Pollard (2009) Science
En las imágenes de
microscopía de fluorescencia,
la intensidad es directamente
proporcional al número de
moléculas en un área definida,
lo que permite seguir la
acumulación y desaparición de
proteínas en los sitios de
endocitosis (“parches de
actina”). La primer proteína que
se detecta es clatrina, luego
aparecen las proteínas
adaptadoras para asociarse
1:1 con clatrina. El factor
promotor de la nucleación
Wsp1 (~200) precede a al
complejo ARP2/3 (~300) justo
antes del ensamblado de
actina en una red de filamentos
entecruzados (~7000 actinas,
~200 proteínas de capping, y
900 proteínas de
entrecruzamiento).
Sirotkin (2010) MBoC
El modelo de nucleación dendrítica explica el ensamblado de redesdendríticas en los sitios de endocitosis
El estado de polimerización puede afectarse con drogasque unen monómeros y filamentos de actina
Algunas drogas se unen y secuestran a los monómeros no ensamblados,
provocando la depolimerización de los filamentos. Otras drogas se unen a los
filamentos y los estabilizan. El efecto de las drogas revela el rápido y continuo
intercambio de subunidades en los polímeros.
La faloidina es una toxina del
hongo Amanita phalloides.
Debido a su unión selectiva a
microfilamentos, derivados de
faloidina conjugados a
fluoróforos se usan en
microscopía para visualizar F-
actina en células fijadas.
ACTIN-SPECIFIC DRUGS
Phalloidin binds and stabilizes filaments
Cytochalasin caps filament plus ends
Swinholide severs filaments
Latrunculin binds subunits and prevents their polymerization
fibroblasto
DAPI
faloidina