Desacopladores de La Fosforilacion
Click here to load reader
-
Upload
jackelyn-rimarachin-casique -
Category
Documents
-
view
284 -
download
30
description
Transcript of Desacopladores de La Fosforilacion

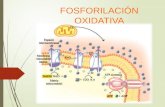
Desacopladores de la fosforilacion
Los agentes desacopladores son un grupo de sustancias que incluye a los fenoles sustituidos (pentaclorofenol y dinitrofenol), hormonas tiroideas a dosis tóxicas, fenilhidrazonas de cianuro de carbonilo, dicumarol, ácidos grasos de cadena larga y algunos antibióticos (como valinomincina y gramicidina), que tienen la propiedad de hacer permeable la membrana mitocondrial a los protones disipando el potencial electroquímico de protones y el gradiente eléctrico consecuente; de esta manera, en las mitocondrias desacopladas la energía liberada por el transporte de electrones se disipa en forma de calor.
Inhibidores de la respiraciónLos inhibidores de la respiración son sustancias que inhiben la respiración celular.
Tipos de Inhibidores
Inhibidores de la cadena respiratoria Inhibidores de la fosforilación oxidativa Desacopladores de la fosforilación oxidativa
Los inhibidores de la respiraciónEste tipo de inhibidores reciben este nombre porque su principal función es el inhibir el transporte de electrones en la cadena de la respiración. Los inhibidores del transporte de electrones más comúnmente usados pueden reunirse en tres grupos principales según el sitio de la cadena respiratoria donde actúan:
1. Sobre la NADH-deshidrogenasa, bloqueando la transferencia de electrones entre la flavina y la ubiquinona. (Inhibidores del sitio I) Barbitúricos , como el amobarbital Piericidina A (antibiótico) Rotenona (insecticida)
2. Actúa bloqueando la transferencia de electrones entre el citocromo b y el citocromo c1. (inhibidores de sitio III) Antimicina
3. Actúan sobre el Hemo a3 de la citocromooxidasa impidiendo su interacción con el oxígeno (inhibidores de sitio IV) Cianuro Monóxido de carbono H 2S
Inhibición de la fosforilaciónActúan en el complejo enzimático (ATPsintasa) que cataliza la síntesis de ATP, bloquean el paso en el cual el ADP se une al fosfato impidiendo que la energía del potencial electroquímico llegue al sistema fosforilante.

Oligomicina Atractilósido (inhibe el transportador que introduce ADP a la mitocondria)
DesacopladoresLa acción de estos consiste en disociar la oxidación en la cadena respiratoria, de la fosforilación. Bloquean la síntesis de ATP, al tiempo que permite que continúe el transporte electrónico a lo largo de la cadena respiratoria hasta el O2.
Son ácidos débiles solubles en lípidos. Un desacoplante muy usado es el 2,4-dinitrofenol (DNP) el cual actúa de aproximándose a
la membrana interna y protonandose, debido al pH más bajo existente en esta zona, esta protonación aumenta la hidrofobicidad del DNP, lo cual permite que difunda en la membrana y que la atraviese por la acción de masa. Una vez dentro de la matriz, el pH más alto hace que el hidroxilo fenólico desprotone. Así pues, el desacoplador tiene el efecto de transporte de H+ de vuelta hacia la matriz, evitando el canal protónico Fo y, por tanto, sin síntesis de ATP. Ya que la entrada de los H+ en la matriz, a través del canal Fo proporciona la energía necesaria para impulsar la síntesis de ATP, Otros desacopladores son:
Dinitrocresol Pentaclorofenol CCCP (m-clorocarbonilcianuro fenilhidrazona), 100 veces más activa que el primero.
Desacopladores e inhibidores.
El uso de inhibidores de la cadena ha permitido trazar el paso de los electrones a través de la cadena y determinar el punto de entrada de diversos sustratos. La velocidad a la cual el oxígeno es consumido por una suspensión de mitocondrias es una medida del funcionamiento de la cadena de transporte de electrones. La velocidad puede ser medida mediante un electrodo de oxígeno.
Gran parte del conocimiento de la función mitocondrial ha resultado de estudios con compuestos tóxicos. Inhibidores específicos se han usado para distinguir el sistema de transporte de electrones del sistema de fosforilación oxidativa, y ha ayudado a definir la secuencia de los transportadores redox en la cadena. Si la cadena se bloquea en un punto, todos los transportadores anteriores quedan más reducidos, y los posteriores más oxidados.
Hay seis tipos de venenos que afectan la función mitocondrial:
1. Inhibidores de la cadena que bloquean la cadena respiratoria.
La rotenona, toxina de una planta, utilizada por indios amazónicos como veneno, también ha sido usada como insecticida.

Actúa a inhibiendo el complejo I. Inhibe la reoxidación del NADH, no afecta la del FADH2. Inhibe la oxidación del malato, que es dependiente del NAD+, no así la del succinato. El succinato entra en el segundo punto de entrada a la cadena, posterior al del NAD+.
El amital (barbitúrico) inhibe al complejo I, afecta las oxidaciones dependientes del NAD+.
La antimicina A (Antibiótico).
Actúa a inhibiendo el complejo III. Inhibe la reoxidación del NADH y del FADH2.
El cianuro bloquea el paso de electrones del citocromo a3 al oxígeno.
Estos inhibidores detienen el paso de electrones de modo que no hay bombeo de protones. Sin gradiente de protones, no hay síntesis de ATP.
2. Inhibidores de la fosforilación oxidativa, venenos que inhiben la ATP-sintasa.
La oligomicina, un antibiótico producido por Streptomyces, inhibe a la ATPasa al unirse a la subunidad Fo e interferir en el transporte de H+ a través de Fo, inhibe por lo tanto la síntesis de ATP.
Diciclohexilcarbodiimida (DCCD), un reactivo soluble en lípidos, también inhibe el transporte de protones por Fo al reaccionar con un residuo de glutámico en una de las subunidades de Fo de mamíferos.

En estas condiciones el gradiente de protones que se produce es mayor que lo normal, sin embargo la energía potencial de éste no puede ser utilizada para producir ATP.
3. Venenos que hacen permeable la membrana mitocondrial interna a los protones. Estos agentes eliminan la relación obligada entre la cadena respiratoria y la fosforilación oxidativa que se observa en mitocondria intacto.
Estos venenos, como el 2,4 dinitrofenol (DNP), el carbonilcianuro-p-trifluorometoxi-hidrazona (FCCP) y el carbonilcianuro-m-clorofenilhidrazona (CCCP) desacoplan la fosforilación oxidativa de la cadena respiratoria, se conocen como agentes desacopladores.
Son compuestos liposolubles y ácidos débiles. Las formas disociadas presentan carga negativa altamente deslocalizada, de modo que el campo eléctrico de los aniones es muy débil, ello permite que difundan libremente a través de un medio no polar como las membranas fosfolipídicas. Este comportamiento no es usual, la gran mayoría de iones con carga son excluidos de un ambiente no polar.
La forma protonada, sin carga eléctrica de estos compuestos, pasa a través de la membrana interna mitocondrial intacta, descargando así el gradiente de pH. En la matriz, a pH más bajo, el ácido débil se disocia, la forma disociada pasa la membrana interna, destruyendo el potencial de membrana. Este proceso se puede repetir, de modo que una pequeña cantidad del agente desacoplante puede catalizar el paso de una cantidad enorme de protones y hacer un corto circuito en la cadena respiratoria.
En resumen, permitiendo el paso de protones a través de la membrana, se disipa el gradiente de protones, no hay bombeo de protones a través de la ATP-sintasa con producción de ATP.
Los agentes desacoplantes son todos sintéticos, sin embargo en el mitocondria del tejido adiposo pardo una proteína desacopladora (termogenina) participa en el delicado control de la termogénesis.

4. Inhibidores de transporte (atractalósido) que previenen ya sea la salida del ATP o la entrada de material combustible a través de la membrana mitocondrial interna.
5. Ionósforos (valinomicina, nigericina) que permiten el paso a través de la membrana a compuestos que normalmente están impedidos.
6. Inhibidores del ciclo de Krebs (arsenito) que bloquean una o más enzimas del ciclo de Krebs.
La producción de ATP aeróbica es más eficiente que la producción anaeróbica.
En 1861, Louis Pasteur observó que en levadura expuesta a condiciones aeróbicas, el consumo de glucosa y la producción de etanol decae precipitadamente (Efecto Pasteur).
Glicólisis anaeróbica:
C6H12O6 + 2ADP + 2Pi 2 lactato + 2H+ + 2ATP
Metabolismo aeróbico de la glucosa:
C6H12O6 + 38ADP + 38Pi 6 O2 6 CO2 + 44H20 + 38ATP
El metabolismo aeróbico es más eficiente que la glicólisis anaeróbica en lo que se refiere a producción de ATP.
Sin embargo, como la concentración de enzimas de la glicólisis es alta, de modo que si no están inhibidas, el ATP puede producirse más rápido que a través de la fosforilación oxidativa.
Por otra parte, el cálculo tradicional de 36 ATP o de 38 ATP, según funcione la lanzadera del glicerofosfato o del malato respectivamente, es obsoleto. Mediciones recientes estiman 30 ATP por glucosa totalmente metabolizada.

MATERIALES DEL EXPERIMENTO 1
Agua destilada
Porque el agua destilada carece de minerales y de cualquier tipo de microorganismo, con lo que al trabajar con ella se evita que las sustancias que pudiera poseer intervengan en los resultados de los experimentos o tareas. De esta forma todas las muestras son exactamente iguales
Cofactor
Definición: Un cofactor es una molécula pequeña necesaria para la actividad de muchas enzimas.
Los cofactores son iones metálicos o moléculas orgánicas que participan con las enzimas en la realización de una actividad enzimática. A los cofactores de naturaleza orgánica se le conocen como coenzimas. Algunos de los iones metálicos más comunes que actúan como cofactores son el manganeso, el magnesio, el molibdeno, el cobalto, el zinc, el hierro, el níquel, el potasio o el cobre.
Una de las principales funciones de los cofactores es sufrir las transformaciones químicas necesarias (oxidación y reducción entre otras) para llevar a cabo la catálisis enzimática. De este modo la enzima queda intacta pudiendo llevar a cabo la catálisis de nuevas reacciones simplemente reemplazando el cofactor modificado por otro nuevo o devolviendo el cofactor a su estado inicial.
A los cofactores que se unen fuertemente a la enzima se les conoce como grupos prostéticos.
Suero Fisiológico (NaCl)
El suero fisiológico o solución fisiológica es una disolución acuosa de sustancias compatibles con los organismos vivos debido a sus características definidas de osmoticidad, pH y fuerza iónica. Está compuesto de agua, electrolitos y, a veces, distintas sustancias, como por ejemplo la glucosa, fuente de carbono y energía para el organismo, y de algunos polisacáridos expansores.
¿Qué es y cómo se usa?quÉ Es
qué Es Suero Fisiológico Y Para Qué Se Utilizasuero Fisiológico Es Una Solución De Cloruro Sódico Y Agua. El Cloruro Sódico Es Una Sustancia Química (comúnmente Llamada Sal) Que Se Encuentra En La Sangre. suero Fisiológico Se Usa Para Tratar:
o Una Pérdida De Agua Del Cuerpo (deshidratación)
o Una Pérdida De Sal Del Cuerpo (depleción De Sodio) Las Situaciones Que Pueden
Causar La Pérdida De Agua Y De Cloruro Sódico Incluyen:
o Cuando No Puede Comer O Beber, Debido A Una Enfermedad O A Tras Una
Intervención Quirúrgica
o Sudor Excesivo Causado Por Fiebre Alta

o Perdida Extensiva De Piel, Como Ocurre En Quemaduras Graves
Suero Fisiológico También Puede Ser Utilizado Para Suministrar O Diluir Otros Medicamentos Para Perfusión
¿Qué debe tener en cuenta antes de usarlo?antes De Usar Suero Fisiológico
antes De Usar Suero Fisiológicono Se Le Deberá Administrar Suero Fisiológico Si Sufre Alguna De Las Siguientes Situaciones Clínicas
o Si Su Sangre Contiene Niveles Altos De Cloruros Superiores A Los Normales
(hipercloremia)
o Si Su Sangre Contiene Niveles Altos De Sodio Superiores A Los Normales
(hipernatremia)
Si Se Ha Añadido Otro Medicamento A Suero Fisiológico, Deberá Consultarse Su Prospecto Para Determinar Si Puede O No Recibir La Solución. tenga Especial Cuidado Con Suero Fisiológico: informe A Su Médico Si Tiene O Ha Tenido Alguna De Las Siguientes Situaciones Clínicas:
o Cualquier Tipo De Enfermedad O Función Empobrecida Del Corazón
o Función Empobrecida Del Riñón
o Tensión Arterial Elevada (hipertensión)
o Acumulación De Líquidos Bajo La Piel, Particularmente Bajo Los Tobillos (edema
Periférico)
o Acumulación De Líquidos En El Pulmón (edema Pulmonar)
o Presión De La Sangre Alta Durante El Embarazo (pre-eclampsia)
o Aumento De La Producción De La Hormona Aldosterona (aldosteronismo)
o Cualquier Otra Condición Asociada A La Retención De Sodio (cuando El Organismo
Retiene Demasiado Sodio), Tales Como El Tratamiento Con Esteroides (ver También
Uso De Otros Medicamentos)
Cuando Le Estén Administrando Esta Solución, Su Médico Podrá Tomar Muestras De Sangre Y Orina Para Controlar:
o La Cantidad De Líquido De Su Organismo

o Sus Signos Vitales
o La Cantidad De Sustancias Químicas Como Sodio Y Potasio En Su Cuerpo (sus
Electrolitos Plasmáticos)
Su Médico Tendrá En Cuenta Si Está Recibiendo Nutrición Parenteral (nutrición Dada Por Perfusión En Vena).durante El Tratamiento Prolongado Con Suero Fisiológico Usted Puede Necesitar Que Le Den Nutrición Extra. uso De Otros Medicamentos informe A Su Médico O Farmacéutico Si Está Utilizando O Ha Utilizado Recientemente Otros Medicamentos, Incluso Los Adquiridos Sin Receta. uso De Suero Fisiológico Con Los Alimentos Y Bebidas pregunte A Su Médico Acerca De Lo Que Puede Comer O Beber. embarazo Y Lactancia consulte A Su Médico O Farmacéutico Antes De Utilizar Cualquier Medicamento. Informe A Su Médico Si Esta Embarazada O En Lactancia. Usted Puede Recibir Suero Fisiológico En Ambos Casos. La Cantidad Que Le Administren Será Cuidadosamente Controlada Por Su Médico. sin Embargo, Si Se Añadiese Otro Medicamento A La Solución Para Perfusión Durante El Embarazo O La Lactancia, Usted Deberá:
o Preguntar A Su Médico
o Leer El Prospecto Del Medicamento Que Se Le Vaya A Añadir
conducción Y Uso De Máquinas suero Fisiológico No Afecta A Su Capacidad Para Conducir O Usar Maquinaria.
¿Cómo se utiliza?cómo Usar Suero Fisiológico
cómo Usar Suero Fisiológicosuero Fisiológico Le Será Administrado Por Un Médico O Una Enfermera. Su Médico Decidirá Que Cantidad Necesita Y Cuando Le Será Administrada, Lo Que Dependerá De Su Edad, Peso, Condición, La Causa De Su Tratamiento Y Si La Perfusión Se Utiliza O No Para Administrarle O Diluir Otro Medicamento. la Cantidad Que Reciba También Puede Afectar A Otros Tratamientos Que Esté Recibiendo. no Debe Recibir Suero Fisiológico Si Hay Partículas Flotando En La Solución O Si El Envase Está Dañado De Algún Modo. generalmente Suero Fisiológico Se Le Administrará A Través De Un Tubo De Plástico Conectado Mediante Una Aguja A Una Vena, Casi Siempre De Su Brazo. No Obstante, Su Médico Podría Utilizar Otro Método Para Administrarle El Medicamento

cuando Se Le Administre Suero Fisiológico Su Médico Podrá Realizar Análisis De Su Sangre Para Controlar Sus Niveles Sanguíneos De:
o Electrolitos (como Sodio O Cloruros) Y Otras Sustancias Químicas Que Normalmente
Están En La Sangre Como La Creatinina (un Producto De Degradación De Los
Músculos)
Cualquier Resto No Utilizado De La Solución Deberá Ser Desechado. Usted No Debe Recibir Suero Fisiológico De Una Bolsa Que Haya Sido Utilizada Parcialmente. si Recibe Más Suero Fisiológico Del Que Debiera si Le Administran Demasiado Suero Fisiológico (sobredosificación), Pueden Producirse Los Siguientes Síntomas:
o Nauseas (malestar)
o Diarrea (perdida De Heces)
o Sed
o Ojos Secos
o Sudoración
o Fiebre
o Aumento De La Presión De La Sangre (hipertensión)
o Dolor De Cabeza
o Irritabilidad
o Convulsiones
o Vómitos
o Calambres Estomacales
o Boca Seca
o Ritmo Rápido Del Corazón (taquicardia)
o Fallo Del Riñón (fallo Renal)
o Mareo
o Inquietud
o Debilidad
o Tics Musculares Y Entumecimiento Acumulación De Líquidos En Los Pulmones
Haciendo Difícil La Respiración (edema Pulmonar)

o Acumulación De Líquidos Bajo La Piel, Particularmente Bajo Los Tobillos (edema
Periférico)
o Respiración Entrecortada (parada Respiratoria)
o Acidificación De La Sangre (acidosis) Que Conduce A Cansancio, Confusión, Letargia
Y Aumento Del Ritmo Respiratorio.
Si Tiene Alguno De Estos Síntomas, Deberá Informar A Su Médico Inmediatamente. Su Perfusión Se Detendrá Y Se Le Tratará Dependiendo De Los Síntomas. si Se Ha Adicionado Otro Medicamento A Suero Fisiológico Antes De Que La Sobredosificación Tuviese Lugar, Podría Ser Que Ese Medicamento También Causase Síntomas. Debe Leer El Prospecto Del Medicamento Añadido Para Ver La Lista De Estos Posibles Síntomas. interrumpción De La Perfusión De Suero Fisiológico su Médico Decidirá Cuando Frenar La Administración De La Perfusión si Tiene Cualquier Otra Duda Sobre El Uso De Este Producto, Pregunte A Su Médico.
¿Cuáles son sus posibles efectos secundarios?posibles Efectos Adversos
posibles Efectos Adversosal Igual Que Todos Los Medicamentos, Suero Fisiológico Puede Producir Efectos Adversos, Aunque No Todas Las Personas Los Sufran. los Efectos Adversos Que Pueden Ocurrir Debido A La Técnica De Administración Incluyen:
o Fiebre (respuesta Febril)
o Infección En El Punto De Inyección
o Dolor Local O Reacción (enrojecimiento O Hinchazón En El Sitio De Administración)
o Irritación E Inflamación De La Vena En La Cual La Solución Es Perfundida (flebitis).
Esto Puede Ocasionar Enrojecimiento, Dolor O Quemazón E Hinchazón A Los Largo
De La Vena En La Cual Se Ha Perfundido La Solución.
o Formación De Coágulos De Sangre (trombosis Venosa), Generalmente En Las
Piernas, Que Causan Dolor, Hinchazón O Enrojecimiento.
o Escape De La Solución Dentro De Los Tejidos Vecinos De La Vena (extravasación).
Esto Puede Dañar Los Tejidos Causando Cicatrices
o Un Exceso De Líquido En Los Vasos Sanguíneos (hipervolemia)

Enzima
Las enzimas son proteinas globulares que actuan como biocatalizadores, es decir, aceleran las reacciones quimicas en los seres vivos sin modificarse. Al acelerarse las reacciones, disminuye la energia de activacion y tiempo de reaccion.
PD: Se llama sustrato a toda molecula sobre la que actua una enzima. A la energia que se necesita para transformar un sustrato en producto se llama energia de activacion y el tiempo que se gasta en el cambio se denomina tiempo de reaccion. Bueno espero haber colaborado en algo. Mucha suerte!
BUFFER FOFATO
(en diapo)
FUNCIONES del NÚCLEO
La principal es la replicación y transcripción de los ácidos nucleicos. Almacena la información genética, pasándola a las células hijas en el momento de la división celular. Una parte de la información genética se encuentra almacenada en el ADN de cloroplastos (5-10%) y mitocondrias (2-5%).El núcleo controla todas las actividades celulares, ejerciendo su control al determinar quéproteínas enzimáticas deben ser producidas por la célula y en qué momento. El control se ejerce a través del ARN mensajero. El ARN mensajero, que se sintetiza por transcripción del ADN, lleva la información al ARN ribosómico, en el citoplasma, donde tiene lugar la síntesis de proteínas enzimáticas que controlan los procesos metabólicos (Fig.8.8).

3.6.3. Función mitocondrial. La principal función de las mitocondrias es generar energía para mantener la actividad celular mediante procesos de respiración aerobia. Los nutrientes se escinden en el citoplasma celular para formar ácido pirúvico que penetra en la mitocondria. En una serie de reacciones, parte de las cuales siguen el llamado ciclo de Krebs o del ácido cítrico, el ácido pirúvico reacciona con agua para producir dióxido de
carbono y diez átomos de hidrógeno. Estos átomos de hidrógeno se transportan hasta las crestas de la membrana interior a lo largo de una cadena de moléculas especiales llamadas coenzimas. Una vez allí, las coenzimas donan los hidrógenos a una serie de proteínas enlazadas a la membrana que forman lo que se llama una cadena de transporte de
electrones. La cadena de transporte de electrones separa los electrones y los protones de cada uno de los diez átomos de hidrógeno. Los diez electrones se envían a lo largo de la cadena y acaban por combinarse con oxígeno y los protones
para formar agua. La energía se libera a medida que los electrones pasan desde las coenzimas a los átomos de oxígeno y se almacena en compuestos de la cadena de transporte de electrones. A medida que éstos pasan de uno a otro, los componentes de la cadena bombean aleatoriamente protones desde la matriz hacia el espacio comprendido entre las membranas interna y externa. Los protones sólo pueden volver a la matriz por una vía compleja de proteínas integradas en la membrana interior. Este complejo de proteínas de

membrana permite a los protones volver a la matriz sólo si se añade un grupo fosfato al compuesto difosfato de adenosina (ADP) para formar ATP en
un proceso llamado fosforilación. El ATP se libera en el citoplasma de la célula, que lo utiliza prácticamente en todas las reacciones que necesitan energía. Se convierte en ADP, que la célula devuelve a la mitocondria para volver a fosforilarlo.
LACTATO DE SODIO
Lactato de sodio
Lactato de sodio
Nombre IUPAC
2-hidroxipropionato de sodio
General
Fórmula molecular C3H5O3.Na
Identificadores
Número CAS 212-762-31
ChEBI 75228

ChemSpider 6049
PubChem 6286
Propiedades físicas
Apariencia líquido transparente
Masa molar 112.0598 g/mol
Propiedades químicas
Solubilidad en agua agua
Familia Lactatos
Valores en el SI y en condiciones estándar
(25 °C y 1 atm), salvo que se indique lo contrario.
[editar datos en Wikidata]
El lactato de sodio es una sal sódica del ácido láctico producida naturalmente mediante la fermentación de azúcares procedentes del maíz o de la remolacha.2 Posee una molécula con forma: NaC3H5O3. Se produce artificialmente igualmente mediante fermentación de substancias azucaradas. Cuando es utilizado en la industria alimentaria se emplea en su denominción el código E 325. Posee diversos empleos, como antioxidante, como estabilizador de otros antoxidantes (sinérgicos de antioxidante) y como prevención de la pérdida de agua de diversos alimentos procesados.
Índice
[ocultar]
1 Propiedades 2 Usos 3 Salud 4 Referencias

Propiedades[editar]
Se presenta en forma de líquido transparente e incoloro, inodoro o con ligero olor característico. Se encuentra disponible también en formato de polvo blanco cristalino. El lactato de sodio se sintetiza artificialmente y naturalmemte mediante la fermentación. En el caso de la fermentación industrial se emplea como substrato el almidón y las melazas. En el caso de la naturaleza, los azúcares procedentes del maíz y de la remolacha. El cuerpo humano sintetiza este compuesto de forma natural en debido a la actividad de la flora intestinal procedente del intestino grueso.3 Posee algunas propiedades quelantes que permite capturar iones de hierro.
Usos[editar]
Se emplea frecuentemente en la industria alimentaria, pudiéndose encontrar en quesos, productos de confitería, enhelados, en la elaboración de diversas gelatinas de fruta y caramelos, margarinas (lácteos en general), sopas y frutas en conserva. En la industria cárnica se emplea como conservante, con su sabor salino característico, en la prevención de proliferación de bacterias patógenas en el pollo.2 Se emplea como un producto que permite hacer sinérgia de antioxidantes
Se suele emplear en la elaboración de ciertos fármacos que tratan los efectos de la deshidratación(predominantemente extracelular) generada por cualquier causa (diarreas, vómitos, fístulas), por hipovolemia, por acidosis metabólica (excepto la acidosis láctica). Se empela igualmente en el tratamiento de aritmias del corazón.4 En la industria de cosméticos puede emplearse como una substancia humectante, en el tratamiento decallosidades en la piel.
Salud[editar]
El lactato de sodio es una de las substancias químicas estudiadas como inductoras químicamente de ataques de pánico en pacientes con cuadros de ansiedad crónica(propiedades panicogénicas).5 Este efecto se lleva estudiando desde los años cuarenta en pacientes administrados por vía intravenosa con existencia de cuadros de ansiedad que se ven abocados a ataques de pánico debido a la realización de ejercicio físico. Cuando se elabora de forma sintética es aceptado por los pacientes deintolerancia a la lactosa, no es así si la procedencia es natural.2
AZUL DE METILENO

Azul de metilenoAzul de metileno
Nombre químico3,7-bis (dimetilamino)-Cloruro de fenazationioCloruro de tetrametiltionina
Fórmula química C16H18N3ClS
Masa molar 319,85 g/mol
Número CAS [61-73-4]
Número EC 200-515-2
Densidad 1.757 g/cm³
Punto de fusión 100 °C
Punto de ebullición Se descompone
SMILESCN(C)c3ccc2nc1ccc(N(C)C)cc1[s+]c2c3.[Cl-]
El azul de metileno, cuyo nombre científico es Cloruro de Metiltionina, es un colorante que se usa para tratar una enfermedad llamada metahemoglobinemia.
Es un compuesto químico heterocíclico aromático con fórmula molecular: C16H18Cl N 3S.
Índice
[ocultar]
1 Medicina o 1.1 Acuicultura

o 1.2 Propiedades 2 Datos técnicos 3 Bibliografía 4 Enlaces externos
Medicina[editar]
El azul de metileno se usa como tintura para teñir ciertas partes del cuerpo antes o durante la cirugía. Su uso es principalmente como antiséptico y cicatrizante interno. También se utiliza como colorante en las tinciones para la observación en el microscopio, y para teñir resultados en los laboratorios.
La empresa farmacéutica TauRx Therapeutics ha comprobado que el uso del azul de metileno (Rember©)1 retrasa el deterioro de las funciones cognitivas de los enfermos de Alzheimer. De cualquier manera, la formulación empleada en los ensayos clínicos no es la utilizada para teñir las células y, por tanto, no debe utilizarse.2
Aunque el mecanismo es la inhibición de la agregación de Tau, parece que mejora la función mitocondrial. Por ello, se ha propuesto que también podría ser utilizado en la lucha contra la enfermedad de Parkinson.
Acuicultura[editar]
Se usa en acuicultura de peces tropicales para tratar las infecciones fúngicas. También puede ser efectivo para tratar peces infectados con el parásito protozoa ich:Ichthyophthirius multifiliis. El azul de metileno es usado en la acuicultura y aficionados a los peces tropicales como un tratamiento para las infecciones por hongos. Puede ser eficaz para el tratamiento de peces infectados con la ICH, los parásitos protozoarios Ichthyophthirius multifiliis. principalmente es usado para proteger los huevos de peces recién puestos de ser infectado por hongos o bacterias. Esto es útil si se quiere incubar artificialmente los huevos de peces. El azul de metileno resulta muy eficaz cuando es utilizado como "baño medicinal de pescado" para el tratamiento de amoniaco, nitrito y el envenenamiento por cianuro, así como para el tratamiento tópico e interno de peces heridos o enfermos como una "primera respuesta".
Propiedades[editar]
Esta sustancia tiene forma de cristales o polvo cristalino y presenta un color verde oscuro, con brillo bronceado. Es Inoloro y estable al aire. Sus soluciones en agua o en alcohol son de color azul profundo. Es fácilmente soluble en el agua y en cloroformo; también es moderadamente soluble en alcohol. también sirve para los hongos de las uñas,otro uso es para tintar la ropa blanca cuando se vuelve amarillenta.

Experimento 2
Succinato de sodio:
Usos: Food Additives
Este producto es un polvo cristalino de color blanco. Sin olor, no ácida, hay sabor de mariscos especial, a través de uso general como agentes aromatizantes, tampones. Se utiliza principalmente en jamón, salchichas, mariscos, condimentos, sake, salsa de soya, salsas y bebidas no alcohólicas y otras industrias alimentarias.
Las normas técnicas
Contenido: 98 a 101%
Solución al 10% el valor de pH: 7-9
Sulfato: ≤ 0,019%
Arsénico (en As): ≤ 2 ppm
Metales pesados (en Pb): ≤ 20 ppm
Prueba de óxido diferente: normal,
El secado de granos: 37 ~ 41% en el caso de anhidro (120 ℃, 3 horas) después de una pérdida del 2% al secarse. Yo peso se mantuvieron sin cambios.
Aplicaciones
Succinato sódico: un polvo blanco, cristalino, con un claro sabor de los mariscos mariscos, y MSG, I G mezclado con un efecto sinérgico de fresca y una buena estabilidad al calor, buena solubilidad, ampliamente utilizado en la sopa instantánea de fideos de mariscos , carne, salsa de soja, productos del mar, condimentos, encurtidos, características succinato de sodio encurtidos:. 1 succinato sódico con características de sabor de mariscos, es un ingrediente para mejorar la comida deliciosa. (2) Además de succinato de sodio puede ser

utilizado solo, pero también puede y glutamato de sodio en combinación con una cierta proporción de la función que mejor puede servir deliciosa. 3 succinato de sodio que tiene un efecto de sabor, a la vez que facilitar otros condimentos estímulos (tales como sabor de sal) producen buen gusto. 4 debido a succinato sódico tiene la estabilidad al calor, que puede jugar su efecto en el tratamiento térmico de los alimentos. 5 solubilidad succinato de sodio, la permeabilidad, la mejora de efecto de sabor, mientras que no es así que el ácido volátil puede evitar que la comida agria.
Precauciones
Este producto es envasado en cartón de 25 kg, el proceso de transporte de la atención con cuidado. Condiciones de almacenamiento: seca y ventilada.
Usos del Succinato De Sodio Alimenticio:
Es utilizado en la fabricación de alimentos, cuenta con etiqueta Kosher. También es utilizado
como excipiente en la elaboración de medicamentos.
Identificadores Químicos del Succinato De Sodio Alimenticio
NFPA 704 del Succinato De Sodio Alimenticio:
0
2
0
Inflamabilidad 0 . Materiales que no se queman.

Salud 2 . Materiales bajo cuya exposición intensa o continua puede sufrirse incapacidad temporal o
posibles daños permanentes a menos que se dé tratamiento médico rápido.
Inestabilidad / Reactividad 0 . Materiales que por sí son normalmente estables aún en condiciones
de incendio y que no reaccionan con el agua.
Inestabilidad / Reactividad . Materiales que por sí son normalmente estables aún en condiciones de
incendio y que no reaccionan con el agua.
Malonato de sodio
El malonato es un inhibidor de la respiración celular, porque se une al sitio activo de la succinato deshidrogenasa en el ciclo del ácido cítrico, pero no reacciona, compitiendo con el succinato. En la reacción de fosforilación oxidativa, el malonato es un inhibidor del complejo II que, nuevamente, contiene succinato deshidrogenasa.1
malonato de sodio(inhibidor de la succinato deshidrogenasa
Actividad mitocondrial?hola a todos!! mi duda es la siguiente: si yo le agrego malonato de sodio(inhibidor de la succinato deshidrogenasa) a mitocondrias activas utilizando piruvato como combustible, la respiracion se detiene y se acumula este intermediario. 1-La inhibicion de la enzima se puede revertir agregando oxalacetato¿Por qué? Si me pueden ayudar con esto desde ya se los voy a agradecer. Besotes!!!
Seguir
1 respuesta
Notificar abuso

Respuestas
Mejor respuesta: O.K. la cosa va más o menos así:
Si tu le agregas piruvato a las mitocondrias estas inician el ciclo de Krebs a traves de la piruvato deshidrogenasa transformando el piruvato en acetilCoenzimaA (acetilCoA) y después en citrato a través de la citrato sintetasa, este citrato es el que propiamente se incorpora al ciclo. Si tu le agregas malonato este inhibe de manera competitiva a la succinato deshidrogenasa haciendo que se acumule el succinato, el alfa-cetoglutarato y el citrato; pero como la inhibición es competitiva, entonces cuando tu agregas oxaloacetato este es transformado en citrato por la citrato sintetasa y este es incorporado al ciclo, por lo que la actividad inhibitoria del malonato se revierte. Recordar los tipos de inhibición enzimática, la inhibición competitiva se caracteriza porque se disminuye la velocidad máxima, pero cuando se agrega más sustrato la velocidad máxima se normaliza porque sigue las leyes de la estequiometría, es decir es más probable que la enzima se encuentre con su sustrato si se aumenta la concentración de este, entonces cuando agregamos oxaloacetato este entra al ciclo aumentando la concentración de succinato que es el sustrato de la succinato deshidrogenasa.
Me hiciste pensar, pero bueno ahí esta, revisa el ciclo de Krebs.
P.D. La razón por la que el malonato inhibe a la succinato deshidrogenasa es porque es una molécula similar al malato y como este es un producto que esta después del paso de la enzima succinatoDH la inhibe (inhibición por producto). Oye y como le hacemos con los besos??? No es cierto no te creas.
Bye y Suerte!!!
Fuente(s):Clases universitarias de Bioquímica.
Cianuro de potasio
El cianuro de potasio o KCN es una sal inorgánica denominada sal de potasio del cianuro de hidrógeno o ácido cianhídrico.

Características[editar]
Es un compuesto cristalino incoloro, similar en apariencia al azúcar, y altamente soluble en agua, en ácidos y bases, es insoluble en etanol o metanol.
Fatalmente tóxico por ingestión, el KCN tiene un olor como el de las almendras amargas,2 pero no todos pueden percibirlo porque la capacidad para ello se debe a un rasgo genético.3 Es una de las pocas sustancias que forman compuestos solubles con el oro formando un complejo cianurado, y por esto se usa en joyería para el dorado químico y para dar brillo a este metal.
Puede usarse en la minería de oro para extraer el metal de los minerales, aunque más comúnmente se usa cianuro de sodio. También se utiliza en la galvanoplastia como agente acomplejante de iones metálicos tales como el cinc, elníquel, el oro y la plata.
Usos[editar]
Es empleado a menudo por entomólogos como agente para matar insectos en los tarros de conservación, ya que la mayoría de los insectos sucumben en segundos, minimizando el daño incluso en las clases más frágiles. El cianuro potásico fue usado por los prisioneros nazis como un medio predilecto y eficiente de suicidio, como fue el caso deGöring y Himmler. Así mismo se empleó en el suicidio masivo de Jonestown
Cianuro de potasio

Cianuro de potasio. El cianuro de potasio o KCN es una sal inorgánica denominada sal de potasio del cianuro de hidrógeno o ácido hidrociánico.
Contenido [ocultar]
1 Características 2 Principales propiedades
físicas y químicas 3 Método de Obtención 4 Aplicaciones 5 Medidas a Medidas a
tomar en caso de derrames y/o fugas
6 Riesgos para la salud 7 Fuente
CaracterísticasEl Cianuro de potasio es un compuesto inorgánico con la fórmula KCN. Este compuesto cristalino incoloro, de aspecto similar al azúcar, es altamente soluble en agua. La mayoría de KCN se utiliza en la extracción de oro, la síntesis orgánica y galvanoplastia. Aplicaciones más pequeñas incluyen la joyería para el dorado químico y pulido.
Dicho compuesto es cristalino incoloro, similar en apariencia al azúcar, y altamente soluble en agua, en ácidos y bases, es insoluble en etanol o metanol.
Fatalmente tóxico por ingestión, el KCN tiene un olor como el de las almendras amargas, pero no todos pueden percibirlo porque la capacidad para ello se debe a un rasgo genético. Es una de las pocas sustancias que forman compuestos
Cianuro de potasio
Nombre (IUPAC) sistemático
General
Otros nombres Cianuro potásico
Fórmula semidesarrollada KCN
Propiedades físicas
Densidad 1520 kg/m 3 ; 1,52g/cm 3
Punto de fusión 907 K (634 °C)
Punto de ebullición 1898 K (1625 °C)
Propiedades químicas
Solubilidad en agua 71,6
Valores en el SI y en condiciones normales
(0 °C y 1 atm), salvo que se indique lo contrario.

solubles con el oro formando un complejo cianurado, y por esto se usa en joyería para el dorado químico y para dar brillo a este metal.
Principales propiedades físicas y químicas
Enlace del Cianuro de potasio
Fórmula química: KCN Nombre químico: Cianuro de potasio Aspecto y color: Cristales sólidos o en diversas formas. Olor Característico. Peso molecular: 65.1 Punto de ebullición: 1625 oC Punto de fusión: 634 oC Peso molecular: 65.1 Densidad relativa (agua = 1): 1.52 Solubilidad en agua: 71,60 g/100 ml a 25 oC
Método de ObtenciónKCN se produce mediante el tratamiento de cianuro de hidrógeno con una solución acuosa al 50% de hidróxido de potasio, seguido por evaporación de la solución en el vacío:
HCN + KOH? KCN + H2O o mediante el tratamiento de formamida con hidróxido de potasio:
HCONH2 + KOH? KCN + 2H2O
Alrededor de 50 000 toneladas de cianuro de potasio se producen anualmente.
AplicacionesKCN y su estrecha relación cianuro de sodio son ampliamente utilizados en síntesis orgánica para la preparación de nitrilos y ácidos carboxílicos, particularmente en la reacción de von Richter.

Es empleado a menudo por entomólogos como agente para matar insectos en los tarros de conservación, ya que la mayoría de los insectos sucumben en segundos, minimizando el daño incluso en las clases más frágiles.
Puede usarse en la minería de oro para extraer el metal de los minerales, aunque más comúnmente se usa cianuro de sodio. También se utiliza en la Galvanoplastia como agente acomplejante de iones metálicos tales como el cinc, el níquel, el oro y la plata.
Bicloruro de mercurio: DESNATURALIZA PROTEINAS
POTENTE VENENO
Cloruro de mercurio (II)
Cloruro de mercurio
Nombre IUPAC
Cloruro de mercurio (II)

General
Otros nombres Cloruro mercúrico;
Cloruro de mercurio (II);
bicloruro de mercurio.
Fórmula semidesarrollada Hg Cl 2
Fórmula estructural
Fórmula molecular ?
Identificadores
Número CAS 7487-94-71
Número RTECS OV9100000
ChemSpider 22517
PubChem 24085
Propiedades físicas
Apariencia Cristal blanco
Densidad 5440 kg/m 3 ; 5.44g/cm 3
Masa molar 271.52 g/mol
Punto de fusión 280 °C (553 K)
Punto de ebullición 302 °C (575 K)
Valores en el SI y en condiciones estándar

(25 °C y 1 atm), salvo que se indique lo contrario.
[editar datos en Wikidata]
El cloruro mercúrico o cloruro de mercurio (II) o bicloruro de mercurio es un compuesto inorgánico de fórmulaHg Cl 2. Es un compuesto muy tóxico. Causa náuseas, vómitos, diarreas, daño renal, vómitos de sangre, hemorragia del estómago, intestinos y otros órganos (especialmente -como suelen hacerlo los compuestos derivados del mercurio- en el cerebro). La ingesta 1 ó 2 g causan casi siempre la muerte.
Aplicaciones[editar]
La principal aplicación del cloruro mercúrico es como catalizador en la conversión del acetileno a cloruro de vinilo, el precursor del PVC:
C2H2 + HCl → CH2=CHCl
Esta tecnología ha sido desplazada por el craqueo térmico de 1,2-dicloroetano.
Referencias[editar]
1. Volver arriba ↑ Número CAS