Curso de postgrado Introducción a la Biotecnología algal · PROTOCOLO C 1- Determinación de la...
Transcript of Curso de postgrado Introducción a la Biotecnología algal · PROTOCOLO C 1- Determinación de la...

1
Curso de postgrado
Introducción a la
Biotecnología algal
Desde el aislamiento de cepas nativas
hasta posibles procesos industriales para
la obtención de biocombustibles y otros
bioproductos.
Protocolos.

2
Listado de protocolos
PROTOCOLO A Observación e Identificación de microalgas y cianobacterias. 3
PROTOCOLO B - Dispositivos de cultivo de microalgas 16
PROTOCOLO C - Determinación de la composición bioquímica de biomasa
algal: determinación de proteínas totales (Método de Lowry)
18
PROTOCOLO D - Transformación nuclear de Chlamydomonas reinhardtii 21
PROTOCOLO E - Determinación de la composición bioquímica de biomasa
algal: Determinación gravimétrica de lípidos totales (Bligh & Dyer)
26
PROTOCOLO F - Detección de lípidos neutros por medio de la técnica de
tinción con Rojo de Nilo
29
PROTOCOLO G - Determinación de la composición bioquímica de biomasa
algal: determinación de carbohidratos totales (Método Antrona)
31
PROTOCOLO H - Parte A: hidrólisis ácida de biomasa algal, fermentación
alcohólica
34

3
PROTOCOLO A
Observación e Identificación de microalgas y cianobacterias
INTRODUCCION
Las algas son organismos muy antiguos que se encuentran presenten en casi
todos los ecosistemas terrestres, presentan una amplia gama de formas, tamaños
y estrategias ecológicas y fisiológicas. Forman un grupo muy diverso, de origen
polifilético, con representantes eucariotas y procariotas, fundamentalmente
acuáticos, autotróficos y/o heterotróficos. Presentan menor complejidad que las
plantas, pero están filogenéticamente relacionadas con las mismas. Tal es así que
presentan rutas metabólicas semejantes como la fotosíntesis oxigénica, y la síntesis
y acumulación de hidratos de carbono y lípidos (Sheehan et al., 1998; Li et al., 2008).
Hasta el momento se han reportado alrededor de 45.000 especies de algas
y se estima que existe más del doble de especies sin identificar. Las algas son uno
de los principales responsables de la producción primaria mundial y son los
productores primarios por excelencia en ambientes acuáticos. Además, participan
en diferentes ciclos biogeoquímicos globales mediante la producción de oxígeno
atmosférico, regulación del clima y la generación de combustibles (Hu et al., 2008;
Sheehan et al., 1998).
Las algas se pueden clasificar de acuerdo a varios criterios tales como su
habitat, tipo de pigmento principal, ciclo de vida, morfología y estructura celular
(Brennan y Owende, 2010). El término microalga hace referencia a un grupo muy
heterogéneo de organismos eucariotas unicelulares cuyo tamaño varía de 2-200µm,
sin embargo, usualmente algunos autores también incluyen dentro de este grupo a
las cianobacterias, organismos procariotas fotosintéticos (Greenwell et al., 2009).
Los principales grupos de microalgas (en términos de abundancia) son:
Cryptophyta, Dinophyta, Euglenophyta, Bacillarophyta y Chlorophyta (Bellinger y
Sigee, 2011; Mutanda et al., 2010, Sheehan et al., 1998).

4
OBJETIVO
Conocer las principales características para la clasificación de microalgas y
cianobacterias y observar las diferentes morfologías y estructuras presentes en las
mismas.
PROCEDIMIENTO
1) En un portaobjetos agregar una gota (10 µL) de cultivo y colocar un
cubreobjetos. Observar la preparación al microscopio, si la imagen no es muy clara
agregar una gota de aceite de inmersión y observar a 50X.
2) Observar morfología y características generales (plastos, pirenoides,
presencia de espinas o espículas, flagelos, estructuras de resistencia, acinetos,
heterocistos, etc.)

5
Recuento celular de microalgas
INTRODUCCION
A pesar del enorme desarrollo tecnológico que ha tenido lugar en los
laboratorios científicos, el conteo visual con hematocitómetro sigue siendo el
método de conteo más utilizado. La cámara Neubauer consiste en una placa gruesa
con forma de porta, cuya porción central está dividida en tres bandas longitudinales
perpendiculares a su eje longitudinal. De ellas, las dos laterales se encuentran sobre
elevadas con respecto de la central en 0.1 mm, y en la central hay grabado un
retículo cuadrangular.
Típicamente, el rango de concentraciones que permite contar el
hematocitómetro está entre 2,5x105 células y 2,5 x106 células por ml. Intentaremos
que la muestra tenga una concentración en torno a 106 (1 millón) aplicando las
diluciones correspondientes.
Por encima de 2,5 millones (2,5 * 106) la probabilidad de cometer errores de
conteo crece demasiado, y también el tiempo y esfuerzo necesario para realizar un
recuento con fiabilidad. Por encima de esta concentración es conveniente diluir la
muestra para acercar la concentración al rango óptimo.
PROCEDIMIENTO
Se toman 10 uL de la muestra de microalgas.
1) Se coloca un cubreobjetos sobre la cámara de Neubauer,
2) Se coloca la punta de la pipeta en el borde del cubreobjetos, en el extremo
de la cámara de Neubauer. Se trata de dejar que el líquido penetre entre la cámara
y el cubreobjetos desde el lateral, por capilaridad.
3) En caso de que aparezcan burbujas, el cubreobjetos se haya movido o
algo no haya salido bien, repetir la operación
4) Observar bajo microscopio óptico a un aumento de 50X

6
MATERIALES
Microscopio óptico
Aceite de inmersión
Cubreobjetos
Portaobjetos
Pipetas
Cámara de Neubauer
BIBLIOGRAFIA
1. Bellinger, E. G., & Sigee, D. C. (2011). Freshwater algae: identification and use as
bioindicators. John Wiley & Sons.
2. Brennan, L., & Owende, P. (2010). Biofuels from microalgae—a review of technologies for
production, processing, and extractions of biofuels and co-products. Renewable and
Sustainable Energy Reviews, 14(2), 557-577.
3. Greenwell, H. C., Laurens, L. M. L., Shields, R. J., Lovitt, R. W., & Flynn, K. J. (2010). Placing
microalgae on the biofuels priority list: a review of the technological challenges. Journal of the
Royal Society Interface, 7 (46), 703-726.
4. Hu, Q., Sommerfeld, M., Jarvis, E., Ghirardi, M., Posewitz, M., Seibert, M., & Darzins, A.
(2008). Microalgal triacylglycerols as feedstocks for biofuel production: perspectives and
advances. The Plant Journal, 54(4), 621-639.
5. Li, Q., Du, W., & Liu, D. (2008). Perspectives of microbial oils for biodiesel production. Applied
Microbiology and Biotechnology, 80(5), 749-756.
6. Mutanda, T., Ramesh, D., Karthikeyan, S., Kumari, S., Anandraj, A., & Bux, F. (2011).
Bioprospecting for hyper-lipid producing microalgal strains for sustainable biofuel
production. Bioresource Technology, 102(1), 57-70.
7. Sheehan, J., Dunahay, T., Benemman, J., Roessler, P.G. 1998. US Department of Energy.s
Office of Fuels development, July 1998. A Look back at the US Department of energy´s
Aquartic Species Program - Biodiesel from Algae, Close out report TP-580-24190. Golden,
CO: National renewable Energy Laboratory.

7
Anexo Protocolo A
CLAVES DICOTÓMICAS PARA IDENTIFICACIÓN DE ALGAS
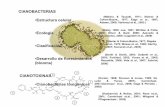
1. Pigmentos dispersos en el citoplasma, sin plástidos ni núcleo definidos, raramente de color verde intenso….CYANOPHYTA
1’. Pigmentos reunidos en uno o varios plástidos, con núcleo….2
2. Plástidos verde intenso….3
2’. Plástidos verde-amarillento, marrones o amarillos….4
3. Reserva de almidón en los plástidos, coloreable con yodo, unicelulares, coloniales o filamentosas….CHLOROPHYTA
3’. Reserva de paramilon fuera de los plástidos, no coloreable con yodo, mayormente
unicelulares….EUGLENOPHYTA
4. Sin reservas de almidón….CHRYSOPHYTA 5
4’. Con reservas de almidón….6
5. Con 1 o 2 flagelos….CHRYSOPHYCEAE
5’. Sin flagelos, con cubierta silícea formada por dos valvas que poseen diversas
ornamentaciones….BACILLARIOPHYCEAE
6. Células provistas de 2 flagelos desiguales y de diferente orientación ubicados en un surco ecuatorial y otro longitudinal….PYRROPHYTA
6’. Células comprimidas provistas de 2 flagelos ligeramente desiguales ubicados en
una foseta subapical….CRYPTOPHYTA
CYANOPHYTA
1. Células solitarias o reunidas en cenobios o colonias....2
1’. Células formando filamentos (tricomas)....5
2. Células irregularmente dispuestas....3
2’. Células regularmente dispuestas....4
3. Células envueltas en vainas gelatinosas estratificadas....Chroococcus
3’. Células rodeadas por vaina gelatinosa difluente, no estratificada....Microcystis
4. Células dispuestas en cenobios planos, rectangulares....Merismopedia
4’. Células dispuestas en la periferia de cenobios
esféricos u ovoides....Coelosphaerium

8
5. Filamentos con heterocistos y/o acinetos....6
5’. Filamentos sin heterocistos ni acinetos, multiplicación sólo por hormogonios....11
6. Heterocistos y acinetos escasos, células terminales generalmente incoloras y
alargadas....Aphanizomenon
6’. Heterocistos y acinetos frecuentes, filamentos solitarios o agrupados....7
7. Filamentos enrollados y entrelazados dentro de una vaina gelatinosa formando un conjunto globoso consistente....Nostoc
7’. Filamentos solitarios o en conjuntos no consistentes....8
8. Filamentos únicamente con acinetos, cortos y con extremos aguzados….Raphidiopsis
8’. Filamentos con heterocistos y acinetos….9
9. Heterocistos generalmente en los extremos del filamento,....Anabaenopsis
9’. Heterocistos generalmente intercalares….10
10. Generalmente células más anchas que largas, filamentos con vaina individual….Nodularia
10’. Generalmente células esféricas o en forma de barril, sin vaina
individual....Anabaena
11. Filamentos provistos de una vaina individual firme....Lyngbya
11’. Filamentos sin vaina....12
12. Filamentos espiralados....Spirulina
12’. Filamentos rectos o curvados....13
13. Células separadas por un puente gelatinoso....Pseudoanabaena 13’. Células adyacentes unidas ....Oscillatoria
CHLOROPHYTA
1. Organismos flagelados, unicelulares o coloniales....Volvocales 2
1’. Organismos no flagelados, unicelulares, cenobiales o filamentosos....5
Volvocales
2. Unicelulares, pared celular gruesa, plástido en forma de copa....Chlamydomonas
2’. Coloniales, de forma esférica o elipsoidal....3
3. Células apretadas unas contra otras....Pandorina
3’. Células más distantes unas de otras....4

9
4. Células dispuestas en capas más o menos paralelas....Eudorina
4’. Células irregularmente dispuestas....Volvox
5. Unicelulares o cenobiales….Chlorococcales 6
5’. La mayoría filamentosos….16
Chlorococcales
6. Unicelulares....7
6’. Cenobiales....9
7. Células fusiformes....Monoraphidium
7’. Células isodiamétricas....8
8. Células esféricas....Chlorella
8’. Células tetraédricas....Tetraedron
9. Células fusiformes....10
9’. Células más isodiamétricas....12
10. Rectas o con forma de media luna poco marcada....Ankistrodesmus
10’. Con forma de media luna bien redondeada....11
11. Células adheridas unas a otras....Selenastrum
11’. Células dispersas....Kirchneriella
12. Células dispersas en una matriz gelatinosa esférica....13
12’. Células adheridas unas a otras....14
13. Células ovoides....Oocystis
13’. Células esféricas....Sphaerocystis
14. Cenobio en forma de empalizada....Scenedesmus
14’. Cenobio con simetría radial....15
15. Cenobio plano....Pediastrum
15’. Cenobio esférico....Coelastrum
16. Filamentos no ramificados, algunas también pueden ser unicelulares….17
16’. Filamentos ramificados….28
17. Zonas de elongación celular en forma de anillo….Oedogonium (Oedogoniales)
17’. Sin zonas de elongación celular diferenciadas….18
18. Conjugación sexual de gametas ameboides no flageladas….Zygnematales 19

10
18’. Gametas flageladas….Ulothrichales 26
Zygnematales
19. Membrana de la célula formando 2 hemicélulas, con poros, en su mayoría unicelulares….Desmidiaceae 20
19’. No forman hemicélulas, todas filamentosas….Zygnemataceae 24
Desmidiaceae
20. Filamentosas….Spondylosium
20’. Unicelulares….21
21. Células sin istmo (constricción que separa las hemicélulas), con forma de media luna más o menos marcada....Closterium
21’’. Células con istmo....22
22. Células con brazos (proyecciones apicales que sobresalen notablemente del cuerpo de la célula)....Staurastrum
22’. Células sin brazos....23
23. Células que presentan numerosos lóbulos profundamente marcados....Euastrum
23’. Células con pocos lóbulos, superficialmente marcados....Cosmarium
Zygnemataceae
24. Plástidos estrellados con un solo pirenoide ….Zygnema
24’. Plástidos con numerosos pirenoides….25
a 1 o 2 plástidos axiales en forma de placa….Mougeotia
25’. 1 a 16 plástidos parietales espiralados….Spirogyra
Ulothrichales
25. Las células quedan unidas de a pares después de la división celular y contenidas dentro de la membrana original....Binnuclearia
26’. Las células no quedan de esa forma....27
26. Células redondeadas en los extremos dispuestas dentro de una vaina general, en los extremos de cada célula se observa un gránulo refringente....Planctonema 27’. Células rectas, con un cloroplasto parietal en forma de anillo incompleto, raramente completo....Ulothrix
27. Monocarióticas, cloroplasto parietal cilíndrico, talo heterotrico (constituido por una parte postrada y filamentos erectos)….Chaetophora (Chaetophorales)
28’. Policarióticas, cloroplasto parietal reticulado con
numerosos pirenoides…Cladophora (Cladophorales)

11
EUGLENOPHYTA
1. Formas sin flagelo, fijas formando colonias....Colacium
1’. Formas flageladas, solitarias, libremente nadadoras....2
2. Células con teca o lórica....3
2’. Células sin teca o lórica....4
3. Lóricas aguzadas en ambos extremos....Strombomonas
3’. Lóricas esféricas o elipsoidales....Trachelomonas
4. Células de sección transversal circular, generalmente alargadas....Euglena
4’. Células de sección transversal comprimida, generalmente
más redondeadas....Phacus
PYRROPHYTA
1. Células sin teca celulósica....Gymnodinium
1’. Células con teca....2
2. Con 1 cuerno largo en la epiteca y 2 o 3 en la hipoteca....Ceratium
2’. Sin cuernos o con cuernos reducidos...3
3. Con 1 placa antiapical (acompañada de 1 suplementaria)....Gonyaulax
3’. Con 2 placas antiapicales más o menos del mismo tamaño....4
4. Con 2 o 3 placas intercalares anteriores y 5 placas postcingulares....Peridinium 4’. Sin placas intercalares anteriores o con 1 sola....Glenodinium
CRYPTOPHYTA
1. Citofaringe conspicua, cromatóforos desde verde-oliva hasta marrones....Cryptomonas
1’. Citofaringe inconspicua o ausente....2
2. Cromatóforo desde verde-oliva hasta marrón o rojo con 1 pirenoide....Rhodomonas
2’. Cromatóforo laminado parietal azul o azul-verdoso....Chroomonas
CHRYSOPHYTA

12
CHRYSOPHYCEAE
1. Células cubiertas por una lóriga en forma de vaso alargado, solitarias o formando colonias arborescentes....Dinobryon
1’. Células cubiertas por escamas silíceas....2
2. Formas solitarias....Mallomonas
2’. Formas coloniales globulosas....Synura

13

14

15

16
PROTOCOLO B
Dispositivos de cultivo de microalgas
OBJETIVO
Conocer y utilizar diferentes sistemas de cultivo de microalgas para la obtención de
biomasa y/o compuestos de interés.
INTRODUCCIÓN
Existen diferentes tipos de sistemas de cultivo de microalgas, en general, se los
puede clasificar en sistemas de cultivo abiertos o cerrados.
Los sistemas de cultivo abiertos comprenden tanto medios naturales (lagunas y
estanques), como artificiales. Entre estos últimos, el más utilizado es el del tipo
“raceway pond”, el cual consiste en un estanque poco profundo (15 a 30 cm) dividido
por un muro central formando 2 canales. La circulación del cultivo se realiza
mediante paletas.
Los sistemas de cultivo cerrados permiten un mejor control de parámetros
(temperatura, luz, pH, etc.), permiten alcanzar mayores productividades, pero
implican mayores costos tanto de instalación como operación. Los diseños en
fotobiorreactores son variados, desde tubulares a planos, entre otros y se suelen
construir en materiales plásticos.
Los fotobiorreactores ambientales (ePBRs) son dispositivos experimentales que
permiten simular las condiciones de cultivo de microalgas a gran escala en piletones
al aire libre, incluyendo la simulación de condiciones climáticas complejas por medio
de sensores incorporados.
PROCEDIMIENTO
El trabajo práctico se dividirá en 4 estaciones:
1) “Raceway ponds”: puesta en marcha e inoculación. A diferentes tiempos se tomarán muestras para seguir crecimiento por densidad óptica (750 nm), recuento celular y peso seco.
2) PBR (fotobiorreactor): puesta en marcha e inoculación. A diferentes tiempos se tomarán muestras para seguir crecimiento por densidad óptica (750 nm), recuento celular y peso seco.

17
3) ePBR (PBR ambiental): Inoculación, establecimiento de parámetros
ambientales (se simularán dos condiciones ambientales de dos lugares
diferentes) y puesta en marcha. Se tomarán muestras periódicamente para
seguir crecimiento por densidad óptica (750 nm) y recuento celular en
hemocitómetro y se determinará el peso seco a tiempo final.
4) Microscopio: se observará la morfología algal y se realizará recuento
celular por medio de un hemocitómetro.

18
PROTOCOLO C
Determinación de la composición bioquímica de biomasa algal:
DETERMINACIÓN DE PROTEÍNAS TOTALES (Método de Lowry)
INTRODUCCIÓN
El método de Lowry consta de dos etapas:
1) Los iones Cu2+, en medio alcalino, se unen a las proteínas formando complejos con los
átomos de nitrógeno de los enlaces peptídicos. Estos complejos Cu2+-proteína tienen un
color azul claro. Además, provocan el desdoblamiento de la estructura tridimensional de la
proteína, exponiéndose los residuos fenólicos de tirosina que van a participar en la segunda
etapa de la reacción. El Cu2+ se mantiene en solución alcalina en forma de su complejo con
tartrato.
2) La reducción, también en medio básico, del reactivo de Folin-Ciocalteu, por los grupos
fenólicos de los residuos de tirosina, presentes en la mayoría de las proteínas, actuando el
cobre como catalizador. El principal constituyente del reactivo de Folin-Ciocalteu es el ácido
fosfo-molibdo-túngstico, de color amarillo, que al ser reducido por los grupos fenólicos da
lugar a un complejo de color azul intenso.
OBJETIVO
Determinar la composición de la biomasa algal, inducida y no inducida para la acumulación
de sustancias de reserva en dos cepas de microalgas de géneros diferentes: Scendesmus
sp. cepa C1S y Desmodesmus sp. cepa FG.

19
PROCEDIMIENTO
1) Centrifugar 1 mL cultivo a 6000 rpm (4°C) durante 5 min. Descartar el sobrenadante.
2) Resuspender las células en 100 uL de dH2O. Realizar una dilución 1/10 y 1/100 a un volumen final de 200 uL.
3) En tubos de hemólisis, colocar 40 uL de la muestra original y de cada dilución (por duplicado).
4) En paralelo realizar la curva estándar con BSA (4 mg/mL). Agregar para 40 uL finales: 0, 5, 10, 20 y 40 uL de BSA y completar con agua (por duplicado).
5) Agregar 10 uL de NaOH 5N a la muestra y a la curva.
6) Colocar en baño térmico a 100 °C durante 10 minutos (tapar los tubos). Enfriar.
7) A los 50 uL de muestra hidrolizada, agregar 1 mL de Reagent A y 100 uL de Folin Reagent 50% (en ddH2O). Vórtex.
8) Incubar 15 min en oscuridad. Vórtex.
9) Leer absorbancia a 750 nm (color azul grisáceo)
10) En paralelo tomar el peso seco a partir de 20 - 50 mL de la muestra desde el cultivo original.
11) Calcular la composición centesimal de proteínas totales de la muestra (% p/p).
Reagent A: 10 mL Na2CO3 2% en NaOH 0.1N
100 ul CuSO4 1 %
100 ul KNa Tartrato 2 %
Folin-Ciocalteu 50%

20
MATERIALES
Falcon 50 ml
Eppendorfs 1.5 ml
Pipetas y tips 5 ml/1 ml/ 200 ul/ 20 ul
Tubos de hemólisis y tapas
Guantes, guardapolvo y protección ocular
EQUIPO
Baño térmico
Vórtex
Espectrofotómetro/cubetas de vidrio 1 ml
Balanza analítica
Centrífugas
Baño seco
REACTIVOS
NaOH 5N
Reagent A
Folin B
BIBLIOGRAFIA
1. Lowry, O. H., Rosebrough, N. J., Farr, A. L., & Randall, R. J. (1951). Protein measurement with
the Folin phenol reagent. Journal of biological chemistry, 193(1), 265-275.

21
PROTOCOLO D
Transformación nuclear de Chlamydomonas reinhardtii
Parte A: Método de agitación con perlas de vidrio
INTRODUCCIÓN
Las microalgas constituyen un grupo heterogéneo de microorganismos,
mayoritariamente fotosintéticos, con gran importancia ecológica y con un enorme
potencial biotecnológico. Varias especies se utilizan actualmente para la producción
a gran escala de carotenoides, ácidos grasos poliinsaturados y otros compuestos
de alto valor añadido con aplicaciones en la industria alimentaria, dietética,
cosmética y de química fina. Más aún, algunas especies de microalgas han sido
propuestas como sistemas alternativos para la expresión de proteínas heterólogas,
incluyendo anticuerpos y otras proteínas terapeúticas y en los últimos años ha
habido un creciente interés en las microalgas como posible materia prima para una
tercera generación de biocombustibles renovables con un balance neutral de
carbono (Mayfield et al.,2007; Radakovits et al., 2010).
A pesar del gran interés biotecnológico de las microalgas, no existe un método
robusto para la transformación estable de la mayoría de las especies. La primera
microalga modificada genéticamente fue la clorofita de agua dulce, Chlamydomonas
reinhardtii.
Existen varios métodos para introducir los genes deseados en la célula
hospedadora. Los más usuales para la transformación de microalgas son: el
bombardeo de microproyectiles o biobalística, la electroporación, fibras de carburo
de silicio y el método de agitación con perlas de vidrio y transformación mediada por
Agrobacterium tumefaciens. (Kindle, 1990; (Kindle et al., 1991; Kumar et al., 2004;
Mayfield et al., 2007; Jeon et al 2013).
Chlamydomonas reinhardtii, ha demostrado ser un organismo muy versátil que
puede ser utilizado tanto en estudios de ciencia básica como en diversas
aplicaciones biotecnológicas.

22
Su transformación genética es relativamente sencilla tanto a nivel nuclear como de
cloroplasto.
OBJETIVO
Modificar genéticamente una cepa de Chlamydomonas reinhardtii CW15 (que
carece de pared celular), por dos métodos diferentes: electroporación y agitación
con perlas de vidrio.

23
PROCEDIMIENTO
1) Colectar 25 -50 mL de cultivos de Chlamydomonas reinhardtii CW15 en fase
exponencial temprana, 1.106 – 2.106 células/mL (OD750 0.2 - 0.4). (La densidad
celular es un variable esencial en la eficiencia de transformación, se pueden usar
densidades menores a 1.106, pero no es recomendable usar densidades mayores
a 3.106 células/mL).
Centrifugar a 2500 rpm durante 10 minutos y descartar el sobrenadante.
2) Resuspender en 5mL de medioTAP.
3) Centrifugar a 2500 rpm durante 10 minutos y descartar el sobrenadante.
4) Repetir pasos c y d.
5) Resuspender en 250 µL de medioTAP.
6) Agregar 2 - 4µg de ADN plasmídico con el gen de interés, previamente linealizado
(pChlamy_4 con ScaI y pCAMBIA 1302 con EcoRI. (La trasformación se puede
llevar a cabo con el plásmido en su forma circular, si se quiere una mayor eficiencia
debe linealizarse).
7) Transferir el mix a tubos de vidrio con 0,3g de esferas de vidrio e incubar al menos
5 minutos a 4°C.
8) Agitar en vortex a velocidad máxima 25 segundos.
9) Transferir las células transformadas a tubos Falcon de 50 mL con 5 mL de
solución TAP-Sac 40 mM.
10) Incubar a 28°C y 50 ±10 µmol m-2 s-1 y agitación a 110 rpm por 24 horas para
permitir la recuperación de las células después de la electroporación. La agitación
no debe omitirse.
11) Centrifugar a 2500 rpm durante 10 minutos y descartar el sobrenadante.
Plaquear las células usando una caja por cada tubo en medio TAP con 5 µg mL-1
de zeocina si se usa el plásmido pChlamy_4, ó 10 µg mL-1 de higromicina si se usa
el plásmido pCAMBIA 1302.
12) Las colonias serán visibles a simple vista a partir del día 7 de cultivo.

24
Parte B: Método de electroporación
PROCEDIMIENTO
1) Colectar 25 - 50 mL de cultivos de Chlamydomonas reinhardtii CW15 en fase
exponencial temprana, 1.106 – 2.106 células/mL (OD750 0.2 - 0.4). (La densidad
celular es un variable esencial en la eficiencia de transformación, se pueden usar
densidades menores a 1.106, pero no es recomendable usar densidades mayores
a 3.106 células/mL).
2) Centrifugar a 2500 rpm durante 10 minutos y descartar el sobrenadante.
3) Resuspender en 5mL TAP-SAC 40 mM (sacarosa) o 5mL solución de
transformación (ej: GeneArt MAX Efficiency).
4) Centrifugar a 2500 rpm durante 10 minutos y descartar el sobrenadante.
5) Repetir pasos c y d.
6) Resuspender en 250 µL TAP-SAC 40 mM (sacarosa) o 250 µL solución de
transformación (ej: GeneArt MAX Efficiency).
7) Agregar 2 - 4µg de ADN plasmídico con el gen de interés, previamente
linealizado (pChlamy_4 con ScaI y pCAMBIA 1302 con EcoRI. (La trasformación se
puede llevar a cabo con el plásmido en su forma circular, si se quiere una mayor
eficiencia debe linealizarse).
8) Transferir las mezclas a cubetas de electroporación (0.4 cm) e incubar al menos
5 minutos a 4°C.
9) Electroporar bajo los siguientes parámetros: 600 V, 50 µF y resistencia infinita.
10) Después de la electroporación, transferir las células transformadas a tubos
Falcon de 50 mL con 5 mL de solución TAP-Sac 40 mM.
11) Incubar a 28°C y 50 ±10 µmol m-2 s-1 y agitación a 110 rpm por 24 horas para
permitir la recuperación de las células después de la electroporación. La agitación
no debe omitirse.
12) Centrifugar a 2500 rpm durante 10 minutos y descartar el sobrenadante.
Plaquear las células usando una caja por cada tubo en medio TAP con 5 µg mL-1
de zeocina si se usa el plásmido pChlamy_4, ó 10 µg mL-1 de higromicina si se usa
el plásmido pCAMBIA 1302.

25
13) Las colonias serán visibles a simple vista a partir del día 7 de cultivo.
Esta metodología está basada en el protocolo de transformación del kit comercial
GeneArt Chlamydomonas TOPO Engineering, cat. A142664 (Invitrogen).
MATERIALES
Medio TAP
Solucion Sacarosa
Erlenmeyer 100 – 250mL
Tubos Falcon 15 -50mL
Tubos eppendorf 1,5 mL
Electroporador
Perlas de vidrio (0,2mm) Vectores utilizados
pChlamy_ 4
pCambia 1302 Agentes de selección
Zeocina
Higromicina
BIBLIOGRAFIA
1. Jeon, K., Suresh, A., & Kim, Y. C. (2013). Highly efficient molecular delivery into Chlamydomonas
reinhardtii by electroporation. Korean Journal of Chemical Engineering, 30(8), 1626-1630.
2. Kindle, K. L. (1990). High-frequency nuclear transformation of Chlamydomonas
reinhardtii. Proceedings of the National Academy of Sciences, 87(3), 1228-1232.
3. Kindle, K. L., Richards, K. L., & Stern, D. B. (1991). Engineering the chloroplast genome:
techniques and capabilities for chloroplast transformation in Chlamydomonas
reinhardtii. Proceedings of the National Academy of Sciences, 88(5), 1721-1725.
4. Kumar, S. V., Misquitta, R. W., Reddy, V. S., Rao, B. J., & Rajam, M. V. (2004). Genetic
transformation of the green alga—Chlamydomonas reinhardtii by Agrobacterium tumefaciens. Plant
Science, 166(3), 731-738.
5. Mayfield, S. P., Manuell, A. L., Chen, S., Wu, J., Tran, M., Siefker, D., ... & Marin-Navarro, J. (2007).
Chlamydomonas reinhardtii chloroplasts as protein factories. Current opinion in biotechnology, 18(2),
126-133.
6. Radakovits, R., Jinkerson, R. E., Darzins, A., & Posewitz, M. C. (2010). Genetic engineering of
algae for enhanced biofuel production. Eukaryotic cell, 9(4), 486-501.

26
PROTOCOLO E
Determinación de la composición bioquímica de biomasa algal:
Determinación gravimétrica de lípidos totales (Bligh & Dyer)
INTRODUCCIÓN
El Método de Bligh& Dyer, es un método simple y rápido de extracción y
recuperación de lípidos basado en la extracción liquida en un sistema de dos fases,
por medio de la homogenización de la muestra con cloroformo, metanol y agua.
Al añadir alícuotas de cloroformo y agua se logra la separación de fases. El material
lípidico se encuentra en la fase no acuosa, mientras que el material no lípidico se
encuentra en la fase acuosa.
OBJETIVO
Determinar la composición de la biomasa algal, inducida y no inducida para la
acumulación de sustancias de reserva en dos cepas de microalgas de géneros
diferentes: Scendesmus sp. cepa C1S y Desmodesmus sp. cepa FG.

27
PROCEDIMIENTO
1) Centrifugar 50 mL cultivo a 6000 rpm (4°C) durante 5 min. Descartar el sobrenadante.
2) Resuspender las células en 2 mL de NaCl 1M y transferir a tubos Kimble de 15 mL.
3) Sonicar (al menos) por 2 ciclos de 1 min (10 segundos ON, 1 segundo OFF), 40% potencia. (El tiempo de sonicado varía de acuerdo a la cepa seleccionada).
4) Agregar 4 mL de metanol y perlas de vidrio de diferentes tamaños, para completar la ruptura celular. Vórtex 2-5 min.
5) Agregar 4 mL de cloroformo y 1 mL de NaCl 1M. Vórtex 5 minutos y agitación manual hasta lograr emulsión.
6) Centrifugar 6000 rpm (4°C) durante 10 minutos. Tomar la fase inferior (pigmentada) y colocar en una placa de Petri, previamente pesada.
7) Vórtex de la fase acuosa (1-2 min, hasta dispersión).
8) Agregar 3 mL de cloroformo. Vórtex 10 minutos y agitación manual.
9) Centrifugar 6000 rpm (4°C) durante 10 minutos. Combinar con extracto anterior. Repetir extracción con 3 mL de cloroformo una vez más y combinar.
10) Evaporar el extracto en la cápsula de Petri.
11) En paralelo tomar el peso seco a partir de 20 - 50 mL de la muestra desde el cultivo original.
12) Calcular y expresar la composición centesimal de lípidos totales de la muestra (% p/p).

28
13) MATERIALES
Falcon 50 mL
Eppendorfs 1.5 mL
Vaso de precipitados
Hielera/Hielo
Bolitas de vidrio
Placas de Petri chicas
Kimble 15 mL
Pipetas y tips 5mL/1mL
Guantes, guardapolvo y protección ocular
Rotulador
EQUIPOS
Balanza analítica
Baño seco
Vórtex
Sonicador
Centrífugas
Ventilador
REACTIVOS
NaCl 1M
Metanol
Cloroformo
BIBLIOGRAFIA
1. Bligh, E. G., & Dyer, W. J. (1959). A rapid method of total lipid extraction
and purification. Canadian journal of biochemistry and physiology, 37(8),
911-917.

29
PROTOCOLO F
Detección de lípidos neutros por medio de la técnica de
tinción con Rojo de Nilo
INTRODUCCION
El Rojo de Nilo (9-diethylamino-5H-benzo (alpha) phenoxazine-5-one), es un
colorante liposoluble e intensamente fluorescente en determinadas longitudes de
onda, que permite la detección de lípidos in situ, por medio de técnicas
fluorométricas (Elsey et al., 2007; Chen et al., 2009).
OBJETIVO
Evaluar la acumulación de lípidos neutros (LN), en células previamente inducidas
por medio de privación de nitrógeno.

30
PROCEDIMIENTO
1) Tomar 1 – 3 mL de cultivo de microalgas.
2) Agregar 5 μM del colorante Rojo de Nilo y un 20% DMSO (permite la
permeabilización de las membranas y paredes celulares)
3) Incubar por 30 minutos en oscuridad.
4) Para una determinación cuantitativa, las células tratadas con Rojo de Nilo utilizar
un espectrofluorómetro (excitar con luz polarizada a 486 nm (Shimadzu, model RF-
540), registra el pico de emisión a 556 nm. Evaluar la acumulación de lípidos en
cultivos analizando el espectro de emisión entre 500 y 700 nm.
5) Para una determinación cualitativa, observar las células en microscopio de
fluorecsencia.
MATERIALES
Colorante Rojo de Nilo Microscopio de fluorescencia Espectrofluorometro
BIBLIOGRAFIA
1. Chen, W., Zhang, C., Song, L., Sommerfeld, M., & Hu, Q. (2009). A high throughput Nile red
method for quantitative measurement of neutral lipids in microalgae. Journal of microbiological
methods, 77(1), 41-47.
2. Elsey, D., Jameson, D., Raleigh, B., & Cooney, M. J. (2007). Fluorescent measurement of
microalgal neutral lipids. Journal of microbiological methods, 68(3), 639-642.

31
PROTOCOLO G
Determinación de la composición bioquímica de biomasa algal:
DETERMINACIÓN DE CARBOHIDRATOS TOTALES (Método Antrona)
INTRODUCCIÓN
El método de Antrona, permite la cuantificación de una amplia gama de
carbohidratos.
En presencia de ácido sulfúrico concentrado, los carbohidratos son deshidratados
a furfurales (o hidroxi-metil-furfurales) los cuales condensan con antrona (10-ceto-
9,10-dihidroantraceno) dando un complejo azul verdoso. La intensidad del color es
cuantificada mediante medición de la absorbancia a 620 nm.
OBJETIVO
Determinar la composición de la biomasa algal, inducida y no inducida para la
acumulación de sustancias de reserva en dos cepas de microalgas de géneros
diferentes: Scendesmus sp. cepa C1S y Desmodesmus sp. cepa FG.

32
PROCEDIMIENTO
1) Centrifugar 5 mL cultivo a 6000 rpm (4°C) durante 5 min. Descartar el
sobrenadante.
2) Resuspender las células en 500 uL de dH2O. Realizar una dilución 1/10 y 1/100
a un volumen final de 200 uL.
3) En tubos de hemólisis, colocar 200 uL de la muestra original y de cada dilución
(por duplicado).
4) En paralelo realizar la curva estándar con Glucosa (10 mM). Agregar para 200
uL finales: 0, 5, 10, 20 y 40 uL de glucosa y completar con agua (por duplicado).
5) Agregar 1 mL del reactivo Antrona a la muestra y a la curva.
6) Colocar en baño térmico a 100 °C durante 15 minutos (tapar los tubos). Enfriar.
Vórtex.
7) Leer absorbancia a 620 nm (color verde)
8) En paralelo tomar el peso seco a partir de 20 - 50 mL de la muestra desde el
cultivo original.
9) Calcular la composición centesimal de carbohidratos totales de la muestra (%
p/p).
10)
Reactivo Antrona (100 mL): En hielo mezclar: 28 mL dH2O
72 mL de H2SO4
50 mg Antrona
1 g tiourea
MATERIALES
Tubos falcon 15 ml
Tubos falcon 50 ml
Pipetas y tips 5ml/ 1ml/ 200 ul/ 20 ul

33
Eppendorfs
Tubos de hemólisis y tapas
Guantes, guardapolvo, protección ocular y máscara de gases
Papel de cocina
Vaso de precipitados de descarte
EQUIPOS
Baño térmico
Centrífugas
Balanza analítica
Vórtex
Espectrofotómetro/ cubetas de vidrio 1 ml
REACTIVOS
Antrona
BIBLIOGRAFIA
1. Dreywood, R. (1946). Qualitative test for carbohydrate material. Industrial &
Engineering Chemistry Analytical Edition, 18(8), 499-499.

34
PROTOCOLO H
Parte A: HIDRÓLISIS ÁCIDA DE BIOMASA ALGAL,
FERMENTACIÓN ALCOHÓLICA
INTRODUCCIÓN
En la actualidad, el biocombustible de mayor producción y distribución mundial es
el etanol, derivado principalmente de fuentes de sacarosa o almidón de
provenientes de cultivos agrícolas, como la caña de azúcar y el maíz (Gray et al.,
2011; Nigam 2011).
Recientemente, las microalgas se ha postulado a las microalgas como materia
prima alternativa a los cultivos tradicionales, con un alto potencial para la producción
de biocombustibles (Nigam 2011; Brennan y Owende 2010), ya que presentan
algunas ventajas en comparación con los cultivos convencionales.
Se ha reportado que varias cepas de microalgas acumulan grandes de cantidades
de carbohidratos (superiores al 40% de la biomasa seca) (Cheaudhary et al., 2014;
Dragone et al., 2011) principalmente como almidón insoluble y celulosa (Dragone et
al., 2011; Domozich et al., 2012). La acumulación de estos azucares se produce en
respuesta a un estres, actualmente el método más utilizado para la inducción de la
acumulación esta respuesta es el estrés nutricional por privación de nutrientes
(Sanchez-Rizza et al., 2017).
A pesar de que la biomasa de microalgas, no es un directamente utilizable por parte
de los microorganismos fermentadores para producir etanol, se acepta que sería
potencialmente más sencillo convertirla en monosacáridos en comparación con los
materiales lignocelulósicos de plantas, principalmente por la ausencia de lignina.
Debido a la tolerancia a altas concentraciones de bioetanol, Saccharomyces
cerevisiae es utilizada como organismo fermentador. Sin embargo, este tipo de
levaduras consumen sólo azúcares simples, como la glucosa. Por lo tanto, el

35
almidón debe ser convertido a azúcares simples, mediante hidrólisis ácida, alcalina
o enzimática (Lee et al., 2016).
La hidrólisis ácida bajo altas temperaturas y presiones es más rápida, fácil y barata
que otros tipos de hidrólisis, pero puede conducir a la descomposición de azúcares
e inhibidores del proceso de fermentación. Por el contrario, la hidrólisis enzimática
se puede completar bajo temperaturas y presiones suaves, pero es más lento, más
caro, y todavía requiere pre-tratamientos físicos o químicos (Choi et al., 2010;
Baeyens et al., 2015; Hernandez et al., 2016).
PROCEDIMIENTO
1) En un tubo Falcon de 15 mL, resuspender 20% de sólidos algales, en 2% de
H2SO4, colocar perlas de vidrio, tapar y agitar vigorosamente en forma manual y con
vórtex. Hidrolizar durante 30 min en autoclave (Perforar la tapa del tubo). Volumen
final: 10 mL. Enfriar.
2) Centrifugar durante 15 min a 8000 rpm (4°C).
3) Trasvasar la fracción soluble a un vaso de precipitados, y llevar a pH 4.5 con
Mg(OH)2. Agitar el hidrolizado con un buzo magnético y utilizar cintas de papel pH
para su medición. Centrifugar 5 min 600rpm.
4) Tomar 100 uL del sobrenadante para cuantificar los carbohidratos totales de la
fracción soluble, mediante el método de Antrona.
5) Fraccionar en viales: 1 mL del hidrolizado a pH 4.5 y en paralelo fraccionar 1 mL
del medio de cultivo control YPD (Yeast extract, Peptone, Dextrose) a pH 4.5, con
una concentración de dextrosa del 10%.
6) Activar la levadura (Saccharomyces cerevisiae) e inocular a un OD 600nm de
0,25. Para activar la levadura, la misma se resuspenderá en 1 mL de dextrosa 0,5
%. Vórtex. Centrifugar a 6000 rpm (4°C) durante 5 minutos. Resuspender en 250
uL. Determinar el OD inicial a 600nm y calcular el volumen correspondiente para
inocular los medios de cultivo (algal y YPD).

36
7) Colocar buzos magnéticos chicos a cada vial y tapar con Parafilm. Perforar con
aguja 5 veces el Parafilm.
8) Colocar los viales en plancha agitadora magnética a 30°C durante 24 hs.
9) Pasadas las 24 hs, tomar una muestra de OD600 nm final y centrifugar el
fermento en tubos eppendorf previamente tarados. 6000 rpm durante 10 min (4°C).
10) Transferir el sobrenadante a otro tubo eppendorf para la determinación
enzimática de alcohol y determinar el peso seco final de la levadura.
11) Realizar diluciones del sobrenadante: 1/5, 1/10 y 1/100.
12) Determinar carbohidratos totales de la fracción soluble, mediante el método de
Antrona.
13) Realizar el ensayo enzimático para determinación de etanol.
MATERIALES
Tubos Falcon 50 mL
Vaso de precipitados
Buzos magnéticos
Pipetas y tips 5mL / 1mL/ 200 uL / 20 uL
Viales de 3 mL
EQUIPOS
Autoclave
Plancha agitadora magnética
Centrífuga Sorvall
Cintas papel pH
REACTIVOS Y MEDIOS DE CULTIVO
H2SO4 9.8%
Mg(OH)2 3.6M
Medio YPD 2% pH 4.5
Antrona

37
PARTE B: DETERMINACIÓN ENZIMÁTICA DE ETANOL
INTRODUCCIÓN
Este ensayo enzimático se realiza con la enzima ADH (alcohol deshidrogenasa)
purificada de cultivos de Saccharomyces cerevisiae. Estas enzimas acoplan la
conversión del alcohol en aldehídos o cetonas, con la reducción de NAD+ (a NADH).
La reacción catalizada es: alcohol + NAD+ aldehído o cetona + NADH
Por lo tanto, la cuantificación de etanol es una medición indirecta dada por la
reducción de NAD+, dependiente de etanol.

38
PROCEDIMIENTO
1) Reacción:
ADH 1/10: 10 uL
NAD+ 25 mM 10 uL
Buffer Tris-HCl pH 8.4 10 uL
H2O 50 uL
Volumen de muestra 20 uL
2) Realizar en paralelo una curva estándar con etanol de grado analítico 99%
pureza (v/v).
3) Incubar durante 25 minutos a RT
4) Agregar 400 uL de dH2O
5) Medir Abs 340 nm (visible) en cubetas de cuarzo de 500 uL
EQUIPOS
Espectrofotómetro/ cubetas de cuarzo de 500 ul
REACTIVOS
ADH 1/10
NAD+ 25 mM
Buffer Tris-HCl pH 8.4

39
BIBLIOGRAFIA
[1] K.A. Gray, L. Zhao, M. Emptage, Bioethanol, Curr. Opin. Chem. Biol. 10 (2006) 141–146.
[2] P.S. Nigam, A. Singh, Production of liquid biofuels from renewable resources, Prog. Energ.
Combust. 37 (2011) 52–68.
[3] J. Baeyens, Q. Kang, L. Appels, R. Dewil, Y. Lv, T. Tan, Challenges and opportunities in improving
the production of bio-ethanol, Prog. Energ. Combust. 47 (2015) 60–88.
[4] L. Brennan, P. Owende, Biofuels from microalgae: a review of technologies for production,
processing, and extractions of biofuels and co-products, Renew. Sust. Energ. Rev. 14 (2010) 557–
577.
[5] M. Navid, M. Borowitzk, The long-term culture of the coccolithophore Pleurochrysis carterae
(Haptophyta) in outdoor raceway ponds, J. Appl. Phycol. 18 (2006) 703–712.
[6] S. Sumathi, S.P. Chai, A.R. Mohamed, Utilization of oil palm as a source of renewable energy in
Malaysia, Renew. Sust. Energ. Rev. 12 (2008) 2404–2421.
[7] A. Singh, P.S. Nigam, J.D. Murphy, Renewable fuels from algae: an answer to debatable land
based fuels, Bioresour. Technol. 102 (2011) 10–16.
[8] Y. Zhou, L. Schideman, G. Yu, Y. Zhang, A synergistic combination of algal wastewater treatment
and hydrothermal biofuel production maximized by nutrient and carbon recycling, Energy Environ.
Sci. 6 (2013) 3765–3779.
[9] M. Do Nascimento, J.C.F. Ortiz-Marquez, L. Sanchez-Rizza, M. Echarte, L. Curatti, Bioprospecting
for fast growing and biomass characterization of oleaginous microalgae from south-eastern Buenos
Aires, Argentina, Bioresour. Technol. 125 (2012) 283–290.
[10] L. Chaudhary, P. Pradhan, N. Soni, P. Singh, A. Tiwari, Algae as a feedstock for bioethanol
production: new entrance in biofuel world, Int. J. Chem. Technol. Res. 6 (2014) 1381–1389.
[11] G. Dragone, B.D. Fernandes, A.P. Abreu, A.A. Vicente, J.A. Teixeira, Nutrient limitation as a
strategy for increasing starch accumulation in microalgae, Appl. Energy 88 (2011) 3331–3335.
[12] D.S. Domozych, M. Ciancia, J.U. Fangel, M.D. Mikkelsen, P. Ulvskov, W.G.T. Willats, The cell
walls of green algae: a journey through evolution and diversity, Front. Plant Sci. 3 (2012) 82.

40
[13] L. Sánchez Rizza, M.E. Sanz Smachetti, M. Do Nascimento, G. L. Salerno, L. Curatti,
Bioprospecting for native microalgae as an alternative source of sugars for the production of
bioethanol, Algal Research 22 (2017) 140-147.
[14] Lee Muei Chng, Derek J.C. Chan, Keat Teong Lee, Sustainable production of bioethanol using
lipid-extracted biomass from Scenedesmus dimorphus, Journal of Cleaner Production (2016).
[15] D. Hernández, B. Riaño, M. Coca, M.C. García-González, Saccharification of carbohydrates in
microalgal biomass by physical, chemical and enzymatic pre-treatments as a previous step for
bioethanol production, Chem. Eng. J. 262 (2015) 939–945.
[16] S.P. Choi,M.T. Nguyen, S.J. Sim, Enzymatic pretreatment of Chlamydomonas reinhardtii
biomass for ethanol production, Bioresour. Technol. 101 (2010) 5330–5336.