Cinética Enzimática de la Glucosa-Oxidasa
-
Upload
david-henriquez-chavez -
Category
Documents
-
view
1.612 -
download
10
Transcript of Cinética Enzimática de la Glucosa-Oxidasa

[Práctica 3: Cinética Enzimática de la Glucosa-Oxidasa] Introducción a la Biotecnología
1
RREESSUUMMEENN
El presente reporte está elaborado en miras a focalizar y entender la aplicación del método
experimental en lo que refiere a la verificación de mediciones haciendo uso del modelo de
Michaelis-Menten para una reacción química a través del estudio de la catálisis enzimática para la
enzima “glucosa-oxidasa” al preparar soluciones con diferentes concentraciones de glucosa (50,
100, 500, 1000, 2000, 3000 y 4000 ppm), donde en los frascos del espectrofotómetro a 10μL de
solución de glucosa se le añadían 10 ml de reactivo enzimático(Glucosa Oxidasa) para todas las
soluciones de las diferentes concentraciones preparadas, luego en un frasco aparte se preparó el
blanco para la realización de la curva de calibración, el cual se preparó usando 10 ml de reactivo
enzimático con 100μL de agua destilada, para cada solución de las diferentes concentraciones se
dio un tiempo de reacción de 45 minutos a 25ºC y se tomaba la lectura de la absorbancia cada 5
min. hasta llegar a 30 min. y luego hasta 45 min. Luego, con los datos de absorbancia obtenidos
para las diferentes concentraciones se elaboró la curva de calibración y el cálculo de las
concentraciones de quinoneimina producidas existentes en cada tiempo “t” junto con el cálculo de
la velocidad de aparición de ésta y la velocidad de desaparición de la glucosa, para después
establecer para cada concentración los parámetros de Michaelis-Menten que se muestran en los
cálculos mostrados en éste reporte.
IINNTTRROODDUUCCCCIIÓÓNN TTEEÓÓRRIICCAA
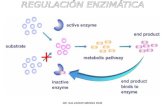
La cinética enzimática estudia la velocidad de
las reacciones catalizadas por enzimas. Estos
estudios proporcionan información directa
acerca del mecanismo de la reacción
catalítica y de la especifidad de la enzima.1
La velocidad de una reacción catalizada por una enzima puede medirse con relativa facilidad. La medida se realiza siempre en las condiciones óptimas de pH, temperatura, presencia de cofactores, etc, y se utilizan concentraciones saturantes de sustrato. En estas condiciones, la velocidad de reacción observada es la velocidad máxima. La velocidad puede determinarse bien midiendo
1 PRODUCTION AND APPLICATION OF ENZYME
http://www.biosimex.com.mx/pdf/insertos%20dedic
ados/Quimica%20clinica/12503%20glucosa.pdf
la aparición de los productos o la desaparición de los reactivos.
Al seguir la velocidad de aparición de producto (o de desaparición del sustrato) en función del tiempo se hace el estudio de la cinética de la reacción. A medida que la reacción transcurre, la velocidad de acumulación del producto va disminuyendo porque se va consumiendo el sustrato de la reacción. Para evitar esta complicación se procede a medir la velocidad inicial de la reacción (v0). La velocidad inicial de la reacción es igual a la pendiente de la curva de avance a tiempo cero. De esta forma, la medida de v0 se realiza antes de que se consuma el parte del total del sustrato, de forma que pueda considerarse la [S] como esencialmente constante a lo largo del experimento.2
2Mier, Geraldine; Rhodes, V.J.; Maharg, Leta; Webb,
Nancy, S; et al.: BEEF TENDERIZATION WITH

[Práctica 3: Cinética Enzimática de la Glucosa-Oxidasa] Introducción a la Biotecnología
2
Además, en estas condiciones no es necesario considerar la reacción inversa, ya que la cantidad de producto formada es tan pequeña que la reacción inversa apenas ocurre. De esta forma se simplifican enormemente las ecuaciones de velocidad.
En otras palabras:
[S]= concentración del sustrato
[P]= concentración del producto
[v0]= velocidad inicial
+ = aparición de producto
- = desaparición de sustrato
Se ha tomado el supuesto que la enzima usada en la práctica (Glucosa-Oxidasa) se comporta según el modelo de cinética de Michaelis-Menten de donde se deduce la siguiente ecuación:
La ecuación es la base de la mayoría de las cinéticas enzimáticas de sustrato único.
La constante de Michaelis Km se define como la concentración a la que la velocidad de la reacción enzimática es la mitad de la Vmax.
3
PROTELYITIC ENZYMES; E.E.U.U.; Food Tech; p.16,111;
Dairy Sci. Abstracts; p.23,197.
3 Murray, Robert; Granner, Daryl; Rodwell, Victor;
Mayes, Peter; 1997; BIOQUÍMICA DE HARPER; México;
Editorial El Manual Moderno; p.77-93.
http://www.biosimex.com.mx/pdf/insertos%20dedic
ados/Quimica%20clinica/12503%20glucosa.pdf
Una forma práctica de linealizar los datos es haciendo uso de la gráfica de Lineweaver-Burk, que es la forma más común de mostrar los datos cinéticos. Para ello, se toman los valores inversos a ambos lados de la ecuación de Michaelis-Menten, el resultado de este tipo de representación es una línea recta cuya ecuación es y = mx + c, siendo el punto de corte entre la recta y el eje de ordenadas equivalente a 1/Vmax, y el punto de corte entre la recta y el eje de abscisas equivalente a -1/Km.4
Fig. 1:
La recta obtenida de la linealización es la pendiente que representa a: Km/Vmax, el intercepto es equivalente a 1/Vmax de la
reacción enzimática.
El reactivo enzimático del que se hará uso
contiene dos enzimas: Glucosa-Oxidasa
(GOD), la cual se hidroliza a ácido glucónico
4 Murray, Robert; Granner, Daryl; Rodwell, Victor;
Mayes, Peter; 1997; BIOQUÍMICA DE HARPER; México;
Editorial El Manual Moderno; p.93-98.
Mier, Geraldine; Rhodes, V.J.; Maharg, Leta; Webb,
Nancy, S; et al.: BEEF TENDERIZATION WITH
PROTELYITIC ENZYMES; E.E.U.U.; Food Tech; p.16,111;
Dairy Sci. Abstracts; p.23,197.

[Práctica 3: Cinética Enzimática de la Glucosa-Oxidasa] Introducción a la Biotecnología
3
y Peroxidasa (POD), que comprueba la
presencia de peróxido de hidrógeno. De
donde luego ocurren las siguientes
reacciones:
La segunda reacción antes mostrada ocurre
tan rápido que podemos suponer que la
velocidad de aparición de la quinoneimina es
igual a la velocidad de consumo de glucosa y
es igual a la velocidad de aparición de
peróxido de hidrógeno, la velocidad de
aparición de la quinoneimina la mediremos
en el espectrofotómetro de UV visible y de
aquí partiremos para hacer el cálculo de las
demás variables.5
5http://www.uco.es/organiza/departamentos/b
ioquimica-biol-
mol/pdfs/08III%20ESPECTROFOTOMETRÍA.pdf
Murray, Robert; Granner, Daryl; Rodwell, Victor;
Mayes, Peter; 1997; BIOQUÍMICA DE HARPER;
México; Editorial El Manual Moderno; p.99-110.

[Práctica 3: Cinética Enzimática de la Glucosa-Oxidasa] Introducción a la Biotecnología
4
MMÉÉTTOODDOOSS
Materiales utilizados:
Espectrofotómetro de UV visible.
Celda para espectrofotómetro.
Frascos volumétricos de 500ml.
Pipeta graduada de 1 mL.
Pipeta graduada de 10mL.
Perilla de succión.
Reactivos:
Reactivo enzimático (Glucosa Oxidasa y Glucosa Peroxidasa).
Solución de Glucosa.
Agua destilada.
Procedimiento:
Aviso previo a la realización de la práctica:
Se tuvo presente la pureza del reactivo de
trabajo, éste debía encontrarse sin nada que
lo contamine, ya que los oxidantes dan color
al mismo permitiendo el acrecentamiento de
blancos, los reductores disminuyen la
respuesta de color y los detergentes, metales
pesados y cianuros son inhibidores de
enzimas. Evitando todo contacto con la piel y
membranas mucosas.
Preparación de la curva de calibración:
1. Se prepararon soluciones de glucosa anhidra con las concentraciones a continuación: 50, 100, 500, 1000, 2000, 3000, 4000 ppm.
2. En los frascos de uso para el espectrofotómetro, se añadió a 100μL de solución de glucosa, 10ml de reactivo enzimático. Esto se llevó
a cabo para todas las concentraciones que se prepararon en el paso no. 1.
3. En otro frasco de uso en el espectrofotómetro, se preparó una solución de 10 ml de reactivo enzimático con 100μL de agua destilada; éste fue usado para tomar el blanco de la curva de calibración.
4. Se dejó que la reacción transcurriera en un tiempo de 45 min. a T=25ºC, donde se tomaba lectura de la absorbancia para cada concentración en el espectrofotómetro a una longitud de onda de 500nm.
5. Luego transcurridos los 45 min. y haber hecho la toma de datos, se llenó la primera tabla de datos de absorbancia proporcionada.
Obtención de datos para la elaboración de
la curva de cinética química:
1. Nuevamente se prepararon las soluciones “glucosa + reactivo enzimático” y el “blanco” como fue detallado en el procedimiento de elaboración de la curva de calibración. De las soluciones de glucosa-reactivo enzimático se tuvieron que preparar desde la concentración de 50ppm hasta 3000ppm, exceptuando la última de 4000ppm.
2. Para cada concentración preparada, se iba tomando el dato de absorbancia en lapsos de tiempo de 5 min. por lectura hasta llegar a 30 min. y luego una última lectura de absorbancia en 45 min. para luego llenar la segunda tabla de datos de absorbancia dada.

[Práctica 3: Cinética Enzimática de la Glucosa-Oxidasa] Introducción a la Biotecnología
5
CCÁÁLLCCUULLOOSS YY RREESSUULLTTAADDOOSS
Para medir la disminución de la
concentración de la glucosa tomaremos
como base la reacción secundaria de
producción de quinoneimina, que es un
compuesto coloreado de rojo, del cual
podemos medir su concentración en la
solución usando un espectrofotómetro de
absorción de UV visible.
La glucosa es oxidada por la enzima glucosa
oxidasa (GOD) para formar un compuesto
orgánico y peróxido de hidrógeno, luego el
peróxido junto con un tinte incoloro y fenol,
por la acción de la enzima peroxidasa (POD),
son transformados a quinoneimina y agua
(ver sistema de reacciones 1).
Glucosa + 𝑂2 + 𝐻2O 𝐺𝑂𝐷 𝐶6𝐻12𝑂7 + 𝐻2𝑂2
2 H2O2 + Tinte Incoloro + Fenol 𝑃𝑂𝐷 Quinoneimina + 4 𝐻2𝑂
La segunda reacción es casi inmediata por lo
que la velocidad de producción de
quinoneimina está determinada por la
formación de peróxido de la primera
reacción. Por esta razón se puede asumirse
que la velocidad de formación del complejo
coloreado es igual a la velocidad de
formación del peróxido de hidrógeno y esta a
su vez es igual a la velocidad de
desaparecimiento de glucosa (sustrato de la
GOD).
Ahora bien los datos obtenidos son:
Concentración Inicial de Glucosa en
ppm
Absorbancia de la Quinoneimina
0 0 50 0,3676
100 0,396 500 0,5894
2000 1,0434 3000 1,2546 4000 1,5173
Tabla 1: Datos para la curva de calibración.
[G] (ppm)
Datos de Absorbancia
5 min 10
min 15
min 20
min 25
min 30
min 50 0,3620 0,3656 0,3667 0,3670 0,3671 0,3673
100 0,3849 0,3926 0,3939 0,3942 0,3954 0,3954 500 0,5384 0,5811 0,5889 0,5909 0,5917 0,5964
1000 0,9689 1,1076 1,1402 1,1467 1,1480 1,1481 2000 0,9497 1,0298 1,0454 1,0479 1,0482 1,0470 3000 1,0934 1,2275 1,2559 1,2626 1,2646 1,2625
Tabla 2: Datos de absorbancia en el tiempo a diferentes
concentraciones iniciales de glucosa [G].
Podemos calcular la curva de calibración en
términos de la concentración de la
quinoneimina [Q]. Sabemos por
estequiometria que por cada mol que se
produce de quinoneimina, se necesitan 2
moles de peróxido y por tanto 2 moles de
glucosa para formarlo, entonces:
𝑄 =1
2[𝐺]
𝑄 = 1
2
Xo ppm de Glucosa
1000mgg
× 180g de Glucosa
mol
= Xo ppm
360000
mol
Lt (Ec.1)

[Práctica 3: Cinética Enzimática de la Glucosa-Oxidasa] Introducción a la Biotecnología
6
Con esto podemos formar una nueva tabla:
Concentración de la Glucosa
(en ppm)
Concentración Quinoneimina
(mol/Lt) Absorbancia
0 0 0
50 0,000138889 0,3676
100 0,000277778 0,396
500 0,001388889 0,5894
2000 0,005555556 1,0434
3000 0,008333333 1,2546
4000 0,011111111 1,5173
Tabla 3: Datos para la gráfica de la curva de calibración.
Graficando y obteniendo la curva de regresión más ajustada tenemos:
Gráfico 1: Curva de Calibración con la curva de mejor
ajuste.
Ahora tenemos una ecuación para encontrar [Q] a partir de la absorbancia con muy buena aproximación:
𝑄 = −0,002𝑎𝑏𝑠4 + 0,0049𝑎𝑏𝑠3 +0,0045𝑎𝑏𝑠2 − 0,0016𝑎𝑏𝑠 − 9 × 10−06
(Ec. 2)
Entonces con los datos de la tabla 2
obtenemos para cada concentración inicial
de glucosa:
Para Xo de 50 ppm de glucosa:
Concentración Inicial de 50 ppm de Glucosa
Tiempo (min)
Absorbancia de Q
Concentración de Q (mol/Lt)
0 0 -0,000009
5 0,362 0,000189295
10 0,3656 0,000200524
15 0,3667 0,000203995
20 0,367 0,000204945
25 0,3671 0,000205262
30 0,3673 0,000205896
Tabla 4: Variación de la concentración de quinoneimina [Q] en el tiempo para una concentración inicial
de 50 ppm de glucosa [G].
Gráfico 2:
Concentración de Q en el tiempo con la curva de mejor ajuste.
De donde obtenemos la curva de mejor ajuste siguiente:
𝑄 = 2 × 10−10𝑡5 − 2 × 10−8𝑡4 + 7 ×10−7𝑡3 − 1 × 10−5𝑡2 + 8 × 10−5𝑡 − 9 × 10−6
(Ec. 3)
[Q] = -0.0026abs4 + 0.0049abs3 + 0.0045abs2 -0.0016abs - 9E-06
R² = 0.9997
-0.002
0
0.002
0.004
0.006
0.008
0.01
0.012
0 0.5 1 1.5 2
Q (m
ol/
Lt)
Absorbancia
Curva de Calibración de Absorbancia vrs
Concentración Molar de Q
[Q] = 2E-10t5 - 2E-08t4 + 7E-07t3 - 1E-05t2 + 8E-05t- 9E-06
R² = 0.9992
-0.00005
0
0.00005
0.0001
0.00015
0.0002
0.00025
0 5 10 15 20 25 30 35
Q (m
ol/
Lt)
Tiempo (min)
Variación de Q vrs tG inicial = 50 ppm

[Práctica 3: Cinética Enzimática de la Glucosa-Oxidasa] Introducción a la Biotecnología
7
Luego para Xo de 100 ppm de glucosa:
Concentración Inicial de 100 ppm de Glucosa
Tiempo (min)
Absorbancia de Q
Concentración de Q (mol/Lt)
0 0 -0,000009
5 0,3849 0,00026417
10 0,3926 0,000291192
15 0,3939 0,000295846
20 0,3942 0,000296924
25 0,3954 0,000301249
30 0,3954 0,000301249
Tabla 5: Variación de la concentración de quinoneimina [Q] en el tiempo para una concentración inicial
de 100 ppm de glucosa [G].
Gráfico 3: Concentración de Q en el tiempo con la curva de
mejor ajuste.
De donde obtenemos la curva de mejor ajuste siguiente:
𝑄 = −4 × 10−9𝑡4 + 3 × 10−7𝑡3 − 8 ×10−6𝑡2 + 9 × 10−5𝑡 − 7 × 10−6
(Ec. 4)
Luego para Xo de 500 ppm de glucosa:
Concentración Inicial de 500 ppm de Glucosa
Tiempo (min)
Absorbancia de Q
Concentración de Q (mol/Lt)
0 0 -0,000009
5 0,5384 0,00098026
10 0,5811 0,001245819
15 0,5889 0,001297405
20 0,5909 0,001310784
25 0,5917 0,001316153
30 0,5964 0,001347896
Tabla 6: Variación de la concentración de quinoneimina [Q] en el tiempo para una concentración inicial
de 500 ppm de glucosa [G].
Gráfico 4:
Concentración de Q en el tiempo con la curva de mejor ajuste.
De donde obtenemos la curva de mejor ajuste siguiente:
𝑄 = −1 × 10−8𝑡4 + 8 × 10−7𝑡3 − 2 ×10−5𝑡2 + 3 × 10−4𝑡 − 5 × 10−6
(Ec. 5)
[Q] = -4E-09t4 + 3E-07t3 - 8E-06t2 + 9E-05t - 7E-06R² = 0.994
-5E-05
-1E-19
5E-05
1E-04
0.00015
0.0002
0.00025
0.0003
0.00035
0 5 10 15 20 25 30 35
Q (
mo
l/Lt
)
Tiempo (min)
Variación de Q vrs tG inicial = 100 ppm
[Q] = -1E-08t4 + 8E-07t3 - 2E-05t2 + 0.0003t - 5E-06R² = 0.9991
-0.0002
0
0.0002
0.0004
0.0006
0.0008
0.001
0.0012
0.0014
0.0016
0 5 10 15 20 25 30 35
Q (m
ol/
Lt)
Tiempo (min)
Variación de Q vrs tG inicial = 500 ppm

[Práctica 3: Cinética Enzimática de la Glucosa-Oxidasa] Introducción a la Biotecnología
8
Luego para Xo de 1000 ppm de glucosa:
Concentración Inicial de 1000 ppm de Glucosa
Tiempo (min)
Absorbancia de Q
Concentración de Q (mol/Lt)
0 0 -0,000009
5 0,9689 0,004830775
10 1,1076 0,0064844
15 1,1402 0,00688594
20 1,1467 0,006966297
25 1,148 0,006982377
30 1,1481 0,006983614
Tabla 7: Variación de la concentración de quinoneimina [Q] en el tiempo para una concentración inicial
de 1000 ppm de glucosa [G].
Gráfico 5:
Concentración de Q en el tiempo con la curva de mejor ajuste.
De donde obtenemos la curva de mejor ajuste siguiente:
𝑄 = −4 × 10−8𝑡4 + 4 × 10−6𝑡3 − 1 ×10−4𝑡2 + 1,4 × 10−3𝑡 + 3 × 10−7
(Ec. 6)
Luego para Xo de 2000 ppm de glucosa:
Concentración Inicial de 2000 ppm de Glucosa
Tiempo (min)
Absorbancia de Q
Concentración de Q (mol/Lt)
0 0 -0,000009
5 0,9497 0,004612282
10 1,0298 0,005542709
15 1,0454 0,005729074
20 1,0479 0,005759072
25 1,0482 0,005762674
30 1,047 0,005748269
Tabla 8: Variación de la concentración de quinoneimina [Q] en el tiempo para una concentración inicial
de 2000 ppm de glucosa [G].
Gráfico 6:
Concentración de Q en el tiempo con la curva de mejor ajuste.
De donde obtenemos la curva de mejor ajuste siguiente:
𝑄 = −6 × 10−8𝑡4 + 5 × 10−6𝑡3 − 1 ×10−4𝑡2 + 1,4 × 10−3𝑡 + 2 × 10−5
(Ec. 7)
[Q] = -4E-08t4 + 4E-06t3 - 0.0001t2 + 0.0014t + 3E-07R² = 0.9998
-0.001
0
0.001
0.002
0.003
0.004
0.005
0.006
0.007
0.008
0 5 10 15 20 25 30 35
Q (m
ol/
Lt)
Tiempo (min)
Variación de Q vrs t
G inicial = 1000 ppm
[Q] = -6E-08t4 + 5E-06t3 - 0.0001t2 + 0.0014t + 2E-05R² = 0.9977
-0.001
0
0.001
0.002
0.003
0.004
0.005
0.006
0.007
0 5 10 15 20 25 30 35
Q (m
ol/
Lt)
Tiempo (min)
Variación de Q vrs tG inicial = 2000 ppm

[Práctica 3: Cinética Enzimática de la Glucosa-Oxidasa] Introducción a la Biotecnología
9
Luego para Xo de 3000 ppm de glucosa:
Concentración Inicial de 3000 ppm de Glucosa
Tiempo (min)
Absorbancia de Q
Concentración de Q (mol/Lt)
0 0 -0,000009
5 1,0934 0,006310506
10 1,2275 0,007967348
15 1,2559 0,008317459
20 1,2626 0,008399711
25 1,2646 0,008424232
30 1,2625 0,008398484
Tabla 9: Variación de la concentración de quinoneimina [Q] en el tiempo para una concentración inicial
de 3000 ppm de glucosa [G].
Gráfico 7:
Concentración de Q en el tiempo con la curva de mejor ajuste.
De donde obtenemos la curva de mejor ajuste siguiente:
𝑄 = −7 × 10−8𝑡4 + 6 × 10−6𝑡3 − 2 ×10−4𝑡2 + 1,9 × 10−3𝑡 + 2 × 10−5
(Ec. 8)
Para conocer la velocidad de reacción inicial
debemos derivar la expresión obtenida de la
regresión de curva de mejor ajuste y
evaluarla en el tiempo 0, así:
Derivando la Ec. 3: 𝑑 𝑄
𝑑𝑡= 1 × 10−9𝑡4 − 8 × 10−8𝑡3 + 2,1 ×
10−6𝑡2 − 2 × 10−5𝑡 + 8 × 10−5
(Ec. 9)
Después para obtener la velocidad de desaparición de la glucosa hacemos la relación de la estequiometria:
−2 ×𝑑 𝑄
𝑑𝑡=
𝑑[𝐺]
𝑑𝑡
Entonces podemos obtener la siguiente tabla
evaluando para cada tiempo t:
Concentración Inicial de 50 ppm de Glucosa
Tiempo (min)
Velocidad de Q (M/ min)
Velocidad de G -1 x (M/min)
0 0,000080 0,000160
5 0,000223 0,000446
10 0,000420 0,000840
15 0,000633 0,001266
20 0,000840 0,001680
25 0,001033 0,002066
30 0,001220 0,002440
Tabla 10: Velocidad de reacción de aparición de la
quinoneimina [Q] y de conversión de la glucosa [G] en el tiempo para una concentración inicial
de 50 ppm de glucosa [G].
Ahora si graficamos los datos obtenemos:
Gráfico 8: Velocidad de reacción en función de la glucosa
versus el tiempo en minutos.
[Q] = -7E-08t4 + 6E-06t3 - 0.0002t2 + 0.0019t + 2E-05
R² = 0.9991
-0.002
0
0.002
0.004
0.006
0.008
0.01
0 5 10 15 20 25 30 35
Q (m
ol/
Lt)
Tiempo (min)
Variación de Q vrs tG inicial = 3000 ppm
0.0E+00
5.0E-04
1.0E-03
1.5E-03
2.0E-03
2.5E-03
3.0E-03
0 10 20 30 40
r d
e [G
]-1
x (
M/m
in)
Tiempo (min)
Velocidad de Reacción d[G]/dt vrs t[G] inicial = 50 ppm

[Práctica 3: Cinética Enzimática de la Glucosa-Oxidasa] Introducción a la Biotecnología
10
Luego, haciendo lo mismo para las demás
concentraciones iniciales:
Derivando la Ec. 4: 𝑑 𝑄
𝑑𝑡= −1,6 × 10−8𝑡3 + 9 × 10−7𝑡2 − 1,6 ×
10−5𝑡 + 9 × 10−5
(Ec. 10)
Concentración Inicial de 100 ppm de Glucosa
Tiempo (min)
Velocidad de Q (M/ min)
Velocidad de G -1 x (M/min)
0 0,000090 0,000180
5 0,000031 0,000061
10 0,000004 0,000008
15 -0,000002 -0,000003
20 0,000002 0,000004
25 0,000002 0,000005
30 -0,000012 -0,000024
Tabla 11: Velocidad de reacción de aparición de la
quinoneimina [Q] y de conversión de la glucosa [G] en el tiempo para una concentración inicial
de 100 ppm de glucosa [G].
Gráfico 8:
Velocidad de reacción en función de la glucosa versus el tiempo en minutos.
Derivando la Ec. 5:
𝑑 𝑄
𝑑𝑡= −4 × 10−8𝑡3 + 2,4 × 10−6𝑡2 − 4 ×
10−5𝑡 + 3 × 10−4
(Ec. 11)
Concentración Inicial de 500 ppm de Glucosa
Tiempo (min)
Velocidad de Q (M/ min)
Velocidad de G -1 x (M/min)
0 0,000300 0,000600
5 0,000155 0,000310
10 0,000100 0,000200
15 0,000105 0,000210
20 0,000140 0,000280
25 0,000175 0,000350
30 0,000180 0,000360
Tabla 12: Velocidad de reacción de aparición de la
quinoneimina [Q] y de conversión de la glucosa [G] en el tiempo para una concentración inicial
de 500 ppm de glucosa [G].
Gráfico 9:
Velocidad de reacción en función de la glucosa versus el tiempo en minutos.
-5.0E-05
0.0E+00
5.0E-05
1.0E-04
1.5E-04
2.0E-04
0 10 20 30 40
r d
e [G
]-1
x (
M/m
in)
Tiempo (min)
Velocidad de Reacción d[G]/dt vrs t[G] inicial = 100 ppm
0.0E+00
1.0E-04
2.0E-04
3.0E-04
4.0E-04
5.0E-04
6.0E-04
7.0E-04
0 10 20 30 40
r d
e [G
]-1
x (
M/m
in)
Tiempo (min)
Velocidad de Reacción d[G]/dt vrs t[G] inicial = 500 ppm

[Práctica 3: Cinética Enzimática de la Glucosa-Oxidasa] Introducción a la Biotecnología
11
Derivando la Ec. 6:
𝑑 𝑄
𝑑𝑡= −1,6 × 10−7𝑡3 + 1,2 × 10−5𝑡2 − 2 ×
10−4𝑡 + 1,4 × 10−3 (Ec. 12)
Concentración Inicial de 1000 ppm de Glucosa
Tiempo (min)
Velocidad de Q (M/ min)
Velocidad de G -1 x (M/min)
0 0,001400 0,002800
5 0,000680 0,001360
10 0,000440 0,000880
15 0,000560 0,001120
20 0,000920 0,001840
25 0,001400 0,002800
30 0,001880 0,003760
Tabla 13: Velocidad de reacción de aparición de la
quinoneimina [Q] y de conversión de la glucosa
[G] en el tiempo para una concentración inicial
de 1000 ppm de glucosa [G].
Gráfico 10:
Velocidad de reacción en función de la glucosa versus el tiempo en minutos.
Derivando la Ec. 7:
𝑑 𝑄
𝑑𝑡= −2,4 × 10−7𝑡3 + 1,5 × 10−5𝑡2 − 2 ×
10−4𝑡 + 1,4 × 10−3 (Ec. 13)
Concentración Inicial de 2000 ppm de Glucosa
Tiempo (min)
Velocidad de Q (M/ min)
Velocidad de G -1 x (M/min)
0 0,001400 0,002800
5 0,000745 0,001490
10 0,000660 0,001320
15 0,000965 0,001930
20 0,001480 0,002960
25 0,002025 0,004050
30 0,002420 0,004840
Tabla 14: Velocidad de reacción de aparición de la
quinoneimina [Q] y de conversión de la glucosa
[G] en el tiempo para una concentración inicial
de 2000 ppm de glucosa [G].
Gráfico 11:
Velocidad de reacción en función de la glucosa versus el tiempo en minutos.
0.0E+005.0E-041.0E-031.5E-032.0E-032.5E-033.0E-033.5E-034.0E-03
0 10 20 30 40
r d
e [G
]-1
x (
M/m
in)
Tiempo (min)
Velocidad de Reacción d[G]/dt vrs t[G] inicial = 1000 ppm
0.0E+00
1.0E-03
2.0E-03
3.0E-03
4.0E-03
5.0E-03
6.0E-03
0 10 20 30 40
r d
e [G
]-1
x (
M/m
in)
Tiempo (min)
Velocidad de Reacción d[G]/dt vrs t[G] inicial = 2000 ppm

[Práctica 3: Cinética Enzimática de la Glucosa-Oxidasa] Introducción a la Biotecnología
12
Derivando la Ec. 8:
𝑑 𝑄
𝑑𝑡= −2,8 × 10−7𝑡3 + 1,8 × 10−5𝑡2 − 4 ×
10−4𝑡 + 1,9 × 10−3 (Ec. 14)
Concentración Inicial de 3000 ppm de Glucosa
Tiempo (min)
Velocidad de Q (M/ min)
Velocidad de G -1 x (M/min)
0 0,001900 0,003800
5 0,000315 0,000630
10 -0,000580 -0,001160
15 -0,000995 -0,001990
20 -0,001140 -0,002280
25 -0,001225 -0,002450
30 -0,001460 -0,002920
Tabla 15: Velocidad de reacción de aparición de la
quinoneimina [Q] y de conversión de la glucosa
[G] en el tiempo para una concentración inicial
de 3000 ppm de glucosa [G].
Gráfico 12:
Velocidad de reacción en función de la glucosa versus el tiempo en minutos.
Ahora que tenemos las velocidades iniciales
a diferentes concentraciones graficamos el
inverso de las velocidades iniciales de
reacción (1/Vo) vrs la concentración inicial de
sustrato, que en este caso es la glucosa
(1/[G]), para poder obtener los parámetros
del modelo de reacción de Michaelis-
Menten.
[Go] mol/Lt
- Vo M/min
1 / [G] - 1 / Vo
0,000277778 0,000160 3600 6250
0,000555556 0,000180 1800 5555,556
0,002777778 0,000600 360 1666,667
0,005555556 0,002800 180 357,1429
0,011111111 0,002800 90 357,1429
0,016666667 0,003800 60 263,1579
Tabla 16: Inversos de la concentración inicial de glucosa
[Go] y de la velocidad inicial en función de la
glucosa (Vo).
Gráfico 13:
Gráfico de los inversos de velocidad vrs. los inversos de la concentración inicial para obtener
los parámetros de la Michaelis-Menten.
La gráfica parece apegarse a la linealidad de groso modo debido a su varianza de 0,8827. Por tanto podemos suponer que el modelo elegido no dista de la realidad.
-4.0E-03
-2.0E-03
0.0E+00
2.0E-03
4.0E-03
6.0E-03
0 10 20 30 40
r d
e [G
]-1
x (
M/m
in)
Tiempo (min)
Velocidad de Reacción d[G]/dt vrs t[G] inicial = 3000 ppm
y = 1.8196x + 561.4R² = 0.8827
-1,000
0
1,000
2,000
3,000
4,000
5,000
6,000
7,000
8,000
-1000 0 1000 2000 3000 4000
-1/
Vo
1/[G]
1/Vo vrs 1/[G] de la Glucosa-oxidasa

[Práctica 3: Cinética Enzimática de la Glucosa-Oxidasa] Introducción a la Biotecnología
13
Con el intercepto en y (x=0) de la curva de ajuste podemos obtener el valor de la velocidad máxima de reacción:
1
𝑉𝑚= 561,4 => 𝑉𝑚 = 0,00178
𝑀
𝑚𝑖𝑛
Luego con el intercepto en x (y=0) podemos
adquirir el valor de la constante de reacción
de Michaelis-Menten:
−1
𝐾𝑚= −
−561,4
1,8196 => 𝐾𝑚 = 0,00324
Quedando totalmente definido el modelo
para la reacción Michaelis-Menten.
BBIIBBLLIIOOGGRRAAFFÍÍAA
3,4,5 - Murray, Robert; Granner, Daryl; Rodwell, Victor; Mayes, Peter; 1997; BIOQUÍMICA DE
HARPER; México; Editorial El Manual Moderno; p.77-110.
2,4 - Mier, Geraldine; Rhodes, V.J.; Maharg, Leta; Webb, Nancy, S; et al.: BEEF TENDERIZATION
WITH PROTELYITIC ENZYMES; E.E.U.U.; Food Tech; p.16,111; Dairy Sci. Abstracts; p.23,197.
1 - PRODUCTION AND APPLICATION OF ENZYME PREPARATIONS IN FOOD MANUFACTURE;
(Symposium, London,1959); Monograph No.11; Industrial Chemical Society; London.
Páginas de Internet consultadas:
5 - http://www.uco.es/organiza/departamentos/bioquimica-biol-
mol/pdfs/08III%20ESPECTROFOTOMETRÍA.pdf
Consultada el día Jueves 27 de Mayo de 2010 a las 22:49 horas
1,3 - http://www.biosimex.com.mx/pdf/insertos%20dedicados/Quimica%20clinica/
12503%20glucosa.pdf
Consultada el día Sábado 29 de Mayo de 2010 a las 23:56 horas