1DESHIDRATACIÓN DE ALCOHOLES PREPARACIÓN DE CICLOHEXENO
-
Upload
christian-camacho -
Category
Documents
-
view
93 -
download
0
Transcript of 1DESHIDRATACIÓN DE ALCOHOLES PREPARACIÓN DE CICLOHEXENO

LABORATORIO DE QUÍMICA ORGÁNICA II (1411)
SEMESTRE 2013-2
TÍTULO :
“DESHIDRATACIÓN DE ALCOHOLES: PREPARACIÓN DE CICLOHEXENO”
Practica número: 1
INFORME
Autor: Sáenz Hernández Roberto Alfredo
Número de Cuenta: 412068676
__________________
Firma

Informe 1. Roberto A. Sáenz-Hernández. 04, marzo 2012. 2
DESHIDRATACIÓN DE ALCOHOLES: PREPARACIÓN DE CICLOHEXENO
Sáenz-Hernández Roberto A.
Laboratorio de Química Orgánica II (1411), Grupo 03, Sem. 2013-2. Facultad de Química, UNAMAv. Universidad 3000, Ciudad Universitaria, CP. 04510, México, D.F.
RESUMEN
Se preparó el ciclohexeno a partir de ciclohexanol por dos por medio de una destilación fraccionada. Se verificó la presencia de alquenos mediante una reacción con Br2/CCl4 y otra con KMnO4 con una muestra del producto. Se purificó la muestra para posteriormente calcular un rendimiento de 34.96 %.
OBJETIVOS
Se pretende preparar ciclohexeno por deshidratación catalítica de ciclohexanol. Al efectuar una reacción controlando la temperatura, se comprenderá la influencia de este factor en una reacción reversible.
RESULTADOS Y ANALISIS
Tabla 1: Datos de los reactivos y productos
I. Reacción de ciclohexanol y ácido sulfúrico
Se hizo reaccionar 0.0961 mol ciclohexanol midiendo 10 mL de esta sustancia.
|10mLciclohexanol❑ ||0.9624 g
1mL || 1mol100.158 g|=0.0961mol
Se colocaron los 10 mL del ciclohexanol en el matraz pera de dos bocas, al cual también se le adicionó 0.5 mL de H2SO4
cuidadosamente y agitando muy bien.
La destilación comenzó a los 75 °C y se mantuvo la temperatura de destilación entre los 75 -80 °C.
Condiciones Experimentales
Temp. destilación (°C)
Vol. del destilado (mL)
Rendimiento de la reacción
(%)
21 °C, concentraciones conocidas
75 - 85 3.4 34.96
|3.4mL ciclohexeno❑ ||0.8110 g
1mL || 1mol82.143 g|=0.0336mol
Cálculo de rendimiento:
Ciclohexanol Ciclohexeno
Masa molar (g/mol)
100.158 82.143
Densidad (g/mL) 0.9624 0.8110
Punto de fusión o ebullición (°C)
p.e.: 160.84 p.e.: 82.98
Masa (g) 9.624 2.757
Volumen (mL) 10 3.4
Cantidad de sustancia (mol)
0.0961 0.0336

Informe 1. Roberto A. Sáenz-Hernández. 04, marzo 2012. 3
|ExperimentalTeórico |×100 %→|0.0336mol .0.0961mol |×100 %=34.96 %
II. Trampa de permanganato
En el arreglo del equipo, se instaló una trampa de permanganato unida justo antes del colector. La función de la trama es de prevenir la liberación del SO2 tóxico liberado por la descomposición del H2SO4, éste se oxidaba por el permanganato.
III. Pruebas de identificación
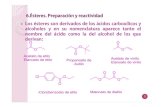
Para comprobar la presencia del ciclohexeno en el producto se efectuaron dos reacciones. Primeramente se adicionó bromo en tetracloruro de carbono como disolvente. Efectivamente se confirmó la presencia de ciclohexeno al observar que la disolución de bromo, originalmente rojiza, tomó un aspecto claro e incoloro. Esto fue debido a la bromación del alqueno presente por medio de un ataque electrofílico del bromo, para primero formar un ion bromonio y posteriormente un alqueno dibromado. Se puede apreciar la reacción por el siguiente mecanismo.
A la vez, se le efectuó otra prueba a otra muestra del producto. Se reaccionaron 1 mL de ciclohexeno y 1 mL de permanganato de potasio 0.2 %. Al ver que la disolución originalmente de color morado se tornó café y turbia, se apreció la presencia del ciclohexeno. Esta prueba es muy común para detectar alquenos ya que es muy simple notar como el permanganato oxida un alqueno; el color café se debe al MnO2 producido.
CONCLUSIONES
La reacción de deshidratación que se realizó es reversible. En la reacción realizada, la sustitución competía con la eliminación. Sin embargo, las reacciones de eliminación son favorecidas a altas temperaturas y también lo son por ácidos cuyas bases conjugadas son pobres nuclófilo, mientras las reacciones de sustitución son favorecidas a bajas temperaturas y por ácidos cuyas bases conjugadas son buenos nuclófilos. Por lo tanto, al conducirse la reacción subministrando calor constante y utilizando ácido sulfúrico como el catalizador, siendo HSO4- un nuclófilo pobre, la síntesis de ciclohexeno por
Teórico: 0.0961 mol 0.0961 molExp.: 0.0961 mol 0.0336

Informe 1. Roberto A. Sáenz-Hernández. 04, marzo 2012. 4
eliminación se favoreció. La destilación fraccionada permitió obtener una pureza más alta del producto deseado. Al condensar el destilado, el producto se removía constantemente del sistema de reacción y por principio de Le Chatelier, también se favorecía la reacción en sentido del producto.
REFERENCIAS
Williamson, K. y Masters, K. (2011). Macroscale and Microscale Organic Experiments. 6a ed. Cengage Learning. Belmont, CA. 131 – 134 pp.
Wade, L, G. (2004). Química Orgánica, Pearson, 5ª ed., México. 248-253 pp.

Espectros de IR.
a) Ciclohexanol
4000.0 3000 2000 1500 1000 605.0
3.910
20
30
40
50
60
70
80
90
100.1
cm-1
%T
3347.12
2935.10 2860.48
2668.41
1714.25
1453.51 1365.22
1299.02
1259.61
1238.99
1174.811139.78
1069.22
1025.52
968.32
925.22
889.53
844.61
789.02
b) Ciclohexeno
4000.0 3000 2000 1500 1000 500 245.0
3.810
20
30
40
50
60
70
80
90
100.0
cm-1
%T
3021.682927.11
2860.042839.50
2659.391654.88
1449.39
1440.19
1385.231324.77
1268.51
1139.62
1039.06
918.89877.40
810.29
719.89
643.34
454.49
405.97