) CIENCIAS - Repositorio CICY: Página de inicio · histología con la finalidad de observar las...
Transcript of ) CIENCIAS - Repositorio CICY: Página de inicio · histología con la finalidad de observar las...

(~ POSGRADO EN
\) CIENCIAS CI CY ( BIOLOCiiCAS
Centro de Investigación Científica de Yucatán, A. C.
Posgrado en Ciencias Biológicas ·
DESARROLLO Y CARACTERIZACIÓN DE UN SISTEMA DE PROPAGACIÓN DE CEDRO ROJO (Cedrela odorata L.) MEDIANTE EMBRIOGÉNESIS SOMÁTICA EN BIORREACTORES DE INMERSIÓN TEMPORAL
Tesis que presenta
ALFREDO DOMINGUEZ HERNÁNDEZ
En opción al título de
MAESTRO EN CIENCIAS BIOLÓGICAS

CENTRO DE INVESTIGACIÓN CIENTIFICA DE YUCATÁN, A. C.
POSGRADO EN CIENCIAS BIOLÓGICAS
RECONOCIMIENTO
CIENCIAS BIOLÓGICAS
Por medio de la presente, hago constar que el trabajo de tesis titulado "DESARROLLO
Y CARACTERIZACIÓN DE UN SISTEMA DE PROPAGACIÓN DE CEDRO
ROJO (Cedrela odorata L.) MEDIANTE EMBRIOGÉNESIS SOMÁTICA EN
BIORREACTORES DE INMERSIÓN TEMPORAL" fue realizado en los laboratorios
de la Unidad de Biotecnología del Centro de Investigación Científica de Yucatán, A.C.
bajo la dirección del Dr. Manuel L. Robert Díaz, dentro de la opción de Ciencias Biológicas
y Biotecnología de plantas, perteneciente al Programa de Posgrado en Ciencias
Biológicas de este Centro.
Atentamente
Dr. Osear A Moreno Valenzuela Director Académico
Mérida, Yucatán, México, 25 de Octubre de 201 1.

DECLARACIÓN DE PROPIEDAD
Declaro que la información contenida en la sección de Materiales y Métodos
Experimentales, los Resultados y Discusión de este documento proviene de las
actividades de experimentación realizadas durante el período que se me asignó para
desarrollar mi trabajo de tesis, en las Unidades y Laboratorios del Centro de Investigación
Científica de Yucatán, A.C., y que a razón de lo anterior y en contraprestación de los
servicios educativos o de apoyo que me fueron brindados, dicha información, en términos
de la Ley Federal del Derecho de Autor y la Ley de la Propiedad Industrial , le pertenece
patrimonialmente a dicho Centro de Investigación. Por otra parte, en virtud de lo ya
manifestado, reconozco que de igual manera los productos intelectuales o desarrollos
tecnológicos que deriven o pudieran derivar de lo correspondiente a dicha información, le
pertenecen patrimonialmente al Centro de Investigación Científica, A.C., y en el mismo
tenor, reconozco que si derivaren de este trabajo productos intelectuales o desarrollos
tecnológicos, en lo especial , estos se regirán en todo caso por lo dispuesto por la Ley
Federal del Derecho de Autor y la Ley de la Propiedad Industrial, en el tenor de lo
expuesto en la presente Declaración.
IBQ. Alfredo Dominguez Hernández

AGRADECIMIENTOS
Agradezco a mis asesores Manuel Luis Robert Díaz y Yuri Jorge Peña Ramírez
por su apoyo incondicional y orientación durante la realización de este trabajo, además
por compartir su conocimiento conmigo y estar al pendiente hasta el final.
. Al Biol. Fel ipe Alonso Barredo Pool y al IBQ. Israel García Sheseña por toda su
ayuda con las técnicas histológicas y la microscopía electrónica de barrido.
A quienes siempre están a mi lado a pesar de estar tan lejos y nunca dudaron que
llegaría a este momento, a mis padres les agradezco todo su amor y cada uno de sus
consejos que me han dado.
A mis compañeros del laboratorio de biorreactores: Miguel , Gastón, Kelly, Juan,
Carlos, y Énder por sus aportaciones y comentarios sobre el trabajo. También a Sara
Murguía por su apoyo tan eficiente en las cuestiones administrativas y de oficina, gracias.
A mis amigos con los que pasamos buenos momentos haciendo aún más divertido
e interesante este camino del posgrado: Max, Ángel, Perfecto, Antonio, Huijara y Martín.
No podía faltar mi estimada lleana gracias por todo, sin tu ayuda no hubieran sido
posibles muchas cosas, entre ellas llegar a este momento culminante, gracias de nuevo.
A Heidy Guadalupe con quien hemos pasado odiseas pero aún seguimos de pie,
gracias por tu cariño y amistad, aquí estoy cuando lo necesites.
A todos mis amigos y compañeros de la comunidad "tengo sed" que de una u otra
forma han colaborado con la realización de este trabajo se los dedico con mucho cariño y
aprecio.

Índice
Índice
ÍNDICE DE FIGURAS ....... .... ............. ......... .. ..... ... .. ....... .. ..... ..... ..... .... ... ..... .. .. ..... ..... .... ..... 11
ÍNDICE DE TABLAS .. .... ........ ... ....... ... .... ..... .. ... ..... .... ... ..... .... .. .... ... .... .. .... ... .... ...... .......... . IV
ABREVIATURAS ...... ... .... ...... .. .... ... ... .. ... ...... ... .. .. .... .. ..... ..... ... ... ... .. ..... .. ...... ... ... ... ...... .. .. .. IV
RESUMEN .... ..... ............... .... .. .. .. ......... .. ... .... ....... .. .......... ..... .. .... ..... .. ... .... ... ... ... .... .. .... ..... 1
INTRODUCCIÓN ......... ... ...... ... ....... ... ....... .... .. .... .... .. .. ..... ..... ...... ... .... .. ..... .... ........ .......... .. . 5
1.1. CEDRO ROJO ....... .. ... ... ... .... ...... .... ... .. ...... .... ..... .... ..... ... ..... .. .... .... .. ...... ....... ..... 7 1.2. BIOLOGÍA DE LA ESPECIE ...... .. ...... .. .. .. .... .... .... .. .. .... .... .. ....... .... ........ .. .. .. .. .. .... 7 1.3. USOS E IMPORTANCIA ECONÓMICA .. ... .. .. ...... .. .. .. .. .. .. .... .. .......... .. ...... ......... .. 8 1.4. PROBLEMÁTICA DEL CULTIVO ...... .. .. ............. .. .. .......... .. .. .... .. ...... .. .. .. .... .. ... ... 9 1.5. LA BIOTECNOLOGÍA COMO ALTERNATIVA PARA EL MEJORAMIENTO VEGETAL .... ....... ...... ........ .... .. .. ... .. ....... ..... ... .. .. ..... .. ....... ..... ..... .. .. ........ ..... .. .... .... ..... ... 11
1.5.1. CULTIVO IN VITRO .. ... .. ... ... ..... .... .... ... ...... ..... .... .. .... ................... ........ .... .. .. 12 1.5.2. EMBRIOGÉNESIS SOMÁTICA (ES) .. .... .... ..... .. .. ...... ...... .. .......... ......... .. .. .. .. 13 1. 5. 3. VÍA DE REGENERACIÓN POR ES .. ...... .... .... .. .. .. .... ........ ... .. .. .... .... ............ 14 1.5.4. TIPOS DE ES ..... .. ..... ...... .. .... .. .. ......... .. ...... ... ... ...... .... ..... .. ...... ......... ........ .... 15 1. 5. 5. FACTORES QUE AFECTAN LA ES .. .. .............. .. ..... .. .. ... .. .... .... .. .. .. ............ . 15 1.5.6. CARACTERISTICAS DE UN EMBRIÓN SOMÁTICO ................ .. ........ ......... 16 1.5. 7. LA ES COMPARADA CON LA EMBRIOGÉNESIS CIGÓTICA. ........... ....... 16
1.6. SISTEMAS DE MICROPROPAGACIÓN .... .. ... ............ .. ...... .. .. .. .. .......... ... ........ 17 1. 6. 1. BIORREACTORES DE INMERSIÓN TEMPORAL .................... ... .... ............ 18 1.6.2. BIORREACTORES DE INMERSIÓN TEMPORAL RITA® ...... .. .. .. .... .. ...... .... 18 1.6.3. FUNCIONAMIENTO DEL EQUIPO .. .... ...... .... ...... ...... .... ... .... ... .... ... .. .. ........ . 19
1.7. ANTECEDENTES DE LA ES EN ESPECIES MADERABLES .. ..... ........ .... .. .... .. 21 1. 7.1. ANTECEDENTES DE LA ES EN CEDRO ROJO .... .... .. .. .......... ...... ........ ... .. 21
2. JUSTIFICACIÓN .... .... ... .... ...... .. ... .. .... .... ..... .... .... ....... .. ..... ... ... .. .... ....... .. ... ...... ...... ... 25
3. OBJETIVOS ..... ... ..... ...... .... .. .... ......... .. ....... ... ....... ....... .. .... .... ..... ... ..... ... .... .. .. .. .... ..... 27
3.1. OBJETIVO GENERAL .. .... .... .... .. .. .... ...... ...... .. .... .... .... .. .. .. .. .. .... .. .. .. ... ..... .... .. .. .. 27 3.2. OBJETIVOS PARTICULARES ...... .. ... .. ......... ..... .. .... .... ........ .. ................ .... ...... 27
4. ESTRATEGIA EXPERIMENTAL ...... .. ...... ..... ...... .. ... ...... ... ... .... .... ... ... ....... .. ..... .... ... . 29
5. METODOLOGÍA .. ... .. ... ..... ..... ....... .... ....... ... .. ......... ....... .... ... ... .... ......... .. ... ....... ....... . 31
5.1. SELECCIÓN Y COLECTA DEL MATERIAL VEGETAL .. ................................... 31 5.2. DESINFECCIÓN DEL MATERIAL VEGETAL ...... .. .... .... .......... .... ......... .. ...... .. .. 31 5.3. EXTRACCIÓN DE LOS EMBRIONES CIGÓTICOS Y ESTABLECIMIENTO IN VITRO .. .... .......... .............. .. ... ......... ........ .. .... .. .. ... ... ........ ... ..... ......... .... ..... ... ... .. ...... ....... 32 5.4. MEDIO DE INDUCCIÓN ... .. ...... .. ...... ...... ... .... ..... ... ........ ...... ...... ... ...... .. ..... .. .... . 32 5.5. ANÁLISIS DE ESTRUCTURAS EMBRIOGÉNICAS .. ... .. ... ...... .. .... .. .. .. .. .... .... .. . 33
5.5.1. ANÁLISIS HISTOLÓGICOS .. .. ..... ..... ...... .. ..... .. .... .. ........ .. ...... .. ... .. ..... ...... .. .. 33 5.5.2. MICROSCOPÍA ELECTRÓNICA DE BARRIDO (MEB). ...... ...... .. .... .......... .. . 34
5.6. ESTABLECIMIENTO DE CULTIVOS EN SISTEMAS DE INMERSIÓN TEMPORAL RITA. ... .... .... ....... .. .... .. ....... ......... ........ .. ....... ... .. ... .. .... ...... .... ... .... ....... ...... 34 5.7. GERMINACIÓN DE EMBRIONES SOMÁTICOS ... ...... .... .. .. .. .... .... .... .. .. .. ......... 35

Índice
6. RESULTADOS ... .......... ... .. ...... ..... ...... .......... ...... .... .... ... ... .. ..... .... ... ........ ....... ..... ..... . 37
6.1. ESTABLECIMIENTO IN VITRO E INDUCCIÓN DE LA EMBRIOGÉNESIS SOMÁTICA ... ...... ........ ........... ....... ... ...... ....... .. .. ... .. ..... ..... .. .......... .... ... .......... ... ........ .... 37 6.2. DESARROLLO DE EMBRIONES SOMÁTICOS Y ANÁLISIS ESTRUCTURAL 39 6.3. PROLIFERACIÓN DE LAS MASAS EMBRIOGÉNICAS EN EL SISTEMA RITA41 6.4. COMPARACIÓN DE EFICIENCIA SISTEMA SEMISÓUDO vs SISTEMA RITA43 6.5. GERMINACIÓN DE EMBRIONES SOMÁTICOS .. ............ .......... .... .. ...... .. .. ...... 45
7. DISCUSIÓN ... .... .... .. ...... ..... ..... ...... ... .... ... ...... ..... ... ... ......... ... ... .... .... .. .. .... .... ... ........ . 47
8. CONCLUSIONES ... ..... .. .... .... .......... .... ... ...... .. .... ..... .... ... .... ....... .. ... ...... .... ............... 51
9. BIBLIOGRAFÍA .. .... ...... ..... .. ... .. ..... ... .... .. ..... ... ..... ...... .' .......... ... .. .... ... ................ .... .... 53
1 O. ANEXO ... .... .... ... ... .... ... .... .. .... .... ...... ....... .. ..... ............ ... ....... ... ... .. ..... ...... ..... ..... ....... 61
ANEXO 1.TABLA DE COMPOSICIÓN DEL MEDIO MS (MURASHIGUE & SKOOG, 1962). 61
Índice de Figuras
Figura 1. Árbol de cedro rojo, hojas, frutos inmaduros, fruto maduro abierto . .. .. ...... .. .... .. .. 8
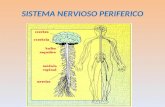
Figura 2. Embriogénesis somática vs embriogénesis cigótica (adaptada de Zimmerman) . ... ... .. .... ..... ....... .. ... ... ....... .. .... .. ... ... .... .. ........... ... .... .. .......... ........ ........ ......... ........ ...... ....... . 17
Figura 3. Flujo de aire en el sistema RITA. Muestra como la entrada y salida del aire es regulado por un electro-válvula de 3 vías, en la inmersión se abre permitiendo el flujo de aire alimentado por la bomba y en la aireación esta se cierra al momento de apagarse el equipo (tomado de VITROPIC S.A, RITA® http://pagesperso-orange. fr/vitropic/rita/es/fonction . htm) ... .. .. .. .... .... ... ....... ... ...... .. ... ... ......... .. .... ........ .......... . 19
Figura 4. Funcionamiento del sistema RITA. 1) Los explantes son colocados en el recipiente sobre la base de poliuretano; 2) es inyectado el aire a una presión de 0,2 bares ascendiendo el medio y desplazando la atmósfera preexistente; 3) los explantes son sumergidos en el medio durante el tiempo programado; 4) pasado el periodo de inmersión la bomba se apaga y la presión del aire disminuye descendiendo el medio (VITROPIC S .A, RITA® http://pagesperso-orange. fr/vitropic/rita/es/fonction . htm) ........ ... ..... ............. . 20
Figura 5. Caracterización de callos proembriogénicos. Tipo A: algodonoso, blanquecino; tipo B: compactos, verde oscuros y de baja velocidad de crecimiento; tipo C: cristalinos, verde claro; tipo D: estructuras amorfas de color café oscuro; tipo E: con apariencia de tejido muerto sin embargo por dentro son viables; tipo F: disgregables, globulares, translúcidos, amarillo claro y con alta velocidad de crecimiento (Dominguez, 2008) .. ...... 23
Figura 6. Fruto, semilla y embrión cigótico de cedro rojo ....... ........ .. .. .... .... .. .... .......... ...... 32
Figura 7. Frutos inmaduros de cedro. Proceso de disección del fruto y embrión cigótico inmaduro extraído en campana de flujo laminar ... ........ .. .. ........ .... .. .... .. .. .. .. ........ .... .. .. .... 37
11

Índice
Figura 8. Callo embriogénico con apariencia friable de color amarillo ........ ................ .... .. 38
Figura 9. Inducción de embriogénesis somática después de 28 semanas. A) callo embriogénico; B) embrión globular-corazón ; C) embrión cotiledonario inicial; D) embrión coti1edonario convertido .......... ... ... .... .. .... ...... .... .. .... ... .. .. ...... .. ..... .. ...... ..... ... .... .... ....... .. .. .. 38
Figura 1 O. Embriones somáticos en proceso desincronizado, presentando varias etapas de desarrollo disgregándose en el medio de cultivo al no tener conexión vascular con el tejido materno .... ..... ...... ...... ... ...... ........ ... ..... ... ........ ........... .. ........ ........ .. ......... .. ...... .. ....... 39
Figura 11. Análisis ultraestructural de embriones somáticos. Escalas: a, b, 100 ¡.Jm, e, h 200 ¡.Jm ... ....... .. ... .. ....... .... ...... ...... ...... .. ... ... ... ............... .... .............. : ... ... .. ......................... 40
Figura 12. Respuesta de los callos bajo diferentes tiempos y frecuencias de inmersión .. 43
Figura 13. Comparación del sistema semisólido vs inmersión temporal. .... ........ .... .. ....... 44
Figura 14. Morfología de embriones somáticos en medio semisólido e inmersión temporal. A) Estructura embriogénica en medio semisólido, B) Embriones en estado cotiledonar en sistema de inmersión temporal. .. ........ .... ...... ............................................ 44
Figura 15. Embrión somático maduro con formación de embriones globulares en la parte radical. .... ..... .. ... .. .. ......... ......... ... ... .. .. ..... ......... ............................................... ... .... ........... 45
Figura 16. Secuencia de germinación de un embrión somático de cedro rojo. A) Embrión somático en estado cotiledonar; B) embrión germinado de cedro rojo ; C) plántula de cedro rojo en invernadero ....... ... ... ... ........ ... ........ .. .. .... ... ........ ..... ......... .. ..... ... ......... ... .. .. ........ ... . 46
111

Índice
Índice de Tablas
Tabla 1. Clasificación taxonómica del cedro rojo .. ...... ..... .... ..... ............................ ........... .. 7
Tabla 2. Características morfológicas del individuo muestreado .... .. .... .. ........ ................ .. 31
Tabla 3. Tiempos y frecuencias de inmersión en el sistema RITA en medio MS líquido sin RCV .... ..... ... ... .. .. ....... ... .. ....... ... ... ...... ... .... .... ...... .. ..... ......... .. ... ........................ .... .. ....... .... 35
Tabla 4. Concentraciones de los RCV empleadas para la maduración y germinación de los embriones somáticos ................. ... ..... ....... ... ... ...... .... ........................... .................... .. 36
Tabla 5. Incremento de biomasa en gramos en los diferentes tiempos y frecuencias de inmersión en sistema RITA con medio MS sin RCV . .. .... ................................ ......... ........ 42
l V
Abreviaturas
Ácido 2,4-diclorofenoxiacetico Ácido 3,6-dicloroanisico Ácido indolacético Ácido indolbutírico Ácido naftalenacético Bencilaminopurina Comisión nacional forestal Cultivo de tejidos vegetales Embriogénesis somática Masa proembriogénica Medio Murashige and Skoog Organización internacional de maderas tropicales Organización de las naciones unidas para la alimentación y la agricultura Recipiente de inmersión temporal automatizado Regulador de crecim iento vegetal Zeatina
2,4-D Dicamba AlA AIB ANA BAP CONAFOR CTV ES MPE MS ITTO
FAO
RITA
RCV ZEA

RESUMEN
Al comienzo del siglo XX Haberlandt propuso que si todas las células de un
organismo tenían la misma información genética que la célula inicial , serían capaces de
volver a expresar el patrón de desarrollo embriogénico hasta formar auténticos embriones
de origen somático. Esta posibilidad se verificó en células del parénquima de ra íz de
zanahoria a finales de los años 50, y desde entonces se ha ampliado a cientos de
especies diferentes. Las primeras especies forestales en las que se logró esta expresión
denominada "totipotencia de las células" fueron Santalum albumen el caso de frondosas
(Rao, 1965), y Picea abies (Chalupa, 1985; Hackman y von Arnold , 1985) y Larix decidua
(Nagmani y Bonga, 1985) en el caso de coníferas. Desde entonces se han regenerado
cientos de especies forestales por embriogénesis somática. Actualmente esta técnica está
siendo aplicada a cultivos tropicales maderables de alta importancia económica, como lo
son algunos miembros de la familia de las Meliáceas entre los que se encuentra el cedro
rojo (Cedrela odorata L.) , segunda especie forestal tropical más importante del mundo
solo después de la caoba (Swietenia macrophyl/a J.), estimada por su madera la cual es
resistente a la putrefacción y a los insectos, la especie se usa en una amplia gama de
productos, incluyendo la construcción y trabajos de gabinete, muebles e instrumentos
musicales, tiene una alta demanda para reforestación y plantaciones comerciales en el
sureste de México.
La presente investigación tuvo como objetivo desarrollar un sistema de
embriogénesis somática en Cedrela odorata, el cual puede ser empleado para la
micropropagación a gran escala así como en estudios de tipo bioquímico, molecular y
anatómico del desarrollo del embrión somático, de la misma forma en aplicaciones de
transformación genética para llevar a cabo mejoras en la planta. El proceso de la
embriogénesis somática fue caracterizado mediante microscopía electrónica de barrido e
histología con la finalidad de observar las estructuras anatómicas y morfológicas del
desarrollo del embrión somático. También se establecieron masas embriogénicas en
sistemas de inmersión temporal RITA® con el fin de acelerar la reproducción y conversión
de una o más etapas del proceso de la embriogénesis somática.
1

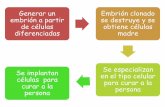
La embriogénesis somática en C. odorata, se indujo de forma indirecta a partir de
masas proembriogénicas, derivadas de embrión cigótico inmaduro después de 24
semanas de cultivo usando medio Murashige and Skoog suplementado con 13.57 IJM de
Dicamba. Mediante análisis histológicos y por microscopía electrónica de barrido de las
masas indiferenciadas, se comprobó la presencia de grupos de células embriogénicas
que pasan por todos los estadios hasta llegar a formar embriones somáticos con una
estructura bipolar sin presentar conexión vascular con el tejido materno. Se logro
incrementar la biomasa en un 300 % después de 4 semanas, usando medio Murashige
and Skoog en el sistema de inmersión temporal RITA® con 3 minutos de inmersión y una
frecuencia de 4 horas. Por otro lado con 1 minuto de inmersión y frecuencia de 4 horas se
observo un mayor desarrollo de los embriones somáticos a estadio cotiledonar.
Este trabajo sienta las bases para la optimización y el escalamiento en
biorreactores para una eficiente propagación clonal, además de la manipulación genética
de esta especie.
2

ABSTRACT
At the beginning of the twentieth century Haberlandt proposed that if all the cells of
an organism had the same genetic information as the initial cell , would be able to re
express the embryogenic development pattern to form authentic embryos of somatic
origin. This possibility was verified in cells of carrot root parenchyma in the late 50's, and
since then has expanded to hundreds of different species. The first tree species was
achieved in this expression called "totipotent cells" were Santalum album in the case of
hardwoods (Rao, 1965) and Picea abies (Chalupa, 1985; Hackman and von Arnold, 1985)
and Larix decidua (Nagmani and Bonga, 1985) in the case of conifers. Since then
hundreds of forest species have been regenerated by somatic embryogenesis. Currently
this technique is being applied to tropical crops of high economic importance of timber, as
are sorne members of the family Meliaceae found between red cedar (Cedrela odorata L.) ,
second largest tropical forest species of the world only after the mahogany (Swietenia
macrophylla J.) , estimated for timber which is resistant to putrefaction and insects, the
species is used in a wide range of products, including construction and cabinet work,
furniture and musical instruments has a high demand for reforestation and commercial
plantation in southeastern Mexico.
The present investigation had the goal to develop a system of somatic
embryogenesis in Cedrela odorata, which can be used for large-scale micropropagation
and studies such as biochemical, molecular or anatomical in the somatic embryo
development, in the same way applications genetic transformation to carry out
improvements at the plant. The process of somatic embryogenesis was characterized by
scanning electron microscopy and histology in order to observe the anatomical and
morphological structures of somatic embryo development. Embryogenic masses were also
established in temporary immersion RITA ® in order to speed up the playback and
conversion of one or more stages of somatic embryogenesis.
Somatic embryogenesis in C. odorata, was induced indirectly from proembryogenic
mass, immature zygotic embryo-derived after 24 weeks of culture using Murashige and
Skoog medium supplemented with 13.57 mM of Dicamba. By histological analysis and
scanning electron microscopy of undifferentiated masses, it was found the presence of
3

----------------------------
embryogenic cell clusters that pass through all stages up to form somatic embryos with a
bipolar structure without vascular connection with the present maternal tissue. Biomass
increase was achieved by 300% after 4 weeks using Murashige and Skoog in the
temporary immersion system with RITA ® 3 minutes of immersion and a frequency of 4
hours. On the other side with 1 minute of immersion and frequency of 4 hours there was a
further development of cotyledonary stage somatic embryos.
This work lays the foundation for optimizing and scaling in bioreactors for efficient
clonal propagation, as well as genetic manipulation of this specie.
4

Introducción
INTRODUCCIÓN
Cedrela odorata Linnaeus (Meliaceae), conocido como cedro o cedro hembra en
español , es la especie del género Cedre/a de mayor importancia comercial y extensión.
Es un árbol del Neotrópico, encontrándose en los bosques subtropical o tropical húmedas
o estacionalmente secas, desde la latitud 26° N en la costa pacífica de México, a través
de la América Central y las Indias Occidentales, hasta las tierras bajas y el pie de los
cerros de la mayoría de la América del Sur hasta una elevación de 1,200 m, con su límite
sureño alrededor de la latitud 28° S en Argentina.
La madera del cedro tiene una alta demanda, debido a que es atractiva,
moderadamente liviana (con un peso específico de 0.4) y su uso primario es para
artículos caseros. El duramen del cedro contiene una resina aromática y repelente a los
insectos que es la fuente de sus nombres populares: cedro, cedro hembra y "spanish
cedar" (su aroma es similar al de los verdaderos cedros, del género Cedrus). La madera
es fácil de trabajar, es resistente a la pudrición en contacto con el suelo como altamente
resistente a las termitas, haciéndola adecuada para la construcción en el exterior. El cedro
tendría un mayor uso si se pudiera cultivar exitosamente en plantaciones (Cintron, 1990).
Cedre/a odorata es una especie forestal tropical que está incluida en la lista de
especies de prioridad por la FAO, razón por la cual, la conservación , estudios de
variabilidad genética, propagación y uso sostenible de esta especie cobra especial
importancia. Esta especie tiene una madera de gran valor en el mercado, y por su
sobreexplotación existen pocas alternativas para recuperar en el corto plazo una riqueza
genética. Por otro lado los intentos para establecer en gran escala plantaciones puras de
cedro han fallado en el país debido al ataque de la plaga Hypsipy/a grande/la (Zeller);
lepidóptero barrenador de yemas, constituye una de las plagas forestales más severas
que reduce el valor comercial de la madera (Cintron, 1990).
Actualmente la carencia de variedades altamente productivas y tolerantes a
factores bióticos y abióticos, en conjunto con la falta de disponibilidad en calidad y
consistencia suficiente para iniciar plantaciones comerciales, constituyen una limitante
para su aprovechamiento comercial a gran escala.
5

Introducción
Los sistemas de regeneración in vitro para la reproducción de plantas basados en
embriogénesis somática además de permitir una reproducción eficiente en otros sistemas
forestales (Jain y col. 1995), constituye la base para la implementación de sistemas
eficientes de transferencia de genes para mejora genética moderna. Esta vía de
regeneración consiste, en la obtención de auténticas semillas somáticas, que tienen su
origen en células somáticas de la planta donante, las cuales se reprograman y siguen un
patrón de desarrollo idéntico al del embrión de origen cigótico. Al nd ser la célula inicial
producto de un proceso de recombinación y fusión de gametos, se conserva íntegramente
el genotipo de la planta donante. Actualmente, esta vía de regeneración cumple con los
requisitos para lograr una óptima propagación vegetativa, y por tanto se considera como
la más adecuada para la micropropagación de especies forestales (Merkle y Dean, 2000;
Sutton, 2002) .
Sin embargo, la producción de plantas clonadas por embriogénesis somática con
fines operativos, tiene que pasar por el desarrollo del cultivo en medio líquido y la
utilización de biorreactores. El cultivo en medio líquido presenta indudables ventajas sobre
el medio semisólido: hay una mayor disponibilidad de los nutrientes y se difunden mejor
los metabol itos excretados por los tejidos. Además, debido a la ausencia de la
interferencia del gelificante, se pueden medir con más facilidad y en forma continua
variaciones en el pH, conductividad , iones, etc., al tiempo que se puede reemplazar por
medio fresco con más facilidad. Sin embargo el cultivo en medio líquido presenta
problemas, como las dificultades de aireación y la inducción de fenómenos de vitrificación
en los tejidos. La técnica de inmersión temporal puede resolver dichos problemas; se ha
comprobado que diferentes frecuencias de inmersión, tienen también efectos de
regulación morfogénica, particularmente en embriogénesis somática (Etienne y Berthouly,
2002). Por ello los sistemas de cultivo en medio líquido utilizando técnicas de inmersión
temporal , se están siendo muy úti les permitiendo el escalamiento de los cultivos.
En este trabajo se llevó a cabo la inducción del proceso embriogénico en Cedrela
odorata y se analizaron los d.iferentes estadios de desarrollo mediante técnicas
histológicas y de microscopia electrónica de barrido. De igual forma se establecieron ®
cultivos en biorreactores de inmersión temporal RITA .
6

Capitulo 1
1. GENERALIDADES
1.1. CEDRO ROJO
El árbol de cedro rojo fue descrito originalmente por Linneo en 1759 en su obra
Sistema Naturae de acuerdo a Cronquist (1981 y 1988) y su clasificación taxonómica esta
descrita en la Tabla 1.
Claslftaclón Tu0fti61Rica
División: Magnoliophyta
Clase: Magnoliopsidae
Sub clase: Rosidae
Orden: Sapindales
Familia: Meliáceas
Género: Cedrela
Especie: Cedrela odorata
Tabla 1. Clasificación taxonómica del cedro rojo.
Cedre/a odorata es una especie tropical maderable que se distribuye en el bosque
tropical perennifolio, tropical subcaducifolio, tropical caducifolio y bosque mesófilo de
montaña (CONAFOR 2000). Su rango de distribución natural va desde el norte de México
(latitud 26° N) hasta Argentina (latitud 28° S), incluyendo el caribe (Styles 1981 , Navarro
1999, CAB 2000) .
En México el hábitat óptimo del cedro rojo se encuentra a altitudes que van desde
los O hasta los 1, 700 metros sobre el nivel del mar, los estados que c~entan con esta
especie de forma natural son: Campeche, Colima, Chiapas, Durango, Guerrero, Hidalgo,
Jalisco, Michoacán, Nayarit, Oaxaca, Puebla, Querétaro, Quintana Roo, San Luis Potosí,
Sinaloa, Sonora, Tabasco, Tamaulipas, Veracruz y Yucatán (FUMIAF, 2005) .
1.2. BIOLOGÍA DE LA ESPECIE
Cedrela odorata L. es un árbol que alcanza los 40 m de altura y un diámetro del
tronco a la altura del pecho (DAP) de 0.6 a 2.5 m. Copa ancha y redonda, con fuste recto,
7

Capítulo 1
corteza externa amarga de color rojizo y fisurada (Figura 1 ). La corteza interna es de color
rosada, posee olor a ajo y sabor amargo. Hojas compuestas, alternas paripinnadas y
grandes, hasta de 1 m de largo, con foliolos de 4.5 a 14 cm opuestos o alternos. Las flores
masculinas y femeninas son de color crema verdoso, se encuentran en la misma
inflorescencia, colocadas en panículas terminales o axilares de 30 a 35 cm.
Los frutos tienen forma de cápsulas de 4 a 7 cm de largo que se abren en cinco
carpelos. En estado inmaduro poseen un color verde y al madurar se tornan café oscuro y
entonces el fruto se desprende liberando las semillas (Figura 1 ). Cada fruto contiene
alrededor de 20 a 25 semillas pequeñas aladas y alargadas, miden de 1.2 a 4 cm de largo
y entre 5 a 8 mm de ancho. El embrión es recto, comprimido, color blanco o crema, ocupa
gran parte de la semilla y tiene dos cotiledones grandes (Salas, 1993; Satis y col. 1999;
Pennington y col. 1998).
Figura 1. Árbol de cedro rojo, hojas, frutos inmaduros, fruto maduro abierto.
1.3. USOS E IMPORTANCIA ECONÓMICA
El cedro rojo es una especie forestal considerada valiosa a nivel internacional
debido a la calidad de su aromática madera, alcanzado altos precios en el mercado
mundial solo detrás de la caoba (Swietenia macrophylla King) (ITTO, 2010).
Tanto la madera como los frutos tienen importancia artesanal para la elaboración
de artículos torneados y esculturas. La madera es apropiada para fabricar elementos no
8

Capítulo 1
estructurales de exteriores e interiores, muebles de calidad y artículos de fantasía y
artesanía (Echenique-Marique y Plumptre, 1990; Anon, 2004). Se utiliza para cajas de
cigarros, roperos y armarios resistentes a los insectos, tablillas para techados, canoas,
lápices (Andrade, 2004), e instrumentos musicales (Ricker y Daly, 1997), en particular
guitarras (INBio, 1999). También se utiliza en aparatos de precisión y como aromatizante
(Andrade, 2004).
Por otro lado de manera de manera empírica y cultural la infusión de las hojas es
usada como medicina para dolor de muelas, oídos y disentería, el tallo es antipirético,
abortivo; el látex es empleado como expectorante contra la bronquitis (FUMIAF, 2005). La
planta ha sido utilizada contra la fiebre y la diabetes (Martins y col. 2003). Se ha
observado una actividad para combatir el paludismo en extractos de madera de C.
odorata (MacKinnon y col. 1997), y ha resultado eficaz en pruebas in vivo (Ornar y col.
2003).
Por su elevado valor comercial, su fácil adaptabilidad y sus efectos restauradores
al medio ambiente, durante los últimos años las plantaciones forestales con cedro rojo
han proliferado en nuestro país. Sin embargo la demanda nacional ha sido creciente
cubriendo sólo un 29% de la demanda demostrando con esto la falta de competitividad del
sector maderero al no poder satisfacer el consumo interno, lo que ha llevado a un
aumento de las importaciones y por lo tanto a una balanza comercial negativa cada vez
más grande en el sector, que para 2007 llegó a ser de 5,593 millones de dólares
(CONAFOR, 2009).
La falta de competitividad del sector se debe a varios factores que tienen que ver
con la baja productividad de los bosques naturales respecto a la productividad que se
obtiene de plantaciones forestales comerciales, incendios, plagas y la tala ilegal,
(Coordinación General De Producción y Productividad, programa operativo anual 2009).
1.4. PROBLEMÁTICA DEL CULTIVO
En 1981 esta especie fue incluida por la FAO en la lista de especies de prioridad,
debido a la creciente escasez ocasionada por su excesivo consumo (Lahera y col. 1995),
de igual forma la especie fue considerada en 1997 por la Union for Nature Conservation
9

Cap ítulo 1
en la red list como especie vulnerable por la tala selectiva (Hilton-Taylor, 2000, IUCN
2004) . Entre los principales problemas que afectan a esta especie podemos destacar:
10
• Sobreexplotación y tala selectiva: esta especie ha sufrido una significativa
sobreexplotación desde hace mas de dos siglos (ITTO 2002; Cavers y col. 2004;
Lamb y col. 2005) y ahora su distribución de forma natural ha disminuido hasta el
punto de que raramente se encuentran grandes árboles de buena forma y tamaño
(Pennington, 1981; Navarro y col. 2004). En donde aún hay selvas, el cedro rojo
está amenazado por la tala selectiva que se enfoca al 90% o más de los árboles
comercialmente aprovechables, reduciendo las densidades poblacionales a casi
cero en escala local y regional.
• Pérdida de diversidad genética: La tala inmoderada de poblaciones naturales
pueden resultar en la pérdida de individuos con características genéticas
deseables (Cornelius y Watt 2003, De la Torre y col. 2008), posiblemente esto
explique por qué los materiales disponibles para restauración o establecimiento de
plantaciones comerciales son altamente susceptibles al ataque de plagas, ya que
la deforestación reduce la diversidad genética de especies a través de la
eliminación de la variación, la interrupción del flujo de genes y el aislamiento
(Bawa y Dayanandan, 1998).
• Prácticas de propagación ineficientes: Por otro lado las prácticas tradicionales
de propagación, para el establecimiento de plantaciones comerciales de esta
especie han evitado incrementar la competitividad y la diversificación del mercado,
por ejemplo la carencia de semillas certificadas que garanticen material elite a los
agriculto'res, para la obtención de más altos rendimientos en la producción de
madera. Pocas han sido las innovaciones tecnológicas introducidas a la fecha para
desarrollar técnicas silvícolas que proporcionen el material para abastecimientos
futuros.
• Ataque de plagas: El ataque de plagas como Hypsipy/a grande/la Zeller (lnsecta:
Pyralidae) también conocido como el barrenador de las meliáceas es una de las
plagas forestales tropicales más estudiadas. Sin embargo, hasta la fecha continúa
siendo el principal obstáculo para el establecimiento de plantaciones comerciales

Capítulo 1
con especies de meliáceas como el cedro rojo (Cornelius y Watt 2003), debido a . que la larva de esta polilla deposita sus huevecillos en los primordios de los
arboles jóvenes destruyendo los tejidos suaves que no están lignificados (Briceño
Vergara, 1997; O'Neil y col. 2001 ; Valera, 1997), generando como consecuencia la
perdida de la dominancia apical y la proliferación de yemas laterales. El ataque de
esta plaga rara vez mata a la planta sin embargo la excesiva ramificación del árbol
imposibilita el uso comercial de su madera, eliminando el valor económico del
árbol (Briceño-Vergara, 1997).
Actualmente, las plantaciones de cedro rojo son sometidas a aplicaciones
intensivas de agroquímicos, sin embargo las personas que aplican estos métodos han sido
víctimas de fuertes intoxicaciones además de aumentar el riesgo de contaminación
ambiental.
Algunos autores han sugerido insistentemente que el mejor camino para combatir
esta plaga puede ser a través de la búsqueda y selección de plantas resistentes a su
ataque mediante un programa de mejoramiento genético de C. odorata (INIFAP, 1997). Se
han observado mecanismos naturales de resistencia sugiriendo la existencia de individuos
de C. odorata con cierto grado de tolerancia en contra del ataque de H. grande/la , lo cual
aumentaría la posibilidad de que individuos tolerantes puedan ser clonados mediante
técnicas biotecnológicas como el cultivo in vitro (Cornelius y Watt, 2003).
1.5.LA BIOTECNOLOGÍA COMO ALTERNATIVA PARA EL
MEJORAMIENTO VEGETAL
El mejoramiento genético de especies forestales usando técnicas tradicionales es
un proceso muy lento debido a sus largos periodos de vida, el tamaño de los arboles, la
recalcitrancia de las semillas, la diversidad genética y la incompatibilidad sexual (Park,
2002) . La biotecnología vegetal y en particular, el cultivo de tejidos ofrecen una amplia
gama de alternativas para resolver estos problemas. Las técnicas de micropropagación
son disponibles para la rápida producción de nuevas variedades y clones para
plantaciones, así como para el rescate de variedades en peligro de extinción. Estas
técnicas también están disponibles para la producción de líneas certificadas sanas la cual
11

Capítulo 1
podría ser considerada como un medio par~ evitar la dispersión de enfermedades. El
implementar técnicas de micropropagación para esta especie sería de gran utilidad.
1.5.1. CULTIVO /N VITRO
El cultivo de tejidos es la ciencia del crecimiento de las células vegetales, tejidos u
órganos aislados de la planta madre en un medio artificial, mediante .la cual se regeneran
plantas llamadas microplantas (George y col. 2008). Es decir, consiste en cultivar
pequeños segmentos de una planta (explante) sobre un medio de cultivo, con el propósito
de regenerar plantas completas, o mantener células desdiferenciadas.
La propagación in vitro fue propuesta por Gottlieb Haberlandt ( 1902) cuando
hipotetizó que puede generarse una planta funcional y completa a partir de una sola
célula, denominando a este evento totipotencialidad de células somáticas, para
rediferenciarse y desarrollar nuevos centros meristemáticos que son capaces de
regenerar una planta normal (Ziv, M. 1999), o que pueden formar tallos, raíces o
embriones somáticos de acuerdo con la competencia que posean y al estímulo que
reciban (Olmos y col. 2004). La regeneración de las plantas puede darse por 2 rutas
morfogénicas:
• Vía Organogénica
Cultivo de yemas o meristemos preexistentes
Regeneración de nuevos brotes por organogénesis
• Vía embriogénica
Inducción de embriones somáticos.
Los primeros dos métodos permiten la formación vía organogénesis de brotes
unipolares y tendrán que ser enraizados en un proceso de múltiples pasos (Thorpe y col.
1991 ). El término organogénesis aplicado al cultivo in vitre de tejidos vegetales se refiere a
la formación de novo de órganos en los explantes cultivados. Entre los órganos que se
pueden formar las raíces, los brotes adventicios, los cuales son estructuras similares a
una yema y tienen la capacidad de originar una nueva planta después de elongarse y
formar las raíces.
12

Capítulo 1
1.5.2. EMBRIOGÉNESIS SOMÁTICA (ES)
La embriogénesis somática (ES) es un proceso en el que una estructura bipolar
(que asemeja a un embrión cigótico) se desarrolla a partir de una célula no cigótica, sin
presentar conexión vascular con el tejido original (Von Arnold y col. 2002). La ES es la
más clara expresión del fenómeno de totipotencia celular enunciado por Haberland en
1902 (citado por Etienne y col. 1999; Solano, 2001 ). La totipotencia, es la capacidad de
las células para formar un nuevo individuo genéticamente idéntico a la célula madre
(Berthouly, 1997).
Desde la primera observación de la formación de un embrión somático en
suspensiones celulares de Daucus carota por Steward y col. (1958) y Reinert (1959), el
potencial de la ES ha sido aplicado a 300 especies de plantas aproximadamente,
pertenecientes a varias familias (Rojas-Herrera y col. 2002).
La ES es una herramienta muy útil para la propagación de plantas y consiste en la
habilidad de las células competentes para cambiar su ruta de diferenciación a fin de
convertirse en embriones somáticos (William y Maheswaran 1986).
En el caso de las dicotiledóneas, un embrión somático es morfológicamente similar
a un embrión cigótico, sobre todo en su desarrollo evolutivo desde proembrión, fase
globular, corazón , torpedo y fase cotiledonar o embrión maduro (Yasuda y col. 2000) .
En los estados iniciales, el suspensor está en menor desarrollo en embriones
somáticos (quizás un reflejo de inutilidad en condiciones in vitre) . Otra diferencia
importante es que el embrión cigótico forma un eje embrional con el meristemo apical
preparándose para la dormancia. Mientras que el embrión somático no sufre desecación
ni dormancia, así la ES se dirige a formar de una célula , una planta sin interrupción
(Merckle, 1990).
Xu y Bewley (1992) con la ayuda de un microscopio electrót:~ico describieron los
contrastantes patrones de desarrollo entre los embriones somáticos y cigóticos,
destacando un desarrollo lento en los estados tempranos y un desarrollo más rápido en
los estados tardíos del embrión somático en comparación con el cigótico; otra diferencia
13

Capítulo I
fue la falta de suspensor bien definido y la formación de múltiples cotiledones mal
desarrollados en embriones somáticos.
Las aplicaciones de la ES son la eliminación viral, propagación clonal ,
conservación de genes, fertilización in vitro, inducción de mutación para diversidad
genética, transformación genética, producción de metabolitos secundarios, cultivo de
protoplastos e hibridización somática (lshii , 1998).
Las principales limitaciones del uso de la ES para la propagación son las bajas
tasas de multiplicación, la producción de variantes somaclonales, la maduración
incompleta, la germinación baja y no sincrónica y el numero bajo de vitroplantas
sembradas en el campo según Merkle (1995).
1.5.3. VÍA DE REGENERACIÓN POR ES
La regeneración de plantas vía embriogénesis somática incluye cinco pasos (Van
Arnold y col. 2002) :
14
a) Iniciación del cultivo embriogénico por cultivo del explante primarioen medio
suplementado con . reguladores de crecimiento vegetal principalmente auxinas
al igual que citocininas.
b) Proliferación del cultivo embriogénico en medio sólido o líquido suplementado
con reguladores de crecimiento en una cantidad similar a la de inicio.
e) Premaduración de embriones somáticos en medio libre de reguladores de
crecimiento vegetal, esto inhibe la proliferación y estimula la formación y el
desarrollo temprano de los embriones somáticos.
d) Maduración de embriones somáticos por cultivo en medio suplementados con
ABA y/o teniendo un reducido potencial osmótico.
e) Regeneración de plantas en medio libre de reguladores de crecimiento.

Capítulo 1
1.5.4. TIPOS DE ES
Los embriones somáticos pueden generarse por dos vías:
• de forma directa a partir de células embriogénicas desarrolladas directamente
del explante (sin la intervención de la fase de callo),
• o de manera indirecta, a partir de tej ido desdiferenciado con desorganizados
ciclos mitóticos no embriogénicos (fase de callo) interpuestos entre el explante
de tejido diferenciado y estructuras embriogénicas reconocidas (Williams y
Maheswaran , 1986; Merkle, 1990).
• La embriogénesis secundaria se refiere al uso de embriones somáticos como
explantes para inducir ciclos repetitivos de embriogénesis, lo que incrementa
las tasas de multiplicación. Tiene la ventaja de ser independiente del explante,
adecuada para la automatización, alta tasa de multiplicación y reproducibilidad
(Vasic y col. 2001 ).
1.5.5. FACTORES QUE AFECTAN LA ES.
El contenido de auxinas y de nitrógeno en el medio de cultivo son generalmente los
factores más importantes en la inducción de la embriogénesis somática. Igual de
importante es la concentración endógena de hormonas del explante, ya que estas influyen
en la capacidad embriogénica. Existen evidencias de que las concentraciones externas de
auxinas o el balance auxinas/citocininas en el cultivo primario de cultivo, es crítico para la
inducción de la actividad mitótica y para la redeterminación epigenética de las células
involucradas en el desarrollo embriogénico. En la mayoría de los casos el regulador de
crecimiento con acción de auxina 2,4-D (2,4-diclorofenoxiacético) es usado en la
inducción de la embriogénesis somática, pero no es el único compuesto utilizado. En el
proceso de embriogénesis somática, generalmente se requieren dos etapas, la de
inducción y la de expresión, la primera con presencia de auxinas y la segunda con bajas
dosis o nula concentración de estas mismas.
15

Capitulo 1
1.5.6. CARACTERISTICAS DE UN EMBRIÓN SOMÁTICO
La característica más distintiva de un embrión somático, es que constituye un
nuevo individuo con estructura bipolar (raíz y brote) capaz de originar una planta
completa. Según Sannasgala (1989), Escalant y Teisson (1989), el embrión somático
presenta las siguientes características:
• Tiene autonomía frente al tejido generador (protegido generalmente por una
epidermis). Histológicamente se plantea que no tiene conexión vascular con el
tejido que le dio origen, por lo que pueden ser separados fácilmente de éste.
• Es una estructura bipolar con un ápice radical, apical y cotiledones.
• Presenta bandas procambiales entre los ápices.
Según Parrott (1993), la inducción del estado embriogénico somático incluye la
inducción de los mismos mecanismos genéticos que conllevan a la embriogénesis
cigótica.
La ES ha sido descrita como un fenómeno muy complicado para el cual la
naturaleza y las características fisiológicas y temporales de los explantes son cruciales
para el éxito. La ES se ha inducido principalmente a partir de explantes como: embriones
cigóticos maduros (Xie y col. 2001; Pinto y col. 2002), brotes epicórmicos (Hernández y
col. 2003), cotiledones y radículas (Tang, 2000) y semillas maduras (Kim y col. 1997;
Murthy y col. 1998).
1.5.7. LA ES COMPARADA CON LA EMBRIOGÉNESIS CIGÓTICA.
La ES es un proceso biológico por medio del cual se obtienen embriones
somáticos a partir de células somáticas. Estos embriones somáticos se desarrollan al
pasar por las fases globular, torpedo y cotiledonar en dicotiledóneas similares a las del
embrión cigótico (Ammirato, 1983). Los embriones somáticos presentan una estructura
bipolar, con meristemos apicales y radicales en extremos en un mismo eje, en donde las
características morfológicas son parecidas a las encontradas en los embriones cigóticos
como se observa en la Figura 2 (Denchev y col. 1992; Abdelnour and Escalant, 1994;
Solano, 2001).
16

Capítulo 1
En el caso de las dicotiledoneas, un embrión somático es morfológicamente similar
a un embrión cigótico, sobre todo su desarrollo evolutivo desde proembrión, fase globular,
corazón , torpedo y cotiledonar o embrión maduro (Yasuda y col. , 2000) , y en
monocotiledóneas pasan por los estados globular, escutelar y· coleoptilar (Gray, 1997).
EMBRIOGENESIS CIGÓTICA
Recweniclón d!" plantas lDmplda~o
<Gemunecioii""~' V
Cre:amtr:nto
Figura 2. Embriogénesis somática vs embriogénesis cigótica (adaptada de Zimmerman).
1.6. SISTEMAS DE MICROPROPAGACIÓN
La micropropagación consiste en la propagación (multiplicación vegetativa) de un
genotipo a gran escala a través del empleo de técnicas de cultivo de tejidos. Esta técnica
es utilizada, en la actualidad, en cientos de laboratorios de todo el mundo para la
producción de millones de plantas de interés comercial.
Micropropagación en medio semisólido: La adición de un gelificante (agar, gelrite,
fitagel , etc) a los medios de cultivos crea un substrato sobre el cual las plantas crecen y
se multiplican. A pesar de las ventajas de la micropropagación como la rápida
propagación, la uniformidad del material clonado y la eliminación de enfermedades, el
hacer uso de los gelificantes, las continuas transferencias a nuevos contenedores y la
mano de obra hacen de éste un proceso caro. Por lo que es necesario desarrollar
métodos alternativos.
17

Capítulo 1
Micropropagación en medio líquido: El cultivo en medio Hquido es considerado como
una solución para reducir los costos de la micropropagación a gran escala . Ofrece varias
ventajas como la eliminación del gelificante, el medio puede ser fácilmente removido, su
esterilización puede ser por filtración, pero su principal desventaja es el alto índice de
vitrificación que produce en los tejidos.
1.6.1. BIORREACTORES DE INMERSIÓN TEMPORAL
Los biorreactores de inmersión temporal son una buena opción para
complementar este método debiendo ser optimizado para cada especie y fase del cultivo.
Su uso podría ser la mejor manera de escalar un proceso de micropropagación,
particularmente de la embriogénesis somática (Etienne y col. 2006). Obteniendo no solo
un eficiente sistema de multiplicación, sino también rápido y económico; debiendo sobre
todo, generar plantas de la mejor calidad que sobrevivan al transplante a condiciones ex
vitro.
El problema de vitrificación (hiperhidricidad) causado por la inmersión continua del
tejido vegetal en el medio líquido puede ser solucionado mediante el método de inmersión
temporal consistente en una fase de inmersión total de los tejidos alternada con otra de
aeración drenando el medio de cultivo.
Los sistemas de inmersión temporal aportan efectos positivos en la
micropropagación durante la proliferación de brotes, microesquejes, microtuberización y
ES, mejorando la calidad de las plantas obtenidas. La duración del tiempo de inmersión y
la frecuencia de la misma, son los parámetros más decisivos para la eficiencia del
sistema. Optimizar el volumen de los nutrientes del . medio y el volumen del contenedor
también mejora la eficacia para la producción de brotes.
1.6.2. BIORREACTORES DE INMERSIÓN TEMPORAL RITA®.
Teisson y col. (1995) diseñaron un "biorreactor de inmersión temporal" al cual
denominaron RITA por sus siglas en francés, este sistema de inmersión temporal
proporciona un manejo simple de las plantas y el medio, además de una nutrición
mejorada debido a que la planta está en contacto con el medio durante la inmersión, y lo
restante de aireación. Hay una disminución de la asfixia en la planta y una renovación
18

Capítulo 1
completa de la atmósfera del cultivo en cada inmersión. Se puede tener control del
proceso morfológico modificando la frecuencia y la duración de la inmersión.
El equipo consta de un vaso que contiene el medio nutritivo y una base de plástico
a media altura con orificios que soporta una esponja de poliuretano donde se colocan los
explantes, además de una conexión vertical que esta al centro del vaso, por la cual entra
y sale el flujo de aire que proporciona la bomba compresora. Este sistema, es
automatizado con el reloj de una computadora que permite la programación de los
tiempos de inmersión y aireación del sistema, mediante un dispositivo de distribución de
aire con una electro-válvula de tres vías que está directamente conectado a la bomba
compresora inyectando un litro de aire por minuto a una presión de 0,2 bar. El aire que
entra en cada biorreactor Rita® está esterilizado por filtros (Figura 3).
--+ INMERSIÓN o I'J !1
l l l lh t
~ ~
Electro·válvula AIREACIÓN de 3 vías '
®Bomba !:?Electroválvula
Figura 3. Flujo de aire en el sistema RITA. Muestra como la entrada y salida del aire es regulado por un electro-válvula de 3 vías, en la inmersión se abre permitiendo el flujo de aire alimentado por la bomba y en la aireación esta se cierra al momento de apagarse el equipo (tomado de VITROPIC S.A, RITA® http://pagesperso-orange.fr/vitropic/rita/es/fonction.htm)
1.6.3. FUNCIONAMIENTO DEL EQUIPO
Una vez instalado el equipo adecuadamente los explantes se colocan sobre el
disco de la esponja de poliuretano y se mantendrá en dos diferentes fases:
19

Capítulo 1
Fase emergida. Esta fase es la de mayor duración donde el explante se mantiene libre del
medio líquido y regularmente las horas dependen de la especie.
Fase sumergida. La duración de esta fase se define por experimentación pero siempre es
corta: Puede variar de 1 minuto por día hasta 4 veces 15 minutos por día.
Una sobrepresión de aire estéril, aplicada en la parte baja del recipiente, permite al
medio de cultivo subir a la parte alta donde se encuentran los explantes. El aire inyectado
permite la oxigenación del medio. Pasado el tiempo de inmersión, la bomba de aire se
apaga. Las presiones se equilibran, y el medio vuelve a bajar por gravedad a la parte
inferior. Por capilaridad, una fina película de medio se mantiene en contacto sobre los
explantes (Figura 4).
Figura 4. Funcionamiento del sistema RITA. 1) Los explantes son colocados en el recipiente sobre la base de poliuretano; 2) es inyectado el aire a una presión de 0,2 bares ascendiendo el medio y desplazando la atmósfera preexistente; 3) los explantes son sumergidos en el medio durante el tiempo programado; 4) pasado el periodo de inmersión la bomba se apaga y la presión del aire disminuye descendiendo el medio (VITROPIC S.A, RITA® http://pagespersoorange. fr/vitropic/rita/es/fonction . htm).
Este biorreactor, que permite además automatizar el sistema, ha sido empleado
con éxito en varios cultivos como el café, caucho, plátano, piña, palma de aceite y cítricos
(Escalant, y col. 1994; Alvard , y col. 1993; Etienne, y col. 1997; Teisson y Alvard, 1998).
20

Capítulo 1
1.7.ANTECEDENTES DE LA ES EN ESPECIES MADERABLES
En especies maderables la ES ofrece ventajas únicas como los más altos
promedios de producción de propágulos por un solo evento de inducción (Pullman y
Johnson 2002; Yildirim y col. 2006), criopreservación de callos embriogénicos (Park,
2002), rejuvenecimiento (Von Aderkas y Bonga, 2000; Ravindra y Nataraja 2007), la
capacidad de producir semillas artificiales (Aquea y col. 2008) y muy marcadamente un
bajo promedio de producción de plantas quiméricas derivadas de experimentos de
transformación genética (Bajaj 1995; Álvarez y Ordás, 2007).
La ES ha sido demostrada en algunos géneros y especies de árboles tropicales
tales como Santalum album, Citrus, Mangifera indica (Jain y col. 1995), y Theobroma
cacao (Maximova y col. 2002).
Entre las especies maderables de origen tropical la ES ha sido reportada para
Eucalyptus (Pinto y col. 2002; Titan y col. 2007), Hevea brasiliensis (Bianc y col. 1999) y
algunos miembros de la familia de las Meliaceas tales como Melia azedarach (Vila y col.
2003; Vila y col. 2007), Azadirachta indica (Shrikhande y col. 1993; Su y col. 1997;
Murthy y Saxena, 1998; Akula y col. 2003; Rout, 2005), Swietenia macrophylla (Maruyama
e lshi , 2009) y Cedrela fissilis (Vila y col. 2009).
1. 7 .1. ANTECEDENTES DE LA ES EN CEDRO ROJO
Hasta la fecha existen algunos reportes en los cuales se ha intentado inducir la
embriogénesis somática en esta especie, como el caso de Muñoz (2003) quien reportó
que el explante que mejor respondió a la inducción de la embriogénesis somática, fue el
entrenudo proveniente de plántulas germinadas in vitro, en medio MS (Murashigue y
Skoog, 1962) con 90.49 IJM de 2,4-D (Ácido 2,4-Diclorofenoxiacético) y 20 mi L-1 de
endospermo líquido de coco, alcanzando un posible estadio globular pero sin llegar a la
formación completa de un embrión somático.
Arellano-Rivas en el 2007 planteó una metodología de propagación para Cedrela
odorata a través de embriogénesis somática y el cultivo de ápices, estableciendo que los
mejores resultados en cuanto a la formación y apariencia de callo embriogénico se
observaron al utilizar 9 1-JM de 2,4-D y 2.25 IJM de cinetina en medio 85 (Gamborg, 1968),
21

Capitulo 1
empleando como explante el cotiledón, donde al igual que en el trabajo anterior, real izado
por Muñoz (2003), se presentaba una cantidad considerable de embriones en etapa
globular pero de igual forma sin desarrollar a las siguientes etapas.
Previamente, nuestro equipo de trabajo reportó (Dominguez, 2008) un protocolo de
ES para C. odorata, en el cual después de hacer una variedad muy amplia de
experimentos con diferentes tipos de explantes (cotiledones, hipocotilos, embriones
cigótico maduros e inmaduros) y RCV's (2,4-D, BAP, Dicamba) se obtuvieron diferentes
tipos de callos como respuesta a las inducciones como se muestra en la Figura 5.
Sin embargo a partir de embriones cigóticos inmaduros, empleando medio MS con
la adición 13.57 1-1M de Dicamba, observamos la inducción de un tipo de callo friable
proembriogénico (Figura 5F) y posteriormente la formación y desarrollo de los embriones
somáticos (Dominguez, 2008; Peña y col. 201 0), en este evento se presentó alrededor de
un 23% de respuesta de los explantes. A las 28 semanas de cultivo se pudo observar la
presencia de todos los estadios de la embriogénesis somática, globular, corazón, torpedo
y cotiledonar, sin embargo los embriones en estado cotiledonar no presentaron desarrollo
de raíces.
Con el objetivo de desarrollar un método eficiente de inducción de ES y la
regeneración de plántulas de embriones somáticos como herramienta para la propagación
clonal , criopreservación y mejoramiento genético, reportamos el establecimiento y la
caracterización de un protocolo para la inducción de la embriogénesis somática y la
regeneración de plántulas de Cedrela odorata.
22

Capítulo!
Figura 5. Caracterización de callos proembriogénicos. Tipo A: algodonoso, blanquecino; tipo B: compactos, verde oscuros y de baja velocidad de crecimiento; tipo C: cristalinos , verde claro; tipo D: estructuras amorfas de color café oscuro; tipo E: con apariencia de tejido muerto sin embargo por dentro son viables; tipo F: disgregables, globulares, translúcidos, amarillo claro y con alta velocidad de crecimiento (Dominguez, 2008).
23

Capítulo 11
2. JUSTIFICACIÓN
A la fecha no existe un protocolo eficiente de regeneración in vitro vía
embriogénesis somática para Cedrela odorata, la conversión. a plántula de los embriones
somáticos en estado cotiledonar reportados por Domínguez en 2008 no se llevó cabo,
tampoco el desarrollo de raíces, por lo anterior proponemos reproducir y establecer un
sistema de regeneración de cedro rojo mediante embriogénesis somática, realizar una
caracterización morfológica del proceso embriogénico por medio de análisis histológicos y
con microscopía electrónica de barrido para observar la formación y conglomeración de las
estructuras embrionarias; al mismo tiempo establecer las mejores condiciones para el
escalamiento del cultivo en sistemas de inmersión temporal; todo esto con miras a futuro
para el mejoramiento genético, propagación masiva y criopreservación de la especie.
25

Capítulo III
3. OBJETIVOS
3.1. OBJETIVO GENERAL
Desarrollar y caracterizar un sistema de propagación de cedro rojo (Cedre/a odorata L.)
mediante embriogénesis somática en biorreactores de inmersión temporal.
3.2. OBJETIVOS PARTICULARES
~ Reproducir el protocolo de inducción de embriogénesis somática en C.
odorata reportado por Dominguez, 2008.
~ Caracterizar morfológicamente el sistema de regeneración a través de
técnicas histológicas y microscopía electrónica de barrido.
~ Generar un eficiente método de propagación mediante embriogénesis
somática en Cedrela odorata.
27

4. ESTRATEGIA EXPERIMENTAL .
Dicamba, ABA, GA3
Selección y colecta de material
Inducción de callo embriogénico
Mantenimiento de embriones somáticos
Multiplicación y desarrollo en biorreactores
\l Germinación de
embriones somáticos
Capítulo IV
.---... Análisis histológico
----t
Análisis por MEB
Tiempo de inmersión
Frecuencia de inmersión
29

Capítulo V
5. METODOLOGÍA
5.1. SELECCIÓN Y COLECTA DEL MATERIAL VEGETAL
Siguiendo las recomendaciones descritas por Longman (1993) la recolección del
material vegetal (frutos inmaduros) se llevo a cabo a partir de un ejemplar elite con
características fenológicas deseables, local izado en poblaciones naturales en el municipio
de Acayucan , Veracruz, México (GPS 18° 02'35.9T'N. 94° 51' 16.44 " W).
Los frutos fueron colectados directamente de un árbol previamente seleccionado
de aproximadamente 1 O años de edad, a los que cuyos parámetros morfológ icos fueron
como lo indica la Tabla 2:
Parámetros Medida Moñológicos (m)
Diámetro a la altura del 1m
pecho (DAP)
Alto del fuste hasta la 1 a 3m
ramificación
Altura 20m
Tabla 2. Características morfológicas del individuo muestreado.
Los frutos contenían alrededor de 15 a 20 semillas en los cuales ya se lograba
distinguir el embrión . Se verificó que las capsulas no presentaran algún tipo de daño
mecánico o hendidura por la cual pudiera ser una vía de contaminación.
5.2. DESINFECCIÓN DEL MATERIAL VEGETAL
Los frutos inmaduros fueron transportados al laboratorio y desinfectados
superficialmente lavándolos en agua corriente con detergente comercial. Posteriormente
los materiales fueron incubados durante tres horas en una solución al 40% (v/v)
preparado a partir de una solución comercial de hipoclorito de sodio al 5.5 % de cloro libre
(Cioralex; Allen), seguido de varios enjuagues con agua destilada desionizada estéri l
(Dominguez, 2008), y llevados a la campana de flujo laminar con la finalidad de abrirlos
bajo condiciones asépticas.
31

Cap ítulo V
5.3. EXTRACCIÓN DE LOS EMBRIONES CIGÓTICOS y
ESTABLECIMIENTO IN VITRO
Una vez que los frutos fueron trasladados a la campana de flujo laminar, se
cortaron longitudinalmente con el bisturí separando los carpelos que contienen a las
semillas, mismas que fueron retiradas con unas pinzas estériles. Para extraer los
embriones, se realizó un pequeño corte en el extremo radicular y aplicando una ligera
presión sobre el lado opuesto para que salga el embrión (Figura 6).
Figura 6. Fruto, semilla y embrión cigótico de cedro rojo.
5.4. MEDIO DE INDUCCIÓN
Los embriones extraídos, se inocularon en el medio de inducción MS (Murashigue
& Skoog, 1962) (ver anexo 1) + 13.57 !JM de Dicamba, 80mM de sacarosa y 0.25%(m/v)
de gelrite para inducir callos embriogénicos. El pH del medio fue ajustado a 5. 7 con
soluciones de KOH 0.2N y HCI 0.1 N, para después, esterilizarlos en un autoclave a 1,46
Kg .cm·2 durante 20 minutos. Los cultivos fueron subcultivados en medio fresco cada 4
semanas. Las condiciones del cuarto de cultivo fueron de 16 horas luz y 8 de oscuridad
climatizado a 27 ± 2°C, con una intensidad lumínica de 70 ¡Jmol M-2 s-1, y una humedad
relativa del40%.
Una vez realizada la inducción después de 9 semanas, los cultivos fueron
analizados y las diferentes estructuras indiferenciadas generadas fueron clasificadas de
acuerdo a su apariencia, color y textura. Solo las estructuras callogénicas que
presentaban la apariencia y similitud con los reportados por Dominguez (2008) , (callos
tipo 4F) , fueron subcultivados en medio fresco cada 3 semanas durante 12 semanas.
32

Capítulo V
5.5. ANÁLISIS DE ESTRUCTURAS EMBRIOGÉNICAS
5.5.1 . ANÁLISIS HISTOLÓGICOS
Para realizar este análisis se tomaron muestras de callos embriogénicos de 9
semanas de cultivo.
• FIJACIÓN.
El fijador FAA: se preparó mezclando 100 mi L-1 de formaldehído, 50 mi/L de Ácido
Acético, 500 mi L-1 Alcohol , y 350 mi L-1 de agua destilada (se preparó el día que se utilizó)
se dividió en viales y se puso en refrigeración a 4°C. Las muestras de tejidos
embriogénicos se colocaron en los viales con solución FAA y se dejaron 4 días, 24 horas
de infiltración a temperatura ambiente y los días restantes a vacío constante a 4°C.
Después de los 4 días se eliminó la solución por decantación y se enjuagó con agua
destilada para eliminar el fijador.
• DESHIDRATACIÓN.
Una vez que se retiró la solución de FAA y se enjuagaron los tejidos y se añadió
una serie de soluciones de etanol de 30%, 50%, 70%, 85%, 96% y alcohol absoluto, 1
hora para cada cambio de solución de etanol al vacío y 4°C., el etanol absoluto se dividió
en dos tiempos de media hora al vacío y 4°C.
• PREINFIL TRACIÓN.
Se retiró completamente el etanol absoluto mediante decantación y con la ayuda
de una pipeta pasteur y se adicionó la resina JB4 (JB-4 Kit de Incorporación, Polyscience)
solución A (JB-4 Embedding monomer) + catalizador (peróxido de benzoilo Plasticized) 48
h. a vacío y 4°C, después se llevó a cabo la infiltración con la resina JB4 solución A +
catalizador+ solución B (JB-4 Embedding) por 4 días.
33

apítuto ================================================================================ ~
• CORTE Y TINCIÓN.
Cuando la resina polimerizó completamente se hicieron cortes de 0.03-0.05 mm en
el micrótomo (Microtome Blades Disposable). Las laminillas se flotan en un cristalizador y
con la ayuda de una pequeña pinza se recogieron en un portaobjetos, secando las
muestras en una placa de calentamiento. Posteriormente se realizó el proceso de tinción
de los portaobjetos con las muestras con 0.05% de azul de toluidina, después de 2 o 3
minutos se enjuagan con agua para eliminar el exceso de colorante; una vez coloreadas
las muestras de azul se contrastó con el reactivo de PAS (Schiff-Ácido Periódico) durante
5 minutos lo que da un color rojo y posteriormente fueron enjuagadas nuevamente con
agua para eliminar el exceso de colorante; finalmente fueron observadas y fotografiadas
con un microscopio Olympus BX42 equipado con una cámara CCD.
5.5.2. MICROSCOPÍA ELECTRÓNICA DE BARRIDO (MEB)
Para realizar estudios ultraestructurales y analizar callos embriogénicos en varios
estadios de desarrollo, los callos embriogénicos fueron colocados en una solución de
fosfatos y deshidratados a través de una serie de concentraciones crecientes de alcohol
(30%, 50%, 70%, 85%, 96% y 100% v/v) , por 60 m in al vacío en un desecador,
posteriormente las muestras se llevaron a punto crítico secándolas a una presión de 1070
psi con C02 (Balzres CPD 020 Critica! Point Dryer; Bai-Tec, Schalksmuhle, Germany) a
una temperatura de -30 oc durante 2 minutos.
El espacio dejado por el etanol es ocupado por el C02 líquido el cual
posteriormente se sublima dejando el espacio celular intacto. Posteriormente las muestras
se colocaron sobre una base con cinta doble adherente para cubrirlas con una capa de
oro (Metalizador Dentan vaccum, Modelo Desk 11) de 120 nm y luego se realizaron las
observaciones la muestra a 10-20 kV utilizando un microscopio electrónico de barrido
Zeiss DSM 940A (Zeiss, Oberkochen, Germany).
5.6. ESTABLECIMIENTO DE CULTIVOS EN SISTEMAS DE
INMERSIÓN TEMPORAL RITA.
Con la finalidad de sincronizar las masas embriogénicas e inducir la germinación
de los embriones somáticos se establecieron cultivos en los biorreactores de inmersión
34

Capítulo V
temporal RITA. Se colocaron aproximadamente 100 mg de tejido (masas embriogénicas)
en los recipientes que contenían 250 mi de medio MS líquido sin RCV, experimentando
con varios tiempos y frecuencias de inmersión (Tabla 3), empleando 2 repeticiones para
cada tratamiento. El material fue incubado en un cuarto en fotoperiodo de 16 horas luz y 8
de oscuridad climatizado a 27±2 °C con una Intensidad lumínica de 70 ¡Jmoi.M-2 s-1 y una
Humedad relativa del 40%. Se espera que las masas embriogénicas se incrementen en
peso y evolucionen en sus diferentes estadios hasta alcanzar una sincronización en el
estado cotiledonar. Los controles serán realizados bajo las mismas condiciones en medio
semisólido.
TIEMPO DE FRECUENCIA DE
INMERSIÓN INMERSIÓN EN HORAS. EN
MINUTOS 2 4 6 8
1 T1 T2 T3 T4
3 T5 T6 T7 T8
Tabla 3. Tiempos y frecuencias de inmersión en el sistema RITA en medio MS líquido sin RCV
De la misma forma que el experimento anterior se realizaron otras pruebas con los
mismos tiempos y frecuencias de inmersión pero empleando el regulador de crecimiento
Dicamba a una concentración de 13.57 IJM (ya que esta fue la concentración con la que
se realizó la inducción de la embriogénesis somática) esperando ver la respuesta de las
masas embriogénicas en su incremento en peso fresco y en la sincronización del cultivo.
5.7. GERMINACIÓN DE EMBRIONES SOMÁTICOS
Para tratar de inducir la germinación de los embriones somáticos se emplearon
concentraciones de ABA y GA3 tal como lo muestra la tabla 4. El medio de inducción fue
el MS, 80mM de sacarosa y 0.25%(m/v) de gelrite. El pH del medio fue ajustado a 5.7 con
soluciones de KOH 0.2N y HCI 0.1 N, para después, esterilizarlos en un autoclave a 1 ,46
Kg .cm-2 durante 20 minutos. Las condiciones del cuarto de cultivo fueron de 16 horas luz y
8 de oscuridad climatizado a 27± 2°C, con una intensidad lumínica de 70 ¡Jmol M-2 s-1, y
una humedad relativa del 40%.
35

Capitulo V
Concentración RCV (IJM)
o 1 3 5
GA3 T1 T2 T3 T4
ABA T5 T6 T? T8
Tabla 4. Concentraciones de los RCV empleadas para la maduración y germinación de los embriones somáticos.
En este experimento se evaluaran la elongación del embrión y la formación de
raíces ya que la conversión de un embrión somático se lleva a cabo cuando el embrión
tiene una apariencia de estructura bipolar, empieza la formación de brotes con hojas
verdaderas, elongación del tallo y de la raíz y la formación de raíces secundarias según lo
describen Litz y Jarret (1991 );
36

Capítulo VI
6. RESULTADOS
6.1. ESTABLECIMIENTO IN VITRO E INDUCCIÓN DE LA
EMBRIOGÉNESIS SOMÁTICA
La metodología de desinfección reportada por Domínguez (2008) para los frutos
inmaduros de cedro fue eficiente debido a que no hubo presencia de microorganismos
contaminates en el proceso de extracción del embrión, ni al momento de su inoculación
en el medio de cultivo. La solución de hipoclorito de sodio al 40% por un tiempo de 3
horas es suficiente para eliminar cualquier amenaza de contaminación. Basado en lo
reportado por Dominguez en el 2008 se llevó a cabo la inducción de la embriogénesis
somática a partir de embriones cigóticos inmaduros de cedro rojo como explantes (Figura
7).
Figura 7. Frutos inmaduros de cedro. Proceso de disección del fruto y embrión cigótico inmaduro extraído en campana de flujo laminar.
La inducción de la embriogénesis somática fue realizada en medio semisólido MS
+ 13.57 !JM de Dicamba obteniendo, después de 9 semanas, masas callosas con
variaciones en color, textura, apariencia y friabilidad. Se observaron estructuras friables
globulares de color amarillo claro, disgregables que se generaron en el tejido materno y
que continuaron en crecimiento (Figura 8). Mientras que otros tipos de callo se
necrosaban y morían. Este tipo de estructuras fueron similares a las reportadas en el
2008 por Dominguez,
37

Capítulo VI
Figura 8. Callo embriogénico con apariencia friable de color amarillo
Figura 9. Inducción de embriogénesis somática después de 28 semanas. A) callo embriogénico; B) embrión globular-corazón ; C) embrión cotiledonario inicial; D) embrión cotiledonario convertido.
En la Figura 9 podemos observar claramente diferentes estadios del desarrollo los
embriones somáticos, en la Figura 9A se observa el explante inicial después de 28
semanas de cultivo en medio MS con Dicamba que empieza a generar estructuras de
38

Capítulo VI
aparitincia disgregable las cualtiS siguen creciendo y separándose del tejido materno con
el paso del tiempo. En la Figura 98 podemos observar la formación de estructuras
globulares claramente disgregables del explante original. En la Figura 9C a las 30
semanas de cultivo se pueden apreciar nuevas etapas del desarrollo de la embriogénesis
somática como son las formas de corazón, torpedo y torpedo cotiledonar, también se
observa una leve apariencia de vitrificación; en la Figura 90 se puede ver la formación de
un embrión somático cotiledonar en proceso de maduración, sin embargo también se
observa la presencia de una nueva formación de estructuras embrionarias secundarias en
la parte que corresponde a la generación de la radícula del embrión somático
6.2. DESARROLLO DE EMBRIONES SOMÁTICOS Y ANÁLISIS
ESTRUCTURAL
Las masas embriogénicas obtenidas fueron analizadas por MEB. En la Figura 11A
donde se logran observar células somáticas en aparente división mitótica, también se
visualiza como forman estructuras que darán lugar a la generación de tejidos. Estas
masas embriogénicas se encuentran en continua división celular, dando lugar al proceso
de embriogénesis somática repetitiva (Merkle y col. 1990) (Figura 1 0), el cual ocurre
cuando los embriones somáticos primarios, en vez de madurar normalmente hasta
plántulas dan origen a ciclos sucesivos de embriones somáticos, que provienen
comúnmente de células superficiales de los cotiledones ó del hipocotilo.
Figura 1 O. Embriones somáticos en proceso desincronizado, presentando varias etapas de desarrollo disgregándose en el medio de cultivo al no tener conexión vascular con el tejido materno.
39

Capítulo VI
Figura 11 . Anál isis ultraestructural de embriones somáticos. Escalas: a, b, 100 ¡Jm, e, h 200 IJm.
40

Capítulo VI
La Figura 11A muestra grupos de células que muestran actividad mitótica (flechas).
La Figura 11 8 muestra una vista más general de A donde se pueden observar múltiples
zonas meristemáticas con activas y continuas divisiones celulares. La Figura 11 C es un
típico embrión globular que presenta la formación de una estructura diferenciada a partir
de agregados celulares que forman el suspensor. En este punto los embriones globulares
comienzan a diferenciarse como lo indica la formación de una capa de células
protodérmicas (p) en la superficie del embrión.
En el panel 11 D se observa la formación de un embrión corazón-torpedo donde se
puede ver que se genera a partir de masas de células isodiamétricas indeferenciadas con
núcleos definidos, citoplasma denso y una típica actividad mitótica de callo embriogénico.
En 11 E se presenta el corte de un embrión con el inicio del desarrollo de estructuras
cotiledonarias, una capa de células protodérmicas y la completa separación del tejido
materno. En la Figura 11 F se muestra el desarrollo de embriones con forma típicas de
corazón a partir de callo embriogénico. Se puede observar la presencia de estructuras
simétricas no fasciadas.
En 11 G se muestra un agregado de células embriogénicas con un desarrollo
asincrónico de embriones en diferentes estadios de desarrollo, desde grupos de células
hasta estructuras cotiledonares. H es una preparación histológica de un brote apical de un
embrión germinado mostrando su tejido conductivo bien diferenciado así como una capa
dérmica.
6.3. PROLIFERACIÓN DE LAS MASAS EMBRIOGÉNICAS EN EL
SISTEMA RITA
Con el fin de incrementar la biomasa, sincronizar los cultivos e inducir la
germinación de los embriones somáticos. Se realizaron experimentos empleando el
sistema de inmersión temporal RITA con medio MS y en ausencia de RCV. En este
sistema se observó lo siguiente: el aumento de la biomasa varía con los tiempos y
frecuencias de inmersión que se manejaron en el sistema, en la tabla 5 podemos observar
que con 1 minuto de inmersión de las masas embriogénicas en el medio líquido y una
frecuencia de inmersión de 4 horas se observa un incremento en el peso fresco después
de 4 semanas en el medio de cultivo. Esto es debido a que las masas proembriogénicas
41

Capítulo VI
se desarrollan principalmente a etapas de torpedo y cotiledonares incrementando su
volumen (Figura 12A). Por otro lado, con 3 minutos de inmersión y una frecuencia de 4
horas la biomasa aumenta hasta 3 veces su peso y volumen después de 4 semanas de
establecido el cultivo (tabla 5), en este punto el cultivo parece sincronizarse mayormente
en estadio globular ya que incrementa el peso pero no se logran observar estadios más
desarrollados (Figura 128).
Con una menor frecuencia de inmersión (cada 2 horas) también se registra un
incremento de biomasa sin embargo es mucho menor en comparación a la que se obtiene
con 1 y 3 de inmersión con frecuencia de 4 horas, en este tratamiento los tejidos
adquieren una apariencia de hiperhidricidad, siendo sensibles y muy frágiles (Figura 12C).
Por otro lado los tejidos con mayor espaciamiento de tiempo entre cada inmersión
presentaron un decremento en el peso de la biomasa (frecuencias de 6 y 8 horas); aquí
los tejidos presentaron características de inanición adquiriendo una apariencia
blanquecina y partes necrosadas (Figura 120).
FRECUENCIA DE INMERSIÓN EN HORAS TIEMPO DE INMERSIÓN
2 4 6 8 EN MINUTOS Peso fresco en mg
1 120 75 80
3 126 90 100
Tabla 5. Incremento de biomasa en gramos en los diferentes tiempos y frecuencias de inmersión en sistema RITA con medio MS sin RCV. ·
42

Capítulo VI
Figura 12. Respuesta de los callos bajo diferentes tiempos y frecuencias de inmersión.
6.4. COMPARACIÓN DE EFICIENCIA SISTEMA SEMISÓLIDO vs
SISTEMA RITA
Al comparar el grado de conversión de los embriones a sus diferentes estadios
(globular, corazón , torpedo, cotiledonar), tanto en el sistema semisólido como con el mejor
tiempo de inmersión temporal donde se alcanzó la mayor sincronización del cultivo (1 min
de inmersión/frecuencia de 3 h) bajo las mismas condiciones de cultivo (medio MS sin
RCV en condiciones de fotoperiodo), podemos observar que existe una significativa
diferencia entre los dos. En medio semisólido existe una mayor proporción de embriones
somáticos en estado globular (Figura 14A) en comparación con el sistema de inmersión
temporal (Figura 13) , pero los estadios más avanzados como el torpedo y cotiledonar se
encuentran en mayor proporción en el sistema RITA que en el semisólido (Figura 148).
43

Capitulo VI
80
70 1/)
60 Q) r::: o 50 ·;: .e
40 E Q)
30 Q) "C
20 ~ o
10
o
L_
cantidad de embriones por estad íos
GLOBULAR CORAZÓN TORPEDO COTILEDONAR
• semisólido
o RITAs
Figura 13. Comparación del sistema semisólido vs inmersión temporal.
Figura 14. Morfología de embriones somáticos en medio semisólido e inmersión temporal. A) Estructura embriogénica en medio semisólido, B) Embriones en estado cotiledonar en sistema de inmersión temporal.
Por otro lado los experimentos realizados con el regulador Dicamba no superaron
los resultados de los experimentos sin RCV (datos no mostrados).
44

Capítulo VI
6.5. GERMINACIÓN DE EMBRIONES SOMÁTICOS
En los experimentos realizados con los RCV ABA y GA3 (1, 3, 5 mg/L) no se logró
la germinación de ningún embrión somático, solo se pudo observar que presentaban una
aparente maduración, ya que los cotiledones tomaron una coloración más verde y se
desarrollan pero la radícula no se desarrolla, se empiezan a generar nuevos ciclos de
división dando lugar de nuevo a embriones en estado globular como lo muestra la Figura
15.
Figura 15. Embrión somático maduro con formación de embriones globulares en la parte radical.
La Figura 15 muestra un embrión somático en estado cotiledonar invidualizado en
medio de cultivo semisólido MS con 3 mg/L de GA3 , aquí se muestra que los cotiledones
están desarrollados sin embargo la parte de la radícula fue sustituida por la formación de
nuevas masas embriogénicas.
Con respecto a la germinación de los embriones somáticos aun no se logra
establecer bien un protocolo , sin embargo nuestro grupo (Peña y col. 201 O) ha obtenido
eventos de germinación como se muestra en la Figura 16.
45

Capítulo VI
Figura 16. Secuencia de germinación de un embrión somático de cedro rojo. A) Embrión somático en estado cotiledonar; B) embrión germinado de cedro rojo; C) plántula de cedro rojo en invernadero.
Estos resultados se han obtenido tratando los embriones somáticos con
concentraciones de 3.8 IJM de ABA, aunque el porcentaje de germinación es muy bajo,
apenas un 12 % de conversión, de las cuales sobreviven el 75 % en el proceso de
transferencia a campo.
46

Capítulo VII
7. DISCUSIÓN
En la actualidad el cedro rojo es la segunda especie forestal tropical más
importante del mundo, existen varias limitantes para su aprovechamiento comercial a gran
escala, entre las que se encuentran la carencia de variedades altamente productivas, la
falta de disponibilidad en calidad y cantidad de materiales para iniciar plantaciones
comerciales y la tolerancia a factores bióticos (ataque del barrenador de yemas) y
abióticos. Para dar solución a estos problemas se requiere de s.istemas de cultivo in vitro,
ya sea para la propagación de las plantas elite producidas, o para regenerar
transformantes que lleven los genes de interés.
La presente investigación tuvo como objetivo general establecer y caracterizar un
sistema de regeneración in vitro de embriones somáticos de Cedrela odorata. Hasta la
fecha no hay reportes de protocolos de regeneración de esta especie vía ES. En nuestro
caso los primeros experimentos estuvieron encaminados a establecer el protocolo
explorando diferentes condiciones para generar embriones somáticos (Dominguez, 2008).
En especies forestales la embriogénesis somática es complicada por las
características fisiológicas y temporales de los explantes los cuales son cruciales para el
establecimiento del cultivo. En nuestro trabajo se utilizaron embriones cigóticos inmaduros
como fuentes de explantes para la inducción de la ES. Existen varios reportes del empleo
de embriones cigóticos inmaduros como principal fuente de explantes para el
establecimiento de protocolos de embriogénesis somática en meliáceas (Shrikhande y col.
1993; Rout 2005; Vila y col. 2007).
Algunas observaciones previas sugieren que la presencia de reguladores del
crecimiento exógenos puede modificar la concentración de los reguladores del
crecimiento endógenos de la planta (Jiménez y Thomas, 2006). La mayoría de los
sistemas embriogénicos requieren una elevada concentración de auxinas, en nuestro
caso se empleó el Acido 3,6-dicloro-2-metoxi-benzoico (Dicamba) el cual ha sido
reportado como iniciador en la inducción de la ES en otras especies tropicales tales como
Eucalyptus grandis (Titen y col. 2007) y E. globulus (Pinto y col. 2002).
47

Capítulo VII
Las estructuras generadas a partir del proceso de inducción sugieren que se trata
de callos proembriogénicos; tanto los embriones cigóticos como somáticos comparten la
misma ontogenia, ambos embriones pasan por los estados globular, torpedo y cotiledonar
para el caso de las especies dicotiledóneas (Ammirato, 1987; Litz and Jarret, 1991 ; Finer,
1994). La observación microscópica reveló que más del 50% del callo genera agregados
de embriones somáticos en todos sus estados de desarrollo.
Por otro lado se observó que existe otro fenómeno en el cual estas masas
proembriogénicas se separan del tejido materno generando más estructuras asincrónicas
desde la etapa globular hasta torpedo, pero que poseen mayor friabilidad que el callo
unido al tejido madre, estas estructuras son de un color amarillo más intenso. Basados en
estos resultados podemos demostrar que el método de inducción reportado por
Dominguez (2008) es reproducible .
La conversión de un embrión somático se lleva a cabo cuando el embrión tiene
una apariencia de estructura bipolar, empieza la formación de brotes con hojas
verdaderas, elongación del tallo y de la raíz y la formación de raíces secundarias según lo
describen Litz y Jarret (1991 ); sin embargo en nuestros experimentos no se llevo a cabo
la elongación de la raíz. Analizando el hecho de que en ninguno de los sistemas de cultivo
se haya observado el desarrollo de raíces probablemente se debió a que inducir el
desarrollo de estas requiere de una relación alta de auxina-citocinina (Villalobos y Thorpe,
1991 ; Salisbury y Ross, 1994). Otros autores han reportado altas concentraciones de ABA
por encima de 98 !JM (Vales y col. 2007) y han evaluado su efecto con algunos
osmoreguladores como el polietylenglicol (Yildirim y col. 2006) o manitol (Uddin y col.
1990; Pullman y col. 2003) y diferentes fuentes de carbón (Bianc y col. 1999; Vila y col.
2007).
Con respecto a la germinación de embriones somáticos se ha reportado que a
bajas concentraciones de GA3 (aproximadamente de 1 mg L-1) se induce la conversión de
ME a plántulas en especies leñosas como el mango, según Laxmi y col. (1999) y en
Azadirachta indica donde se empleó una concentración de 3 mg L-1 (Gyana, 2005). Los
experimentos realizados en nuestro grupo, con los cuales se obtuvieron eventos de
germinación han sido repetidos, pero hasta la fecha no se ha logrado un método eficiente.
48

Capítulo VII
Se ha estudiado que el efecto de algunos reguladores como el hidrolizado de caseína y
endospermo líquido de coco (Rugkhla y Jones, 1998) favorecen el acondicionamiento de
las plantas en condiciones in vitre. Para mejorar las tasas de conversión , puede ser
importante tener en cuenta el momento de la transferencia ex vitre, dado que en algunas
especies se ha observado que la transferencia de los embriones recién germinados
proporciona mejores tasas que las de plantas inicialmente desarrolladas in vitre (Merkle y
Watson-Pauley, 1994).
Otro punto importante es la formación de estructuras globulares en la parte basal
del embrión en estado cotiledonar, lo cual ocurre en muchas angiospermas, sobre todo
cuando los embriones alcanzan este estado de diferenciación, este proceso de
embriogénesis recurrente se basa en la proliferación de la caliptra del embrión somático
primario que genera, tras una meristematización en múltiples zonas de su superficie,
desarrollos embriogénicos secundarios de tipo multicelular (Puigderrajols y col. 1996).
Otros autores opinan que esto ocurre cuando los embriones somáticos primarios no
maduran normalmente hasta plántulas y en lugar de ello dan origen a ciclos sucesivos de
embriones somáticos, que provienen comúnmente de células superficiales de los
cotiledones ó hipocotilo (Merkle y col. 1990).
Para el caso del establecimiento de los cultivos embriogénicos en el sistema de
inmersión temporal RITA, se ha comprobado que diferentes frecuencias de inmersión, con
el estrés ayuno-nutrición que propician , tienen también efectos de regulación morfogénica,
particularmente en embriogénesis somática (Etienne and Berthouly, 2002) . Esta técnica
ha mostrado grandes posibilidades para regular el desarrollo, en medio líquido, de
embriones somáticos de diferentes especies, sincroniza·ndo cultivos, impidiendo la
aparición · de embriogénesis secundaria y estimulando la maduración (Cabasson y col. ,
1997; Etienne Y. col. , 1997).
Vemos que el posible estrés causado por la ausencia de elementos nutritivos,
como en el caso de las masas embriogénicas que estuvieron con 1 minuto de inmersión y
una frecuencia de 8 horas, puede ejercer un efecto negativo en el desarrollo de los
embriones somáticos por inanición, perdiendo peso y tomando una apariencia de tejido
muerto tal como lo menciona Fernández-Guijarro y col. (1994) .
49

Capítulo VIl
Por el contrario los callos embriogénicos que permanecieron con 3 minutos de
inmersión con frecuencia de 2 horas, presentan síntomas de hiperhidricidad (vitrificación)
reflejo del excesivo contacto con el medio liquido, por lo que la entrada de agua a las
células es elevada provocando que se vuelvan transparentes y sensibles al contacto.
De acuerdo a los resultados obtenidos en el sistema de inmersión temporal RITA
(Figura 13), se puede ver que existe una mayor sincronización del cultivo en comparación
con el sistema semisólidó. En el sistema RITA hay un incremento en el número de
embriones en los estados corazón y torpedo dando lugar a una mayor conversión de
embriones a estado cotiledonar (la suma de los estadios corazón, torpedo y cotiledonar da
aproximadamente un 50% de embriones en estadio avanzado) , en cambio en el
semisólido el grado de avance en sus estadios es menor ya que existe un incremento en
la formación de embriones en estado globular siendo menos los embriones que alcancen
el siguiente estadio de desarrollo (embriones en etapas corazón, torpedo y cotiledonar
suman solo un 30% mientras globulares son un 70%). A pesar de lograr obtener un
tiempo de inmersión/aireación en el cual se incrementa la biomasa y otro donde se
desarrollen los embriones hasta etapa cotiledonar, no se observó el desarrollo de raíces
funcionales.
En los sistemas de inmersión temporal el periodo de inmersión es muy importante
porque determina la absorción de los nutrientes y el control de la hiperhidricidad. Los
tiempos varían considerablemente dependiendo de la especie por ejemplo 1 hora de
inmersión con una frecuencia de 6 horas fueron necesarios para la eficiente tuberización
de la papa, pero en cambio para café y el árbol de goma solo basto 1 minuto de inmersión
por cada 12 horas de aireación para la estimulación de la embriogénesis somática como
lo reportan Etienne y col. (1997a, b). El desarrollo de un eficiente protocolo de
regeneración de embriogénesis somática para C. odorata es necesario para la
transferencia de genes de resistencia a insectos, tolerancia a estrés abiótico, velocidad de
crecimiento, ganancia de biomasa, todos ellos elementos clave para el mejoramiento
genético de esta especie que podrían permitir el establecimiento de plantaciones
comerciales para la producción de madera. Con estas acciones se podría aliviar la presión
de la tala inmoderada sobre las poblaciones naturales, la cual es la meta para la
conservación y proliferación de la diversidad genética.
50

Capitulo VIII
8. CONCLUSIONES
Se determinó que la desinfección de los frutos inmaduros debe llevarse a cabo
incubándolos durante tres horas en una solución al 40% (v/v) preparado a partir de una
solución comercial de hipoclorito de sodio al 5.5 % de cloro libre (Cioralex; Allen), seguido
de varios enjuagues con agua destilada desionizada estéril.
Se desarrolló un protocolo reproducible para la inducción de la ES a partir de
embriones cigóticos inmaduros de C. odorata con la adición de 3 mgl-1 de Dicamba
(13.57 IJM) al medio de cultivo MS.
Se caracterizó el proceso de ES mediante estudios histológicos y por microscopía
electrónica de barrido determinando los estadios de desarrollo de los embriones
somáticos.
Se obtuvieron eventos de germinación de los ES en medio MS con
concentraciones de 3.8 1JM de ABA después de 4 semanas de cultivo, obteniendo un 12%
de conversión y un 75% de sobrevivencia a campo.
Se establecieron cultivos en el sistema de inmersión temporal RITA sincronizando
el desarrollo de los embriones en estadios avanzados (corazón, torpedo, cotiledonar 50%
en comparación con el sistema semisólido donde solo el 30% alcanzan estas etapas) , con
un tiempo de 1 minuto de inmersión y una frecuencia de 4 horas en un periodo de 4
semanas, en medio MS basal sin reguladores.
Con el sistema de inmersión temporal RITA se logró un aumento en biomasa de
aproximadamente un 300 % de proliferación , con un tiempo de 3 minutos de inmersión y
una frecuencia de 4 horas en un periodo de 4 semanas, en medio MS basal sin
reguladores.
51

Capítulo IX
9. BIBLIOGRAFÍA
Abdelnour, A. ; Escalant, J. 1994. Conceptos básicos del cultivo de tejidos vegetales.
CATIE, Turrialba, Costa Rica. 38 p.
Aitken-Christie, J. y H.E. Davies. 1988. Development of semi-automated propagation
system. Acta Hort. 230:81-87.
Ammirato, P.V. 1987. Organizational events during somatic embryogenesis. Plant Tissue
and Cell Culture. Alan R. Liss. New York.
Andrade T. A., 2002. Micropropagación de cedro rojo (Cedrela odorata L.) como
herramienta para su manejo. Programa de Agroecosistemas Tropicales, Colegio de
Postgraduados, Campus Veracruz.
Andrade T. A., 2004. Capacidad morfogenética de diferentes explantes de cedro rojo
(Cedre/a odorata L.). Tesis de Maestría en Ciencias. Veracruz: Colegio de Postgraduados,
Campus Veracruz.
Arellano, R. A. 2007. Cultivo in vitro de cedrela odorata L. Tesis de licenciatura, facultad
de ciencias, UNAM. México.
Attree, S. M. and Fowke, L. C. 1993. Embryogeny of gymnosperms advances in
synthetic seed technology of conifer. Plant Cell Tiss. Org. Cult. 35: 1-35.
Berthouly M. and Etienne H. (1999). Somatic embryogenesis of coffee. In : Jain SM,
Gupta PK and Newton RJ (eds) Somatic Embryogenesis in Woody Plants, Vol. 5 pp259-
288. Kluwer Academic Publishers, Great Britain .
Berthouly, M. 1997. Biotecnologías y técnicas de reproducción de materiales promisorios
en Coffea arabica. EN: Memorias del XVII Simposio latinoamericano de Caficultura.
Heredia, Costa Rica. pp 25- 49.
Biondi, S. and Thorpe, T. 1981. Clona! Propagation of Forest Tree Species. COSTER
Symp. On Tissue Culture of Economically lmportants Plants. Ed A.N. Rao. p 197-202.
Singapore
53

Capítulo IX
Cabasson C, Alvard D, Dambier D, Ollitrault P and Teisson C (1997) lmprovement of
Citrus somatic embryo devolopment by temporary immersion. Plant Cell , Tissue and
Organ Culture 50:33-37
Capó,M. and S. Sanchez.1992. Las actividades forestales y su impacto en el
ecosistema. Departamento forestal UAAAN y colegio de postgraduados, Chapingo México.
Pp 153-160.
Carpineti L. 2005. Importancia de la silvicultura clonal. ldia XXI 8:153-156.
Celestino, C. l. Hernández, E. Carneros, D. López-Vela y M. Toribio. 2005. La
embriogénesis somática como elemento central de la biotecnología forestal. Investigación
agraria. Sistemas y recursos forestales, ISSN 1131-7965, Vol. 14, N° 3. Págs. 345-357.
Chalupa V., 1985. Somatic embryogenesis and plantlet regeneration from cultured
immature and mature embryos of Picea abies (L.) Karst. Comm lnst For 14, 57-63.
Comisión Nacional Forestal (CONAFOR) 2001 . Programa para el desarrollo de
plantaciones forestales comerciales (PRODEPLAN).
Comisión Nacional Forestal (CONAFOR) 2005. Manual practico para la producción de
plantas. 197p.
CONAFOR, 2000. Ficha técnica de Cedre/a odorata L. , Comisión Nacional Forestal.
México. 6p.
Cronquist, A. 1981. An integrated system of classification of flowerings plants. Columbia
University Press., Nueva York.
Cronquist, A. 1988. The evolution and classification of flowering plants. 2a edición. New
York botanical garden, Bronx.
Cuenca, B., San José M. C., Martínez M. T., Ballester A., Vieitez A. M., 1999. somatic
embryogenesis from stem and leaf explants of Quercus robur l. plant cell rep 18, 538-543.
54

Capitulo IX
Denchev P, Kuklin A and Scragg A. 1992. Somatic embryo production in bioreactor.
Journal of Biotechnology 26: 99-109.
Domínguez H. A. (2008). Desarrollo de un metodo de propagación masiva de plantulas
de cedro rojo (Cedrela odorata L.) por medio de embriogénesis somática empleando
biorreactores de inmersión temporal RITA®. Tesis de licenciatura CICY. Mérida Yucatán.
Edwin F. George; Michael A. Hall; Geert-Jan De Klerk. 2008. Plant Propagation by
Tissue Culture 3rd Edition, 1-28. Springer
Etienne H, Lartaud M, Michaux-Ferriere N, Carron P, Berthouly M and Teisson C
(1997 8) lmprovement of somatic embryogenesis in Hevea brasi/iensis (Mull Arg) using
the temporary immersion technique. In Vitro Cell. Dev. Biol. 33:81-87.
Etienne H., Berthouly M., 2002. Temporary immersion systems in plant
micropropagation. Plant Cell Tissue Org Cult 69, 215-231
Etienne,H., Bertrand,B., Anthony,F., Cote,F., Berthouly,M. 1997A, L'embryogénése
somatique, un outil pour l'amélioration génétique du caféier, ASIC, Nairobi
Etienne-Barry D, Bertrand B, Vasquez N and Etienne H (1999) Direct sowing of Coffea
arabica somatic embryos mass-produced in a bioreactor and regeneration of plants. Plant
Cell Reports 19:111-117.
Fernández-Guijarro, B., Celestino C., Toribio M., 1994. Somatic embryogenesis in
Quercus suber L. En: Biotecnology of Trees (Pardos J.A., Ahuja M.R., Elena Rossello R. ,
eds). Investigación Agraria. Sistemas y Recursos Forestales. Fuera de Serie n.0 4. INIA.
Madrid, EspaAa. pp. 105-110.
Fernandéz-Guijarro, B; Celestino, C and Toribio, M. 1995. lnfluence of Externa! Factors
on Secundary Embriogenesis and Germination in Somatic Embrios from Leaves of
Quercus suber Plant Cell, Tissue and Organ Culture. Kliwer Academic Publisher. 41 : 99-
106. Netherlands.
55

Capitulo IX
Fundación Mexicana para la investigación Agropecuaria y Forestal, A.C. Plan de
Negocios para el cu ltivo de la especie forestal comercial Cedro Rojo (Cedrela odorata L. )
en México. Noviembre de 2005.
Grijpma, P. 1976. Resistance of Meliaceae against the shoot borer Hypsipy/a with
particular reference to Toona ci/iata M. J. Roem. var australis (F v M) C.D. C. In: J. Burley y
B.T. Styles (eds.). Tropical trees, variation , breeding and conservation . l,.ondon. Linnean
Society Symposium. Series Number 2. pp. 69-78.
Hackman 1. , Von Arnold S., 1985. Plantlet regeneration through somatic embryogenesis
in Picea abies (Norway spruce). J. Plant Physiol121, 149-158.
INIFAP-SAGAR, 1997. Combate biológico del barrenador de brotes en plantaciones de
Cedro Rojo y Caoba. En Tecnologías Llave en Mano División Forestal. México D.F. , pags.
149-150.
Inventario Forestal Nacional, 2000. Investigaciones Geográficas, Boletín del Instituto de
Geografía, UNAM, Número 43, 2000, pp. 183-203. La condición actual de los recursos
forestales en México.
Lahera W.; Álvarez A. and Gómez S. 1995. Estado del Programa de mejoramiento
genético de Cedrela odorata L. Desarrollado en Cuba. Recursos Genéticos Forestales No
22. FAO. p 27-28. Roma- Italia.
Litz, R.E y Jarret, R.L. 1991. Regeneración de plantas en el cultivo de tejidos:
embriogénesis somática y organogénesis. En: Cultivo de tejidos en la agricultura:
Fundamentos y aplicaciones. Roca, W. M y Mroginsky L. A (eds). CIAT (Centro
Internacional de Agricultura Tropical). Cali , Colombia. pp 143-173.
Maene L., Debergh P. (1985) Liquid medium additions to established tissue cultures to
improve elongation and rooting in vivo. Plant Cell Tissue Organ Cult. 5:23-33.
Maruyama, E., l. Kinoshita. lshi, H. Shigenaga, K. Ohba and A. Saito. 1997. Alginate
encapsulated technology for the propagation of the tropical forest trees: Cedrela odorata
56

Capítulo IX
L. , Guzuma crinita mart. and Jacaranda momosaefolia D. Don silvae genetica, 46(1): 17-
23.
Maruyama, E.; lshii, K.; Saito, A. and Migita, K. 1989. Micropropagation of Cedro
(Cedrela odorata L) by Shoot-Tip Culture. Journal of Japanese Forestry Science Society
71 :329-3Japon.
Maruyama, E.; lshii, K.; Saito, A. and Migita, K. 1989. Micropropagation of Cedro
(Cedre/a odorata L) by Shoot-Tip Culture. Journal of Japanese Forestry Science Society
71 :329-3Japon.
Marzocca, A. 1985. Nociones básicas de taxonomía vegetal Instituto Interamericano de
Cooperación para la Agricultura. San José.
Merkle S.A., Dean J.F.D., 2000. Forest tree biotechnology. Current Opinion Biotech 11 ,
298-302.
Merkle S.A., Watson-Pauley B.A., 1994. Ex vitro conversion of pyramid magnolia
somatic embryos. Hort-Science 29, 1186-1188
Merkle S.A., Wiecko A.T., Sotak R.J., Sommer H.E., 1990. Maturation and conversion of
Liriodendron tulipifera somatic embryos. In Vitre Cell Dev Biol26, 1086-1093.
Muñoz, T. S., 2003. Embriogénesis somática en Cedro rojo (Cedre/a odorata L.) a partir
de cotiledones. Tesis de licenciatura. CIRGEBV, Lima, Perú.
Murashige, T; Skoog, F. 1962. A revised medium for rapid growth and bioassays with
tobacco tissue culture. Physiologia Plantarum 15:53-58
Nagmani R., Bonga J.M., 1985. Embryogenesis in subcultured callus of Larix decidua.
Can J ForRes 15, 1088-1091 .
Newton, A. C. 1990. Selección por resistencia al perforador de las meliáceas. Noticiero
(5). Mejoramiento genético y semillas forestales para América Central. Turrialba. Costa
Rica. CATIE.
57

Capitulo IX
Newton, A. C. Baker P., Ramnarine S., Mesén F. y Leakey, R.R.B. 1993. Mahogany . .
shoot borer: prospects for control. Forest Ecology and Management.
Olmos S., Lucciani G. y Galdeano E. Micropropagación. [ed.] Rubinstein C.y Mroginski
L. Echenique V. Biotecnología y Mejoramiento Vegetal. s.l. : INTA, 2004, págs. 163-172.
Patiño, F. 1997. Recursos Genéticos de Swietenia y Cedrela en los Neotrópicos.
Propuestas para Acciones Coordinadas. Organización de las Naciones Unidas para la
Agricultura y la Alimentación . Roma-Italia. p 58.
Peña R. Y., García S. 1., Hernández E. A., Domínguez H. A., Barredo P. F. A.,
González R. J. A., Robert D. M. L., 201 O. lnduction of somatic embryogenesis and plant
regeneration in the tropical timber tree Spanish red cedar [Cedrela odorata L.
(Meliaceae)] . Plant Cell Tiss Organ Cult.
Pérez, F. J. 2001. Desarrollo de un método de micropropagación aplicable a genotipos
selectos de Cedrela odotata L. Tesis Mag. Se. CATIE, Turrialba, Costa Rica . 81 p.
Preece J.E., 1995. Can nutrient salts partially substitute for plant growth regulators? Plant
Tissue Cult Biotech 1, 26-37.
Pullman GS, Johnson S, Peter G, Cairney J, Xu N (2003) lmproving loblolly pine
somatic embryo maturation: comparison of somatic and zygotic embryo morphology,
germination, and gene expression. Plant Cell Rep 21 :747-758
Ramage C.M., Williams R.R., 2002. Mineral nutrition and plant morphogenesis. In Vitre
Cell Dev Bici Plant 38, 116-124
Rao P.S., 1965. In vitro induction of embryonal proliferation in Santalum album (L.)
Phytomorphology 15, 175-179.
Rugkhla A., Jones M. G. K., 1998. Somatic embryogenesis and plantlet formation in
Santalum album and S: spicatum. J Exp Bot 49, 563-571
Salas Estrada, J. B. 1993. Arboles de Nicaragua. Nicaragua, Managua, Instituto
Nicaragüense de Recursos Naturales y del ambientes, IRENA. 390 P.
58

Capítulo IX
Solano, W. 2001 . Efecto de las Características de Cultivo en Suspensión Celular y en
Biorreactor con Inmersión Temporal sobre la Propagación masiva de Coffea arabica por
Embriogénesis Somática. Tesis Licenciatura en Ingeniería en Agronomía con énfasis en
Fitotecnia. Turrialba, Costa Rica. Universidad de Costa Rica . 87 p.
Sutton W.R.J. , 2000. Wood in the third millennium. Forestry Prod J 50, 12-21 .
Tautorus, T.E., L.C. Fowke, and D. l. Dunstant. 1991 .Somatic embryogenesis in conifers.
Canadian Journal of Botany 69-1873-1899.
Teisson, C. and Alvard, D. A new concept of plant in vitre cultivation liquid medium:
Temporary immersion .. [ed .] M Terzi y col. En : Current lssues in Plant Molecular and
Cellular Biology. s.l. : Kluwer Academic Publishers, Dordrecht, The Net, 1995, págs. 105-
110.
Thorpe, T. 1991 . Introducción al Cultivo de Tejidos y Biotecnología Vegetal. Resúmenes
del curso Técnicas y Aplicaciones de Biotecnología en Especies Forestales. (ed) Villegas
Leopoldo. Corporación Andina de Fomento. Caracas. Venezuela. pp 91 -107.
Tisserat, B. & Vander~ook, C.E. (1986) Computerii:ed-long term tissue culture for
orchids. Amer. Orch. Soc. Bul. 55: 35-42.
Tullume, C. 2000. Características anatómicas y propiedades físico mecánicas del Cedro
(Cedrela odorata L) proveniente de Satipo. Tesis para optar el título de Ingeniero Forestal.
UNALM - Perú.
Vágner M., Vondráková Z., Fischerová L., Opatrná J. , 2005. Norway spruce somatic
embryogenesis: membrane rafts as compromise between liquid and solidified media. En:
Liquid Culture Systems for in vitro Plant Propagation (Hvoslef-Eide A.K. , Preil W. , eds).
Springer, Dordrecht, The Netherlands. pp 295-302.
Valverde C. L., Dufour, M., Villalobos, V. 1998. In vitro organogenesis in Albizia
guachapele, Cedrel/a odorata and Swietenia macrophylla (Fabaceae, Meliaceae). Revista
de Biología Tropical. 46 (2) : 225-228.
59

Capitulo IX
Vargas, J. and A. Velásquez. 1992. La deforestación y su contribución al desarrollo
ambiental Programa Forestal. Colegio de postgraduados. Chapingo. México. Pp 141-152.
Vasic, D., Alibert, G., Skoric, D. Protocols for efficient repetitiva and secondary somatic
embryogenesis in Helianthus maximil/iani (Schrader). s.l. : Plant Cell Rep. , 2001 . Vol. 20,
págs. 121-125.
Villa lobos V. and Thorpe T. (1991) Micropropagación: conceptos, metodología y
resultados. En: Roca WM y Mroginski LA (Eds) Cultivo de Tejidos en la Agricultura, pp.
127-141 . CIAT, Colombia.
Zimmerman, J. L. (1993) "Somatic embryogenesis: A model for early development in
higher plants." The Plant Cell 5.1 O: 1411-23.
Ziv, M. Bioreactor technology for plant micropropagation. s.l. Horticultura! rewiews. ,
1999. Vol. 24, págs. 1-29.
60

Capítulo X
10. ANEXO
Anexo 1. Tabla de composición del medio MS (Murashigue & Skoog, 1962).
Cantidades para un NOMBRE DEL
FORMULA P.M. (g) litro en
COMPUESTO Masa (mg) Moles (mM)
Compuesto inorgánicos Macro nutrientes Nitrato de K NOs 101.108 1900 18.792 potasio Nitrato de NH4N03 80.04 1650 20.615 amonio Cloruro de KCI2.2H20 147.02 440 2 .993 calc io Sulfato de MgS04.1H20 246.498 370 1.501 magnesio Fosfato de KHzP04.HzO 136.09 170 1.249 potasio monobásico M icronutrientes Sulfato MnS04.H20 169.01 16.9 0.1 manganeso Sulfato de zinc ZnS04.?HzO 287.54 8.6 0.0299 Aci do bórico H3B0 3 61 .86 6.2 0.1 002 Yoduro de Kl 166.01 0.83 40999x1o-;j potasio Sulfato de cobre CuS0.4SH20 249.68 251JQ 0.11JM Molibdato de Na2Mo04.2H20 241.95 2501-19 1.031-JM sodi.o Cloruro de CoCb.6H20 237.93 25 j.Jg 0.1051JM cobalto Sulfato ferroso FeS04.7HzO 278.028 27.8 0.0999 Na2EDTA C1oH14N201oNa2.2H20 372.30 37.3 0.1002 Compuestos orgánicos Aminoácidos Glicina C2HsN02 75.07 2.0 0.0266 Vitaminas Myo-inositol CsH120s 180.2 100 0 .555 Tiamina-HCI C12H11CIN4oS.HCI 337 .3 0.1 2.964x10-4 Ac. Nicotínico C6HsNOz 123.1 0.5 4 .062x1o-~
Piridoxina-HCI CsH1N03.HCI 205 .6 0.50 2.432x1o-j
61